11.2 大量元素:氮、磷、钾、钙、镁、硫
11.2.1 土壤中的氮
氮素(nitrogen):氮是植物重要营养元素,是蛋白质的主要组成万分。植物缺氮时表现为植株矮小,叶色发黄。
蛋白质
①酶蛋白: 在细胞中数量最丰富,起催化作用。
②结构蛋白:存在于植物细胞的胞壁、胞质中。
③贮芷蛋白:存在城植物种子中,供种子萌发时利用。
另外,氮还是叶绿素及许多植物激素的重要成分。
11.2.1.1氮素的来源和分布
土壤中的氮素来源于大气。土壤表层的含氮量通常为0.02-0.5%。地球总氮量的98%存在于地球深处的岩浆岩中,远离我们所生活的土壤-植物-大气-水分环境。因此,我们将重点讨论生物圈中2%的氮素循环。土壤中的大部分氮素来源于生物固氮。
陆地生态系统中大部分的氮存在于土壤中。土壤中的含氮量是森林生态系统中植物含氮量的10到20 倍。土壤中大部分氮以有机分子的形态存在。土壤有机质含有5%的氮,因而土壤氮的分布和有机质的分布是密切相关的。除了使用过大量化肥的土壤,一般土壤中的无机氮(铵态氮和硝态氮)少于全氮的1-2%。与大多数有机氮不同的是,矿质态氮极易溶于水并且很容易被淋失和挥发损失。
11.2.1.2氮素的形态:土壤中的氮素以两类形态存在:无机态氮和有机态氮,大部分的土壤氮以有机态存在。

土壤中的无机态氮含量极不稳定,常常受土壤温度,湿度,植物吸收,微生物活动,有机质含量等因素的影响。因此,无机态氮常常发生显著的季节性变化或昼夜变化。
有机态氮: 有机态氮通常占土壤全氮量的95%以上。有机态含氮化合物以蛋白质,氨基酸和其它复杂的有机氮化合物形态存在。根据它们的可溶性和分解的难易程度可分为:
①可溶性的有机氮:可溶于水的有机氮,如简单的氨基酸,可直接被植物吸收利用,尤其在植物具有菌根时。通常占全氮的5%。
②水解性有机氮:在酸或碱的作用下能水解为简单的可溶性的有机氮含氮有机氮化合物。如蛋白质,多肽,氨基糖等。通常占全氮的25%。
③非水解性有机氮:是有机氮中最稳定的成分,如腐殖质、杂环态氮等。但人们对它的特性还不太了解。大部分有机氮可形成有机-矿质复合体,这种有机态氮在土壤中比未形成有机-矿质复合态的有机氮更稳定。土壤中这部分氮有时可高达50%,
11.2.1.3 氮素循环(nitrogen cycle)
图3所描述的氮素循环表明,土壤中氮素的循环过程有以下几个方面:
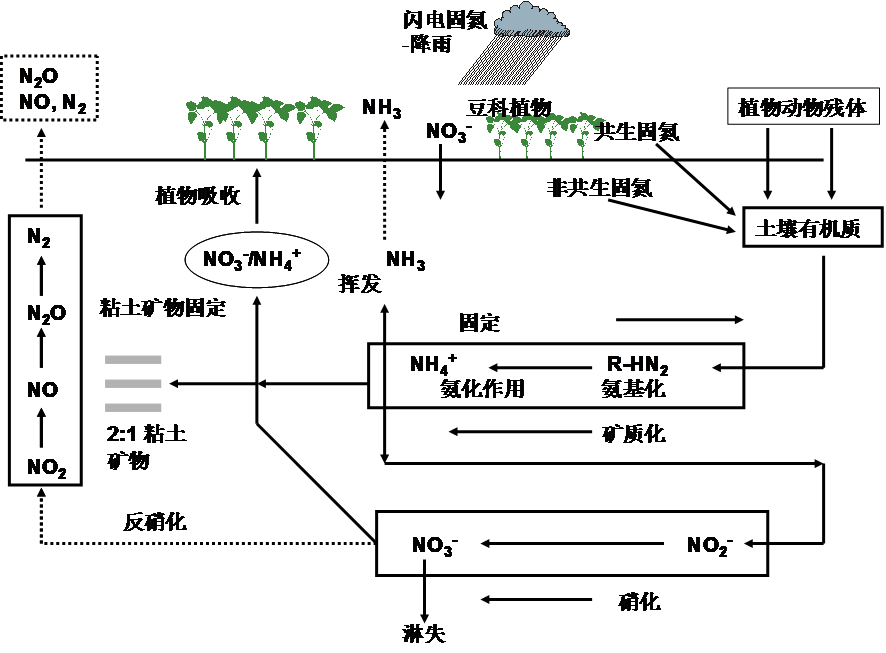
生物固氮(biological nitrogen fixation):一些微生物可将大气中的氮气转化为含氮的有机化合物,从而为各种生物体所利用(见第三章土壤生物)。据估计,陆地生态系统可固定130-180´106 吨的氮,大概是工业固氮(化学肥料)的两倍。
矿质化过程:土壤氮是有机态的含氮化合物分解为无机态氮(铵离子和硝酸根离子)的过程(见土壤有机质一章)。
固定作用(immobilization): 无机态氮(NH4+和 NO3-)转化为有机态氮的过程称为氮的固定。氮的固定包括生物固定(biological fixation)和非生物固定(nonbiological fixation)作用。
①生物固定:微生物分解土壤中的含碳有机化合物获取能量,同时利用土壤中的氮合成微生物体内的氮,从而固定土壤溶液中的铵态氮和硝态氮。当微生物死亡后,又可释放出铵态氮和硝态氮,也可转化为腐殖质等,因此生物固定是氮素的临时贮存。
②非生物固定:NH4+被2:1型粘土矿物固定晶格内部,在森林土壤中相当重要。
氮素的损失:
氨的挥发(ammonia volatilization):在碱性土壤溶液中,铵离子可转化为氨挥发掉。
反硝化作用(denitrification):反硝化作用是氮以气态损失的另一种途径。
11.2.2 土壤中的磷
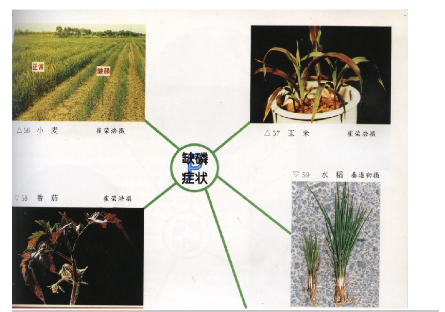
磷是细胞核的成分之一,在果实及种子里含有较多的磷,磷对细胞分裂和植物器官的分化,特别是开花结果起着重要作用。磷对提高植物的抗病性、抗 性和抗旱能力有良好的作用。植物缺磷(图4)抑制体内细胞分裂,使生长缓慢,缺磷体内植物蛋白质合成减慢,有氨基酸积累,同时营养器官内含有大量糖类,有利于叶内合成花青素,使叶子呈紫色、深绿色,根系发育不良,植株表现矮化现象,结实率下降。
土壤磷肥力的难题:土壤缺磷有三方面的原因。
土壤全磷含量低,通常不超过全氮含量的十分之一到四分之一。
磷化合物在土壤中的难溶性导致它很难被植物吸收利用。土壤中的速效磷含量与全磷含量很少相关,所以土壤全磷量不能作为土壤磷素供应水平的确切指标
当有机或无机磷肥施用后,可溶性的磷很容易被固定变为不溶性的。一般每年只有10-20%的磷肥能被植物吸收利用。
11.2.2.1磷素的形态:
无机态磷(inorganic phosphorus):(占全磷的50-75%)
1、水溶态磷(water-soluble phosphorus):土壤溶液中磷的含量很低。通常在贫瘠的土壤中为0.001ppm,在极肥沃的土壤中可达1ppm左右。磷素是以水溶性的磷酸氢根和重过磷酸根进入植物根系的。 H2PO4-和HPO42-是植物吸收的主要形态,但一般认为H2PO4-更容易被植物吸收利用,因为植物根际一般呈酸性。
pH<7.2以H2PO4-为主。
pH>7.2以HPO42-为主。
pH=7.2时两者相等。
2 吸附态磷(adsorped phosphorus):通过通过各种力被土壤固相表面吸附的磷酸根或磷酸阴离子。吸附和解吸处于动态平衡,当溶液中磷被移走(如植物吸收)时,吸附态磷就释放到溶液中,同样,溶液中磷增加,则有部分磷被吸附而呈吸附态磷。
3 矿物态磷(mineral phosphorus):无机磷几乎99%以上以矿物态存在。不同土壤中有不同的含磷矿物存在。
石灰性土壤中主要是磷酸钙盐:氟磷灰石,氢氧磷灰石,碳酸磷灰石。
酸性土壤中发磷酸铁和磷酸铝盐为主:有磷铝石和粉红磷铁矿。
4、闭蓄态磷(occluded phosphorus):酸性土壤中被水化氧化铁所包裹的磷化合物。
土壤有机磷(soil organic phosphorus):土壤中的有机磷一般占全磷的50%。表土中有机磷一般占全磷的20-80%。随着土层深度的增加,有机磷所占的比例减少而无机磷的比例
逐渐增加。
5、肌醇磷酸盐(inositol phosphate)或肌醇(inositol),这部分占全有机磷全量的10-50%。
核酸(nucleic acids):占有机磷全量的0.2-2.5%。
6、磷脂(phosphatides):占土壤有机磷全量的1-5%。
以上有机磷在土壤微生物的作用下,部分最终可分解产生无机磷酸盐,被植物吸收利用。
土壤中的有效磷一般不超过土壤全磷的0.01%。在土壤中极大部分磷以三种形态存在:有机磷,磷酸钙和磷酸铁、铝等。有机磷以活性,迟效性和缓效性有机质形态存在。在碱性土壤里, 无机磷主要是以磷酸钙,磷酸镁等形态存在。在酸性土壤里无机磷主要是以磷酸铁,铝形态存在。这些磷将被缓慢地释放到土壤中。以上组分中的大部分磷由于可溶性低,对植物的有效性很低。
11.2.2.2磷素的循环(phosphorus cycle):土壤-植物系统中磷的循环图5
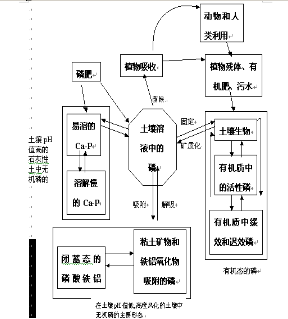
11.2.2.3土壤磷的调节:目的是要提高土壤磷的有效性,其途径如下:
调节土壤酸度到中性范围:因为此时磷的固定最少。
提高土壤有机质:
土壤中磷的固定是影响磷有效性的主要原因。固定主要通过吸附和化学沉淀进行,大多数情况下,磷的固定是不容易逆转的。影响磷固定的因素:
A、土壤矿物:磷的吸附和解吸将受到矿物表面类型的影响。铁铝氧化物,它们的丰度以在高度风化的, 酸性的土壤中最高,可吸附大量的磷。非晶质的氧化物由于表面积大,更容易吸附磷。1:1型粘土矿物如高岭石比2:1型粘土矿物如伊利石更容易吸附磷,因为它们含有更多的铁铝氧化物。石灰性土和钙饱和的粘土含有较低的可溶性磷,因为磷很容易被沉淀和吸附。相对而言,和中性或碱性土相比,相同表面积的酸性土可固定两倍的磷,且被固定磷的结合强度比在中性或碱性土中高5倍。
B、土壤pH值:在土壤pH极高或极低时,磷都很容易被固定。当pH值保持在6.0-7.0时磷被固定的可能性最小,土壤磷素对植物具有最大的有效性。
C、土壤有机质:通常有机质可阻止磷的固定。
D、土壤中的阴离子和阳离子效应:由于两价的阳离子比一价的阳离子吸附力大,因而对磷的吸附力也强。如上所述,由于无机和有机阴离子都可以和磷竞争吸附电位,从而导致对土壤溶液中磷的吸附作用降低。阴离子与矿物表面结合能力越强,被吸附的可能性就越大。
实际应用:
当土壤中施用磷肥后,起始为快速吸附,然后反应速率减慢。磷的吸附常常会随着温度的提高而逐渐提高。磷肥在土壤中的残留时间越长有效性越低。为使磷肥的施用满足植物对磷的需求,应注意以下几方面:
a磷肥施用量需要大于植物的需求量。
b注意磷肥的施用方式和深度。 将施入的磷肥集中施于作物可利用的位置, 如采用条施,以减少固定提高磷肥的利用率。将磷肥和氮肥同时施用,也可以提高磷肥的利用率。施用有机肥可提高原有土壤磷的有效性,
c施用含于有机肥中的磷素。
d对树木幼苗接种真菌菌株,可提高磷的利用率。
![]() 11.2.3 土壤中的钾:
11.2.3 土壤中的钾:
钾素(图6)是植物生长必需的关键元素之一,在植物的生物化学和生理生态上起着重要的作用。钾在气孔保卫细胞的泵入和泵出可改变其渗透势,从而调节气孔的关闭。钾可以平衡细胞质中的无机和有机阴离子,对pH值的改变起缓冲作用。钾还参与酶的活动,蛋白质的合成,细胞的分裂以及光合作用。钾能增强植物对环境胁迫的适应力,提高植物的抗旱能力,和提高植物在冬季的抗冻能力。钾还能增强植物的抗病抗虫能力。
11.2.3.1土壤钾的含量;大多数土壤含钾较多,在0.5-2.5%之间。质地较粗的砂质或石英质土壤含钾量低于质地较细,含钾丰富的矿物风化形成的土壤。![]()
11.2.3.2土壤钾的形态:土壤中钾的形态可大致分为四类:
土壤溶液中的钾:土壤溶液中的钾一般在4ppm左右,土壤饱和提取液中的钾在3到156ppm。在干旱或盐碱地中含钾量可能很高。
交换性钾(exchangeable potassium):静电作用带负电的土壤胶体可吸附钾离子(占全钾的1-2%)。
以上两种形态的钾能被植物直接吸收,称速效钾。
非交换性钾(non-exchangeable potassium):缓效钾(占全钾的2-8%),是指存在于膨胀性层状硅酸盐矿物层间和颗粒边缘上的一部分钾。包括天然层状硅酸盐矿物如黑云母和伊利石中的钾和由交换性钾或水溶性钾转变为层间钾。这部分钾在一定条件下可以逐渐解释,供植物吸收利用。
物中的钾:包括白云母,金云母,正长石和微斜长石。钾长石是土壤中含钾最丰富的矿物,但矿物钾是被固定在晶格之间的,因而只能在晶格被破坏后,钾才能释放出来。
11.2.3.3土壤钾的循环:
钾的输入途径主要有大气沉降和矿物风化释放。每年降雨可提供每公顷1到5公斤的钾。在幼年土上, 矿物风化每年可提供每公顷5到10公斤的钾,而砂质,老年土风化提供的钾每公顷不到1公斤。尽管一些土壤全钾含量很高,但其中大部分的钾存在于原生矿物中或是以非交换性钾的形态存在, 因而有效钾的含量并不一定高。一般来说,钾的输入大于输出。一般砂质土,有机土,一些老年、高度风化的土壤由于不断地被淋洗降低了钾的供应,从而可能限制植物的生长。
植物需吸收利用大量的钾,其需要量一般是磷的5到10倍,或和氮的需要量相当。如果地上部分被收获走,从土壤里损失的有效钾的量可能很大。
钾的循环和转化的动态性变化很强。由于植物不断吸收钾以及钾的淋洗,钾不断地但缓慢地从原生矿物中释放出来,变成有效态的钾,以补充土壤溶液中损失的钾。 如果土壤中钾的含量偏高,那么钾就容易被固定。这4种形态的钾在土壤中的分布很大程度上与土壤中的粘土矿物种类有关。如2:1型的粘土矿物比高岭石含钾量高。土壤溶液中的钾可被植物和微生物吸收利用,或被吸附在土壤胶体表面,或从土壤根系区中被淋洗。
11.2.4.土壤中的钙 :
钙对细胞膜的结构形成和渗透性具有特别重要的作用。钙可以提高硝态氮的吸收, 因而与氮的生理代谢相关。钙对细胞的生长和分裂起着重要的作用。缺钙(图7)会抑制幼苗顶端芽苞的形成和发育,以及根尖的形成,从而导致植物生长停止。植物体中的含钙量通常在0.2-1%。
11.2.4.1土壤钙的含量:一般土壤并不缺钙,但在土壤淋洗强烈以及未施石灰的酸性土壤上,也会发生缺钙现象。湿润地区砂质土壤含钙量较少,湿润温带地区的非石灰性土壤含钙量在0.7-1.5%左右。湿润热带地区风化强烈的土壤只含有0.1-0.3%的钙。干旱地区土壤一般含钙量较高。在大多数森林土壤溶液里,钙是主要的阳离子(Fisher和Brinkley, 2000)。土壤中的含钙量在15ppm左右就足以满足植物生长的需求。
11.2.4.2土壤钙的形态:
水溶性钙(water-soluble calcium):土壤水溶液中的钙离子。
交换态钙(exchangeable calcium):胶体吸附的可交换性钙离子。
矿物态钙(mineral calcium):钙长石(CaAl2Si2O3)是土壤中钙最主要的来源。钙也可来自黑云母、磷灰石、及黑色硅质土以及石膏(CaSO4.2H2O)。
11.2.4.3决定土壤钙的有效性的因素:
土壤全钙含量:阳离子交换量低的砂质、酸性土壤全钙含量可能太低而不能满足植物吸收。
土壤pH值:土壤pH值低(土壤溶液中H+离子含量高)将阻碍钙的吸收。
土壤阳离子交换量和钙的饱和度:在酸性土壤上,低饱和度不利于钙的吸收。钙饱和度高意味着土壤酸度适宜植物的生长和微生物的活动,或意味着酸性土壤里可交换性的Al含量低,或在碱土里钠的含量低;
粘土矿物种类:2:1型粘土矿物比1:1型粘土矿物要求钙的饱和度高,才能提供足够的有效钙。例如,蒙脱石钙饱和度达到70%才能提供足够的有效钙,而高岭石只需40%到50%的钙饱和度就可以提供足够的有效钙;
土壤溶液中钙与其它阳离子的比值:过量的NH4+, K+, Mg2+, Mn2+, 和 Al3+等将降低植物对钙的吸收,但NO3-的存在可增加植物对钙的吸收。
11.2.5 土壤中的镁:
镁是叶绿素的成分。叶绿素中的镁通常是植物体中镁总含量的15-20%。镁离子是多种酶的活化剂,还可促进植物对磷的吸收。植物体内ATP能量的转移也需要镁的参与。因而镁是植物新陈代谢所需的重要元素。植物体中镁的浓度变化在0.1-0.4%之间。
11.2.5.1土壤镁的含量:土壤中镁的行为与钙相类似, 一般土壤并不缺镁,但在土壤淋洗强烈的酸性土壤上。在湿润地区的粗质和砂质土壤上,镁的含量只有0.1%,而在干旱和半干旱地区的细质土壤上镁的含量可达到4%。在温带地区土壤中镁的含量一般在5到50ppm。镁的浓度一般是钙的20到50%。在砂质土壤上,特别是施KCl 和 K2SO4肥料的土壤,镁的淋失是一个很严重的问题,因为可溶性的Cl-和 SO42-可促使镁的淋失。11.2.5.2土壤镁的形态
水溶性镁(water-soluble magnesium):土壤水溶液中的镁离子。
交换态镁(exchangeable magnesium):胶体吸附的可交换性镁离子。
矿物态镁(mineral magnesium):黑云母,白云石,蛇纹石等矿物风化可产生镁。次生矿物如绿泥石,伊利石,蒙脱石和蛭石等也含镁。
11.2.5.3易缺镁的土壤:当土壤中的交换性镁低于25-50ppm时,土壤可能缺镁。
阳离子交换量低的酸性,砂质,和淋洗强烈的土壤,常常缺镁(图8)。石灰性且含镁量低的土壤,酸性土施有大量含镁低的石灰的土壤,经常施用大量铵态氮肥和钾肥的土壤,以及植物对镁的需求量很高时,都会产生土壤缺镁的现象。湿润地区的砂质土出现缺镁的可能性最大,因为这些土壤中全镁和交换性镁都较低。在一些强酸性土壤上,交换性铝的含量高时可限制植物对镁的吸收。当铝饱和度超过60-70%时,土壤就会缺镁。 Ca/Mg值大 (超过10:1到15:1) 时,土壤也会缺镁。植物对镁的吸收也受到钾离子和铵离子的干扰,因为镁与铵及钾离子在被植物吸收时可产生竞争作用。
11.2.6.土壤中的硫:
硫是合成氨基酸如半光氨酸,光氨酸,蛋氨酸必需的元素。硫也是联合酶A合成的必需元素之一,从而参与脂肪酸,氨基酸的合成和氧化,以及柠檬酸循环中的中间产物的氧化。叶绿素的合成也需要硫。植物含硫(图9)量一般在0.1-0.5%。
6.1土壤硫的形态:土壤中的硫最初来源于岩石中的金属硫化物。在风化过程中,矿物中的二价硫(S2-)被氧化为硫酸根。
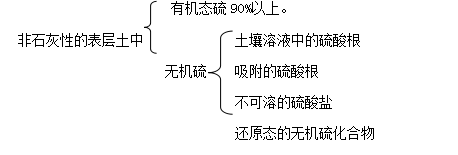
11.2.6.2决定土壤中溶液中硫酸根浓度的因素:硫酸根是硫被植物吸收的最主要形式,虽然植物叶片也可吸收少量的二氧化硫。土壤溶液中硫酸根的浓度,取决于有机硫的矿质化,植物的吸收及硫酸根随着土壤水在土壤剖面的上下移动这些过程之间的总平衡。
硫酸根的淋洗:土壤中阳离子的种类组成将影响硫酸根的淋失。在土壤溶液中含钾和钠离子多时,硫酸根的淋失最显著,其次是钙和镁离子为主的土壤,而在含大量交换性铝的酸性土壤里淋失最小。
硫酸根的吸附:在降雨量大的地区高度风化的土壤里,因含有大量的铁铝氧化物,可吸附的硫酸根,土壤里被吸附的硫可以提供植物生长所需硫的很大一部分,因为这些被吸附的硫是有效的。硫被吸附的机理有:1)阴离子吸附,阴离子可被铁铝氧化物表面,或在pH低的土壤,粘土矿物特别是高岭石发生边缘碎裂而产生的正电荷所吸附;2) Al(OH)x复合体吸附硫酸根;3)在某些条件下具两性反应的土壤有机质带正电荷从而吸附阴离子。
许多土壤因素都会影响到硫酸根的吸附或解吸,如土壤胶体的数量和种类,土壤pH值,硫酸根的浓度,土壤溶液中其它离子的存在,都是影响硫酸根吸附的最重要的因素。
有机硫的矿质化与固定: 有机硫的特性将影响到植物可利用硫的释放。硫的矿质化和固定都是微生物过程,受影响微生物活动的因素影响。有机硫转化为硫酸根称为矿质化,相反则为固定。硫的有效性取决于土壤有机硫的释放以及动植物残余物的降解。若C/S比值低于200:1,则发生硫净矿质化,大于400:1,则产生硫的净固定。简单地说,硫的矿质化受土壤有机质含量,土壤温度,湿度,土壤pH值,扰动,以及硫化酶活性的影响。
11.2.6.3硫的循环(sulfur cycle):硫素的循环比氮素的循环更复杂,因为硫的循环既部分类似于磷的循环又部分类似于氮的循环。和磷酸盐相似,硫酸根离子也被特性吸附,导致大量的硫酸根变成无效的。硫酸盐是土壤中硫的唯一普遍存在的游离态。土壤中硫酸盐的去向和磷酸盐相似:被植物或微生物吸收,形成不可溶性盐类沉淀,产生阴离子吸附,或从根区被淋洗走。但不同于磷酸盐的是,硫酸钙,硫酸铁,硫酸铝是可溶性的,因而森林土壤中硫酸盐的沉淀对硫的有效性并不起很重要的作用。
满足森林植被正常生长一般每年每公顷需从土壤中吸取5-10公斤硫。在未污染的地区,大气每年每公顷可输入1到5公斤硫,并且以硫酸钠或硫酸钙为主的形式进入森林生态系统。在工业污染严重的地区,大气输入的硫可高达每年每公顷20到50公斤, 淋洗损失可高达每年每公顷10到20公斤,并常以酸雨的形式进入森林生态系统。


