8.3 土壤阳离子交换作用
8.3.1土壤阳离子交换吸附作用的概念:
土壤胶体表面所吸附的阳离子(主要是扩散层中的阳离子),与土壤溶液中的阳离子或不同胶粒上的阳离子相互交换的作用,称为阳离子交换吸附作用。阳离子交换作用对土壤中养分的保持和供应起着重要作用。当土壤溶液中阳离子吸附在胶体上时,表示阳离子养分的暂时保蓄,即保肥过程;当胶体上的阳离子解离至土壤溶液中时,表示养分的释放,即供肥过程。
8.3.2.土壤阳离子交换吸附作用的特点
8.3.2.1.阳离子交换吸附作用是一种可逆反应,而且一般情况下,可迅速达成可逆平衡。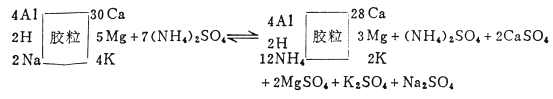
因此,在自然状况下,很难把土壤胶体上某一阳离子完全彻底地代换到溶液中去。同时,土壤胶体上吸附的阳离子也必然是多种多样的,不可能为单一种离子所组成。在湿润地区的一般酸性土壤中,吸附的阳离子有Al3+、H+、Ca2+、Mg2+、K+等;在干旱地区的中性或碱性土壤中,主要的吸附性阳离子是Ca2+,其次有Mg2+、K+、Na+等。
8.3.2.2阳离子交换与吸附的过程以等量电荷关系进行 一个Ca2+可交换两个Na+;一个二价的钙离子可以交换两个一价的氢离子。
8.3.2.3交换反应的速度受交换点的位置和温度的影响:
位置:如果溶液中的离子能直接与胶粒表面代换性离子接触,交换速度就快;如离子要扩散到胶粒内层才进行交换,则交换时间就较长,有的需要几昼夜才能达成平衡。
高岭石类矿物交换作用主要发生在胶粒表面边缘上,所以速率很快;蒙脱石类矿物的离子交换大部分发生在胶粒晶层之间,其速率取决于层间间距或膨胀程度;水云母类的交换作用发生在狭窄的晶层间,所以交换速率较慢。
温度:高温度可加快离子交换反应的速率,因为温度升高,离子的热运动变得更为剧烈,致使单位时间内碰撞固相表面的次数增多。
8.3.3.影响阳离子交换作用的因素
8.3.3.1阳离子的交换能力 是指一种阳离子将胶体上另一种阳离子交换下来的能力,主要决定于阳离子被胶粒吸附的力量(或称阳离子与胶体的结合强度),它实质上是阳离子与胶体之间的静电能。
离子电荷价 :M3+>M2+>M+(M表示阳离子)
离子的半径及水化程度: 同价离子,凡离子本身半径愈大,重量愈大的离子,其代换力和结合强度也愈大,因为离子水化半径越小,其与胶粒间距离也愈小(表5)。
表5 离子价、离子半径及水化程度与交换力的关系
离 子 | 价 数 | 原 子 量 | 离子半径(nm) | 代换力顺序 | |
未 水 化 | 水 化 | ||||
Na+ | 1 | 23.00 | 0.093 | 0.790 | 6 |
NH4+ | 1 | 18.01 | 0.143 | 0.532 | 5 |
K+ | 1 | 39.10 | 0.133 | 0.537 | 4 |
Mg2+ | 2 | 24.32 | 0.078 | 1.330 | 3 |
Ca2+ | 2 | 40.08 | 0.106 | 1.000 | 2 |
H+ | 1 | 1.008 | — | — | 1 |
离子运动速度:凡离子运动速度愈大的,其交换力也愈大。例如氢离子就是这样,而且氢离子水化很弱,通常H+只带一个水分子,即以H3O+的形态参加交换,水化半径很小,因此它在交换力上具有特殊位置。综上所述,阳离子交换力大小的顺序为:
Fe3+>Al3+>H+>Sr2+>Ba2+>Ca2+>Mg2+>Rb+>K+>NH4+>Na+
提请注意的是,这种次序不是绝对不变的,它只是一般的情况。由于土壤中吸附剂(即各种胶体)的不同和浓度不同,都可导致离子交换能力序列的变化。所以严格地说,没有一个统一的序列能够适应任何一种土壤。
8.3.3.2阳离子的相对浓度及交换生成物的性质:阳离子交换作用也受质量作用定律所支配,如果溶液中某种离子的浓度较大,则虽其交换能力较小,同样能把胶体上交换能力较大的其它阳离子代换下来。另外,当交换后形成不溶性或难溶性物质时,或将其交换后的生成物不断除去时,都可使交换作用继续进行。例如:
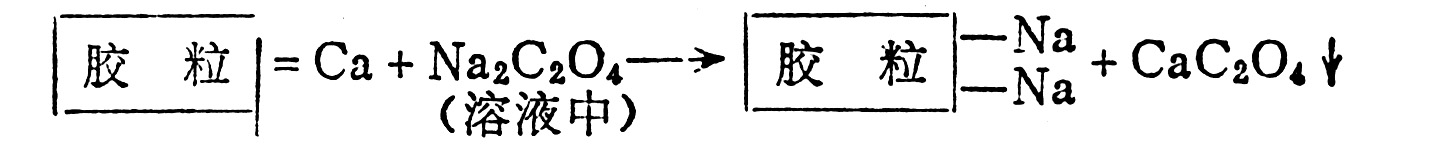 上式中Na+的交换能力虽小于Ca2+,但溶液中有丰富的Na+,而且代换后生成难溶性的草酸钙,使溶液中Ca2+的浓度维持很低,故其交换作用可继续进行。
上式中Na+的交换能力虽小于Ca2+,但溶液中有丰富的Na+,而且代换后生成难溶性的草酸钙,使溶液中Ca2+的浓度维持很低,故其交换作用可继续进行。
又如:
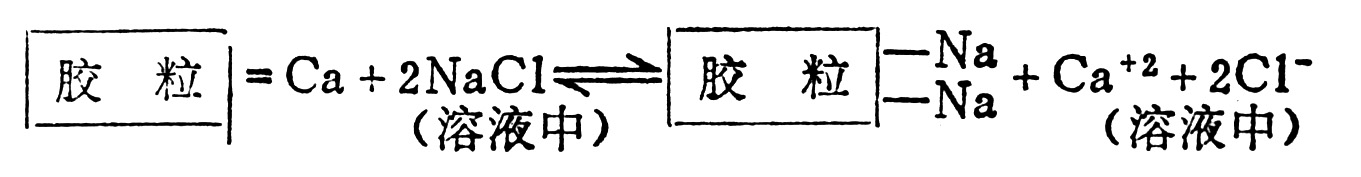
在此,若不把交换过程中产生的Ca2+不断除去,则交换作用很快即达到平衡。但是,只要改变溶液中Na+或Ca2+的浓度,平衡即可破坏。因此,利用这一规律,我们完全有可能控制土壤中阳离子交换作用的方向。
8.3.3.3胶体性质:一般情况下,交换量大的胶体(如蒙脱石)结合两价离子的能力强,结合一价离子的能力稍弱;反之,交换量小的胶体(如高岭石)则结合一价离子能力强,与两价离子的结合能力较弱,即一价离子可将两价离子交换下来。又如:水云母具有六角形网孔(晶孔),容易吸附与其孔径大小相当的K+和NH4+,这些离子一旦进入六角形孔穴,即可发生配位作用,很难出来,只有当晶层破裂时,被固定的K+、NH4+方可重新释放出来。
阳离子交换作用的这些特点和规律是我们施肥和改良土壤等措施的理论依据。例如施用化肥后,可溶性养分的保蓄,以及施用石灰改良酸性土,施用石膏改良盐碱土等措施,都是对这些原理的实际应用。
8.3.4.土壤阳离子交换量
8.3.4.1阳离子交换量(cation exchange capacity)的概念:土壤溶液在一定的pH值时,土壤能吸附的交换性阳离子的总量,称为阳离子交换量(即CEC)。通常以1kg干土所含阳离子的厘摩尔数表示,可写为:厘摩[尔](+)每千克,或简写为:cmol(+)·kg-1。因为阳离子交换量随土壤pH值变化而变化(因可变电荷变化),一般未特别注明时,是以pH为7的条件下测定土壤的交换量。
注:阳离子交换量的大小与土壤可能吸附的速效养分(即阳离子)的容量有关,是土壤保肥力的重要指标。
8.3.4.2影响土壤阳离子交换量的因子:主要是土壤胶体上负电荷的多少,而影响土壤胶体负电荷的,主要是土壤中带负电荷胶体的数量与性质。具体有以下四个方面:
土壤质地(soil texture ):土粒愈细,无机胶体数量愈多,交换量便愈高。故一般地说,粘土交换量大于壤土和砂土,粘土的保肥力也较高。表6。
表6 不同质地矿质土壤的阳离子交换量
质 地 | 砂 土 | 砂 壤 土 | 壤 土 | 粘 土 |
阳离子交换量 cmol(+)·kg-1 | 1~5 | 7~8 | 7~18 | 25~30 |
土壤腐殖质(soil humus):腐殖质的阳离子交换量远远大于无机胶体,其交换量一般为150~500cmol(+)·kg-1。
土壤无机胶体的种类: 蒙脱石类的阳离子交换量最大,水云母类次之,高岭石类的阳离子交换量较小,至于含水氧化铁、铝等胶体的阳离子交换量就更小了,它们在酸性条件下,反而带正电,根本不吸附阳离子。各类土壤胶体阳离子交换量的大小见表8-7。
表7 土壤胶体的阳离子交换量
胶体种类 | 腐殖质 | 蛭 石 | 蒙脱石 | 水云母 | 高岭石 | 含水氧化铁、铝 |
阳离子交换量 cmol(+)·kg-1 | 150~500 | 100~150 | 80~100 | 20~40 | 5~15 | 微 量 |
土壤酸碱反应:土壤反应影响胶体的可变电量,从而影响阳离子交换量。土壤溶液的pH值很小,土壤胶体的负龟荷就少,阳离子交换量也小。例如粘土矿物中联系于破裂边角硅离子的氢氧群,在pH值小于6时,H+的解离很少,pH值增至7时解离增加。而破裂边缘联系于铝离子的氢氧群,同样随pH值增大于而解离H+,只是它开始解离时所要求的pH值较高,pH值为8时,H+才开始显著解离。
几种胶体随pH变化其电荷量的变化见图9
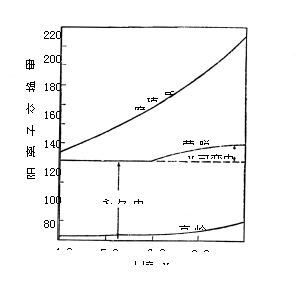
不同土壤胶体的阳离子交换量随pH值增大而增大的情况,见表8。
表8 不同pH条件下土壤胶体的阳离子交换量(cmol(+)·kg-1)
pH4.5 | pH6.4 | pH8.1 | |
沼泽土胡敏酸 | 170.0 | 286.3 | 400.0 |
灰化土胡敏酸 | 234.0 | 410.0 | 508.7 |
黑钙土胡敏酸 | 292.2 | 432.9 | 590.5 |
pH2.5~6 | pH7 | ||
高 岭 石 | 4 | 10 | |
蒙 脱 石 | 95 | 100 | |
我国北方的土壤含蒙脱石、水云母较多,土壤反应又多为中性或微碱性,因此,阳离子交换量一般较高。例如东北的黑土、内蒙的栗钙土的交换量在30~50 cmol(+)·kg-1。
我国华南、西南的红、黄壤地带,无机胶体以高岭石和含水氧化铁、氧化铝为主,土壤酸性大,pH值低,阳离子交换量小,一般每千克土只有十几个厘摩尔,广东的砖红壤的交换量只有5.2cmol(+)·kg-1。
长江中下游发育在冲积母质上的土壤,粘土矿物以蒙脱石、水云母为主,交换量大约为20~30cmol(+)·kg-1;
阳离子交换量和施肥有密切关系。在施肥时不仅要了解作物的需要,同时还要考虑土壤交换量的大小。例如在砂土上施用化肥,由于土壤交换量小,土壤保肥力差,应该分多次施肥,每次施量不宜多,以免养分淋失。对于交换量小、保肥力差的土壤,可通过施用河塘泥、厩肥、泥炭或掺粘土,以增加土壤中的无机、有机胶体,以及通过施用石灰调节土壤反应等来提高土壤的阳离子交换量。
8.3.5. 土壤盐基饱和度
胶体上吸附的阳离子分为两类:一类是致酸离子(如H+ 和Al3+),另一类是盐基离子(如Ca2+、Mg2+、K+、Na+、NH4+等)
8.3.5.1土壤盐基饱和度的概念:指土壤胶体上交换性盐基离子占交换性阳离子总量的百分率。以算式表示为:
如果土壤胶体上的交换性阳离子绝大部分都是盐基离子,即为盐基饱和的土壤,否则就属盐基不饱和。
8.3.5.2影响土壤盐基饱和度的因素:主要是生物、气候,影响盐基淋失和积累强度。
气候:我国南方岩石矿物风化作用强、盐基淋失强,一般为盐基不饱和的土壤(酸性土壤),北方则相反,土壤的盐基饱和度都在80%以上(中性或碱性土壤)。
地上植被类型:一般阔叶树种吸收盐基比针叶树多,通过枯落物归还给土壤的盐基也多,另外,针叶在分解过程中产生相对较多的有机酸,增强了盐基的淋溶作用,使针叶林下耕层土壤盐基饱和度更低于阔叶林土壤。
母岩(mother rock)(或母质mother material):原母质所含盐基的多少对土壤盐基饱和度有较大影响,在相同或类似的生物气候条件下,玄武岩发育的土壤盐基饱和度高于花岗岩。
8.3.5.3土壤盐基的组成:不同类型的土壤,交换性阳离子的组成也不同。
一般土壤中,交换性阳离子以Ca2+为主,Mg2+次之,K+、Na+等很少。如江苏下蜀黄土上的黄棕壤的交换性阳离子,Ca2+占65~85%,Mg2+占15~30%,K+和Na+占2~4%。盐碱土中则有显著数量的Na+,酸性土中有较多的H+和Al3+,在沼泽化或淹水状态下,还有Fe2+、Mn2+等。
8.3.6.交换性阳离子(exchangeable cation)的活度及其影响因素
植物吸收养分是植物与土壤间进行离子交换吸收的过程。这种离子交换吸收的方式有两种:一种是根胶体上的离子与土壤溶液中的离子进行交换;另一种是根胶体与土壤胶体直接进行离子交换,不需要通过溶液作为媒介,这种吸收只有根毛与土壤胶体紧密接触的情况下发生,故又称接触交换。
8.3.6.1交换性离子的饱和度 胶体上某种阳离子占整个阳离子交换量的百分数,即该离子的饱和度。饱和度愈大,该离子的有效性愈大,因为离子与胶体的结合强度随其饱和度的增加而降低,其活度随饱和度的增加而增强。
在相同饱和度下,一价离子的活度(离子活度是指实际能解离出来的交换性离子的数量),远远大于二价离子,因此一价离子的有效性大于二价离子。这是因为一价离子与胶体的结合强度小于二价离子。
在生产实践上,一些有效的施肥措施,其原因之一就是提高了离子的饱和度,增加了离子的有效性。例如,农谚:“施肥一大片,不如一条线”,以及采用“穴施”、“条施”、“大窝施肥”等集中施肥的方法,都是增加离子饱和度,提高肥料的利用率。
8.3.6.2陪补离子的种类 土壤胶体一般同时吸附多种离子,对于其中某一离子来说,其他离子都是它的陪补离子。凡是与土壤胶体结合强度大的离子,其本身有效性低,但对共存的其他离子的有效性愈有利。
浙江农业大学曾对Ca2+以三种不同的陪补离子,在胶体种类和数量相同(交换量相同)的土壤上试验。甲土以H+作为Ca2+的陪补离子,乙土和丙土分别以Mg2+和Na+作为Ca2+的陪补离子,三种土壤处理中Ca2+的饱和度相等,但甲土Ca2+的有效度远较乙、丙土为大,并影响到产量(表9)。
表9 不同陪补离子对交换性钙有效性的影响(小麦盆栽试验)
土壤处理 | 交换性阳离子组成 | 盆中幼苗干重(g) | 盆中幼苗吸钙量(mg) |
甲 | 40%Ca+60%H | 2.80 | 11.15 |
乙 | 40%Ca+60%Mg | 2.79 | 7.83 |
丙 | 40%Ca+60%Na | 2.34 | 4.36 |
8.3.6.3无机胶体的种类 一般来说,在饱和度相同的情况下,各营养离子在高岭石上的有效性大,蒙脱石次之,水云母最小。但个别情况也有例外。
8.3.6.4离子半径(ionic radius)大小与晶格孔穴(lattice hole)大小的关系 K+的半径为0.133nm,NH4+半径为0.143nm,它们的大小都近于晶格孔隙大小,容易固定于晶孔中,降低有效性。蒙脱石表面的硅四面体数量多,故这种晶孔固定作用含蒙脱石多的土壤多于含高岭石多的土壤。
8.4 土壤阴离子的交换吸附作用
8.4.1.阴离子的交换吸附作用概念:
8.4.1.1阴离子的交换(anion exchange):土壤胶体表面的阴离子与土壤溶液中的阴离子发生互换和过程。阴离子交换作用有些也是可逆反应,能很快达到平衡,而平衡的转移也受质量作用定律的支配。
土壤阴离子的吸附:被吸附的阴离子往往转而固定在土壤中,所以在土壤学中也常常把阴离子交换吸附和其后的化学固定作用,总称为阴离子的吸附作用。
8.4.1 2阴离子的吸附(anion adsorption):在很大程度上决定于胶体矿物硅酸与铁、铝氧化物的比例(即胶体矿物全量化学组成中SiO2与Fe2O3+Al2O3的克分子比率,简写SiO2/R2O3)。S. Mattson认为SiO2/R2O3=1时,阴离子吸附较强;SiO2/R2O3=2时,阴离子与阳离子吸附相当;SiO2/R2O3=3或更大时,阴离子吸附减弱,而阳离子吸附增强。土壤中1∶1型粘土矿物愈多,铁、铝、锰的氢氧化物的无定形胶体物质愈多,pH值愈低,则阴离子吸附愈强。
8.4.2. 阴离子的交换吸附力
根据实验结果,土壤中各种阴离子被吸附的能力,可分为以下三类:
8.4.2.1.易于被土壤吸附的阴离子 如磷酸离子(H2PO4-、HPO42-、PO43-)、硅酸离子(HSiO3-、SiO32-)及某些有机酸的阴离子。这一类的阴离子常和土壤中的阳离子进行化学反应,产生难溶性化合物而被固定在土壤中,即所谓化学固定作用。磷酸的化学固定是土壤养分上极为突出的问题。
8.4.2.2.很少被吸附或不能被吸附而产生负吸附的阴离子 如Cl-、NO3-、NO2-等。这些阴离子在土壤溶液中的浓度往往超过它们在胶粒与溶液界面上的浓度,即负吸附现象。
8.4.2.3.介于以上两者之间的阴离子 如SO42-、CO32-及某些有机酸的阴离子。
据实测,阴离子吸附能力的次序如下:
F ->草酸根>柠檬酸根>H2PO4->HCO3->H2BO3->CH3COO->SCN->SO42->Cl->NO3-
B.A.柯夫达提出了下列阴离子吸附的一般顺序:
OH->PO43-≥SiO32->SO42->Cl->NO3-
8.4.3. 土壤阴离子的负吸附(soil anion negative adsorption):
指距带负电荷的土壤胶粒表面愈近,对阴离子的排斥力愈大,因此,负电胶粒表面的阴离子数量反较自由溶液少。前已说明,土壤中大多数胶体或大多数情况下带负电,根据库仑定律,这些带负电的胶粒必然对阴离子产生负吸附现象。只是由于土壤中多少带有一些正电荷,以及阴离子的化学固定作用而掩盖了负吸附。


