第八章 土壤胶体与土壤离子交换.ppt(下载附件 2.01 MB)
要求
[1]掌握土壤胶体的概念及特征;
[2]掌握土壤胶体的类型;土壤阳离子交换作用的概念、特点和影响因素;
[3]掌握阳离子交换量、盐基饱和度等概念及其影响阳离子交换的因素;
[4]了解2:1型粘土矿物和1:1型粘土矿物的物理和化学特性以及与肥力关系;
[5]了解我国土壤粘土胶体的分布规律。
第八章 土壤胶体和土壤离子交换
8.1 土壤胶体
土壤具有吸附和交换阳离子、阴离子的能力,这种作用主要取决于土壤胶体以及存在于土壤溶液中的各种离子。土壤中离子交换作用的强弱和交换量的大小,与土壤胶体的种类、数量、结晶构造以及环境条件有密切关系,它对土壤养分的保持、供应及土壤其它性质影响很大。胶体分散系是土壤中最活跃的部分,它是土壤各种理、化性质的基础。
8.1.1.土壤胶体(soil colloid)的的概念:
颗粒直径(非球形颗粒则指其长、宽、高三向中一个方向的长度)在1~100nm范围内的带电的土壤颗粒与土壤水组成的分散系。通常情况下,直径小于2µm(或1µm)的土粒便具有胶体的性质,因而被视为土壤胶体颗粒。
8.1.2.土壤胶体的构造(图1)
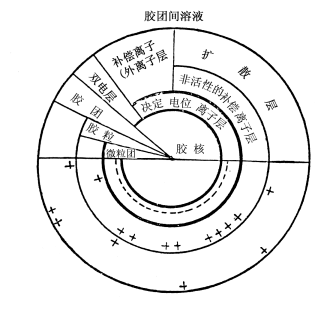
8.1.2.1胶核:
是胶粒的基本部分。土壤胶体胶核的成分由二氧化硅、氧化铁、氧化铝、次生铝硅酸盐、腐殖质等的分子团所组成。
扩散层的离子具有较强的交换能力,容易和土壤溶液中的其它相同电荷的离子互相取代。扩散层以内的部分,即从胶核到非活性补偿离子层,称胶粒。连同扩散层的全部构造,则称胶团或胶胞。
注:把土壤胶粒完全理解为图1的球形构造,显然是错误的。现代土壤学的研究说明,只有土壤有机胶粒,或无定形的氢氧化铁、氢氧化铝、含水氧化硅和水铝英石等矿质胶粒可以认为近似圆球形构造。而土壤中大多数矿质胶粒,例如层状硅酸盐类粘土矿物通过X-射线和电子显微镜的研究,已经明确是层状构造图2。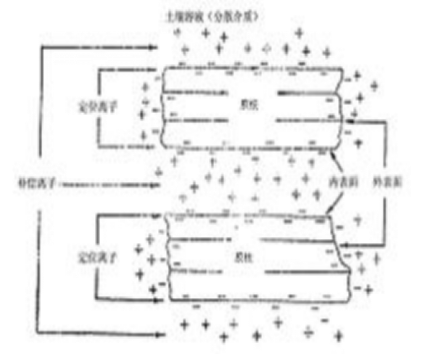
8.1.3.土壤胶体的性质
8.1.3.1土壤胶体具有巨大比表面积(specific surface area)和表面能(surface energy):
单位质量或体积物体的总表面积称为比表面积或比面,单位cm2·g-1或cm2·cm-3。物体分割得愈细小,单体数愈多,总面积愈大,比面也愈大(表1)和(表2)。
表1 1cm3物质表面积随分散度变化的情况
立方体边长 (cm) | 立方体数目 | 总表面积 | 比表面积 (cm2·cm-3) |
1 | 1 | 6cm2 | 6 |
0.1 | 103 | 60cm2 | 6×10 |
0.01 | 106 | 600cm2 | 6×102 |
0.001 | 109 | 6000cm2 | 6×103 |
0.0001 | 1012 | 6m2 | 6×104 |
0.00001 | 1015 | 60m2 | 6×105 |
0.000001 | 1018 | 600m2 | 6×106 |
0.0000001 | 1021 | 6000m2 | 6×107 |
表2 各粒径土粒的比面
土粒 (粒径mm) | 比表面积 (cm2·g-1) | 土粒 (粒径mm) | 比表面积 (cm2·g-1) |
粗砂粒(1) | 22.6 | 粘粒(0.0005)500nm | 45,200 |
中砂粒(0.1) | 226 | 胶粒(0.0001)100nm | 226,000 |
细砂粒(0.01) | 2,260 | 胶粒(0.00005)50nm | 452,000 |
粘粒(0.001) | 22,600 | 胶粒(0.00001)10nm | 2,260,000 |
实际土壤的颗粒形状多种多样,只有砂粒近似球形,但也不是光滑的球体,表面大多凹凸不平。如上所述,大部分粘粒、胶粒和一部分粉砂粒是片层状。因此,实际土壤胶体的表面积和比面都大于单纯的光滑的球体。
由于土壤胶体具有巨大表面积,从而具有巨大的表面能。因为物体表面分子与物体内部分子所处的条件不同,颗粒周围吸力不均衡,或不饱和,从而使表面分子产生一定的剩余自由能(称表面能)。表面能是胶体产生物理吸附(如对液体分子或气体分子吸附的原因。
8.1.3.2土壤胶体的带电性:
土壤中所有胶粒都是带电的(胶体的基本条件),这是土壤产生离子吸附和交换、离子扩散、酸碱平衡、氧化还原反应以及胶体的分散与絮凝等现象的根本原因。而这些反应都直接或间接关系到土壤的水、肥、气、热性质,因此,土壤胶体的带电性对土壤肥力性质有重要影响。胶体电荷的来源由以下几种途径:
同晶异质代换作用(isomorphic substitution):层状铝硅酸盐粘土矿物在形成时,中心离子可以被其它相近或稍大的同性离子代换而产生电荷,但矿物的结晶构造型式不变。
例如四面体中的硅可被铝代换,八面体中的铝可被铁、镁代换,晶体中产生了剩余负电荷,使晶层带负电。由于这种电荷是晶体组成本身产生的,它不随介质pH值的变化而变化,所以称为永久负电荷(permanent negative charge)或内电荷。
晶格破碎边缘的断键 在矿物风化破碎的过程中,晶体晶格边缘的离子有一部分电荷未得到中和,而产生剩余价键,使晶层带电。例如晶格在硅层或铝层截面上断裂,Si—O—Si,Al—O—Al在断裂后,断面上留下Si—O-、Al—O-,从而带负电。
胶体表面分子的解离或吸收离子而带电荷
结晶的粘土矿物大部分表面都裸露着—OH原子团,在一定条件下,当H+解离后,则使胶核带负电,如H2SiO3和层状硅铝酸盐粘土矿物中解离H+后使胶核带负电。当OH-发生解离时,则胶核带正电,如Fe(OH)3或Al(OH)3中的OH-解离后则带正电。这种作用与普通酸碱解离相似,受溶液的pH影响,因此称为可变电荷(variable charge)。
Fe(OH)3或Al(OH)3解离H+而成为带负电的胶体,还是解离OH-而成为带正电的胶体主要取决于溶液的pH值。
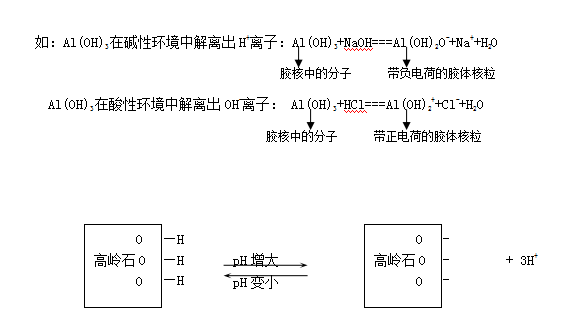
腐殖质类有机胶体,其分子上的羧基和酚羟基上的H+解离而带负电,分子上胺基则可吸收H+而带正电荷。
当土壤胶体解离阳离子和阴离子数量相等,即胶体的正负电荷相等时,此时胶体悬液的pH值称为等电点(isoelectric point)。在土壤pH5—8的条件下,腐殖质和铝硅酸盐等胶体都带负电,表现为对阳离子的吸附,只有Fe(OH)3和Al(OH)3带正电,吸附阴离子。故土壤胶体在通常情况下以带负电为主。
8.1.3.3土壤胶体的分散(dispersion of soil colloid)和凝聚(gelatination of soil colloid):
胶体可以有两种状态。一种是溶胶,即溶液状态的胶体,胶粒互相排斥,分散在溶液里;一种是凝胶,即絮状无定形沉淀状态的胶体,胶粒互相凝聚在一起成较大的颗粒。
土壤胶体由于大多带有负电荷,相互具有负电位,而互相排斥,不易凝聚。要使胶体凝聚,必须减小动电电位,减小扩散层厚度,以减小排斥力和胶团之间的距离。如电解质可使溶胶发生聚沉,因为加入电解质后,离子浓度增大,部分扩散层中的反离子进入非活性层,使扩散层变薄,动电电位随之降低。当扩散层全部反离子都转入非活性层内,此时的ζ电位下降到零,胶粒呈电中性,很快凝聚沉淀。实验证明动电电位下降到零以前,就开始凝聚。电解质对胶体的凝聚作用受以下因素的影响:
电解质的浓度愈大,愈能有效地中和异电胶体的电性,愈能减小扩散层厚度,使胶粒凝聚。
电解质中异电离子的价数愈高,聚沉能力愈大,三价离子大于二价离子,二价离子大于一价离子;同价离子中,凝聚力大小与本身半径和水化半径有关,凡离子本身半径大或水化后半径小的离子凝聚力大,相反则小。电解质阳离子对于负电胶体的凝聚力大小顺序如下:
Fe3+ > Al3+ > Ca2+ > Mg2+ > H+ > K+ > NH4+ > Na+
阳离子凝聚力的大小,可从含有不同阳离子的电解质促使胶体凝聚时的浓度来证明,表3。
表3 0.5µm粘土悬浊液开始凝聚时的电解质浓度
电解质名称 | 开始凝聚时的浓度(mol·L-1) | 电解质名称 | 开始凝聚时的浓度(mol·L-1) |
NaCl | 0.0250~0.0125 | CaCl2 | 0.0006~0.00025 |
NH4Cl | 0.0250~0.0125 | AlCl3 | <0.000042 |
KCl | 0.0250~0.0125 | FeCl3 | <0.000042 |
MgCl2 | 0.0006~0.00025 | HCl | 0.001~0.0005 |
注:胶体的凝聚作用,有的是可逆的,有的是不可逆的。一价阳离子所引起的凝聚作用是可逆的,二价和三价阳离子引起的凝聚作用是不可逆的。因为二价或三价阳离子凝聚力强,它们具有两个以上的价键,可同时粘结在两个胶粒上,使胶粒联系得极紧密,使水分子不易渗入粒间孔隙而分散胶粒。只有在机械力的辅助下,才能破坏其胶结而水化。而一价阳离子,如Na+,不能同时连接两个胶粒,而且水化能力大,一旦遇水即可充满水膜而使胶粒分散开来。阳离子这种凝聚作用的可逆和不可逆,与土壤结构的稳定性有关,钙离子和腐殖质胶结的结构具有水稳性,而钠离子胶结的不具水稳性,就是这个道理。
农业上促进土壤团粒结构形成措施的理论解释:土壤干燥、冻结过程中,水膜消失,也就加大了电解质浓度,减小扩散层厚度,使胶粒互相凝聚而形成结构。生产上晒垡、冻垡等措施也就起了这个作用,所以晒、冻垡有利于土壤形成结构;相反,土壤水分过多,土壤溶液电解质浓度相应减小,扩散层加厚,胶粒互相排斥而成溶胶状。常年泡水的沤水田、烂泥田,土粒分散,缺少结构,通气性差,栽秧后易产生浮秧,就是因为胶粒分散,土壤不沉实。这种情况下,施用石灰(CaO)、石膏(CaSO4),增加Ca2+浓度,对沉实土壤,改良土性,有明显效果。


