一、SO2
1、SO2的来源
自然源是火山爆发和还原态硫化物(H2S)的氧化;人为源是化石燃料(主要是煤)的燃烧。其次是有色金属冶炼、石油加工和硫酸制备等。
主要化学反应
4FeS2+11O2→2Fe2O3+8SO2 CH3CH2CH2CH2SH→H2S+2H2+2C+C2H4
2H2S+3O2→2SO2+2H2O
2.SO2的迁移转化
(1)SO2的催化氧化
2SO2+2H2O+O2→2H2SO4 SO42-+2NH4+ →(NH4)2SO4 2SO2+O2→2SO3
(2)SO2的光化学氧化 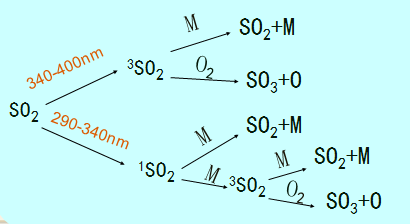
(3)SO2的氧化条件 在阴天,相对湿度高和颗粒物浓度大的条件下,SO2的转化途径以催化氧化为主;在晴天,相对湿度低,大气中同时含有NOx和CH化合物时,尤其是颗粒物含量少时,SO2的转化途径以光化学氧化为主。
3.硫酸盐气溶胶的生成
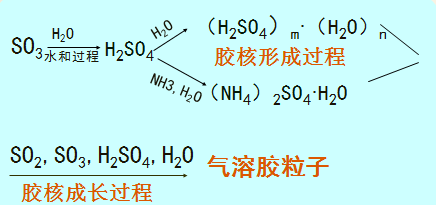
SO2与颗粒物有协同作用。颗粒物是SO2的凝结核,形成气溶胶粒子,造成更大的危害。
4.SO2的归宿
大气中的SO2经过一系列的化学转化之后,最终形成硫酸或硫酸盐,然后以湿沉降或干沉降的方式降落到地球表面。
二、NxOy的来源及化学转化
1、NOx的主要来源
来自于化石燃料高温燃烧和硝酸、化肥等生产排放的废气,以及汽车排气。
2、NOx的迁移转化
(1)NO的主要转化途径
2NO + O2 → 2NO2 NO + O3 → NO2 + O2 NO + H2O → NO2 + OH NO + RO2 → RO + NO2
NO + NO2 + H2O → 2HNO2 HNO2 + hv → NO + OH
(2)NO2的主要转化途径
NO2 + hv → NO + O NO2 + OH + M → HNO3 +M NO2 + RO2 + M → RO2NO2(PAN)
NO2 + O3 → NO3 + O2 NO2 + NO3 + M → N2O5 + M N2O5+ H2O → 2HNO3
NH3 + HNO3→ NH4NO3 2NO2+ NaCl → NaNO3 + NOCl
3.NOx的归宿
NOx的最终归宿是形成硝酸和硝酸盐。大颗粒的硝酸盐可直接沉降到地表或海洋中。小颗粒硝酸盐被雨水冲刷也沉降到地表和海洋中。


