原理
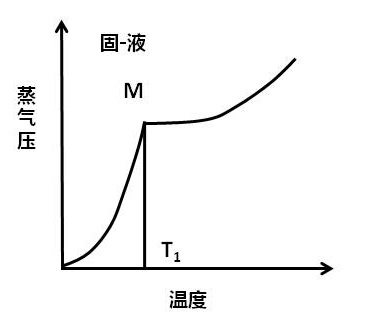
固液两相蒸汽压一致,固液两相平衡共存,这时的温度T即为该物质的熔点。
纯粹的固体有机化合物一般有固定的熔点。即在一定的压力下,固液两态之间的变化非常敏锐,自初熔至全熔(熔点的范围称为熔程)温度不超过0.5-1度。
如果该物质含有杂质,则其熔点往往比纯粹的低,且熔程较长。故测定熔点对于鉴定纯粹有机物和定性判断固体化合物的纯度具有很大的价值。
熔化过程
化合物初始是为固相,加热使温度上升达到熔点。开始有少量液体出现,而后固液平衡。继续加热,温度不再变化,此时加热使固体不断转变为液体,两相间仍为平衡,最后的固体完全熔化后,继续加热则温度线性上升。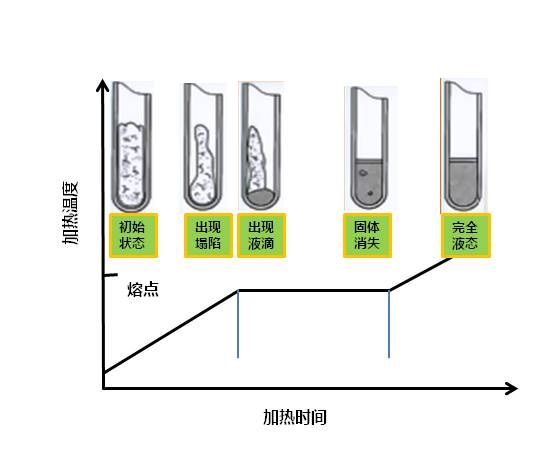
熔点测定仪

最简单廉价的熔点测定仪是使用提勒管测定熔点,在提勒管中加入浓硫酸,样品管粘附在温度计上,用酒精灯加热,记录温度。
简易操作的数字化仪器逐渐丰富实验室,数字熔点仪使用广泛!但是使用前需要温度校正!
操作要点
熔点管本身要干净,管壁不能太厚,封口要均匀。
样品一定要干燥,并要研成细粉末,往毛细管内装样品时,一定要反复冲撞夯实,管外样品要用卫生纸擦干净。
将样品放入熔点测定仪,升温速度不宜太快,特别是温度接近样品熔点。开始是可以稍快5oC/min, 接近熔点时1-2 oC/min,对未知物的熔点,第一次可快速升温,测定化合物的大概熔点。
熔点的记录,熔点是记录一个温度范围(熔程,熔距)。
样品开始塌落是熔化开始的信号,熔化开始于看到第一滴液体,记下此时的温度,到所有晶体完全消失呈现透明液体时再记录这时温度,这两个温度就是样品的熔点范围。
熔点的测定至少要重复两次,每一次用新的熔点管装样品。第二次测定时,要等仪器温度冷至熔点30oC以下再进行。
注意事项
熔点管必须洁净,管底封好。
样品要研碎,填装要实,否则会产生空隙,不易传热,造成熔程变大。
样品不干燥或含有杂质,会使熔点偏低,熔程变大。
样品量(1 cm),太少不便观察,而且熔点偏低;太多会造成熔程变大,熔点偏高。


