家兔失血性休克及抢救
【实验目的】
1.知识目标:能准确阐明休克的发生机理及临床表现;
2.技能目标:能熟练完成失血性休克动物模型的复制;
3.素质目标:通过本实验的学习,学生能综合分析休克的各种急救治疗措施的效果差异,关心和爱护休克病人。
【实验原理】
休克是多病因、多发病环节、有多种体液因素参与,以机体循环系统功能紊乱,尤其是微循环功能障碍为主要特征,并可能导致器官功能衰竭等严重后果的复杂的全身调节紊乱性病理过程。休克的微循环学说,认为各种原因引起的休克都可导致微循环障碍,休克发病的关键不在于血压,而在于血流,因而提出在改善微循环、保证组织有效灌流的基础上采用血管活性药物治疗休克。本实验通过动脉放血复制失血性休克,观察休克过程中机体的变化,通过实验了解抢救休克的治疗原则。
【材料与方法】
一、实验对象:家兔,体重2.0~3.0kg
二、器材、药品
手术器械、输液输血装置、气管插管、动脉和静脉导管、输尿管插管、微循环观察装置、lml、20ml和50ml注射器、BL-420生物信号采集与处理系统或BI-2000医学图像分析系统(观察微循环)、20%氨基甲酸乙酯溶液或1%普鲁卡因、0.2%肝素生理盐水、654-2注射液、去甲肾上腺素注射液、生理盐水、灌流液(台氏液+1%明胶)。
三、方法与步骤
(一)动物准备
1.麻醉与固定:静脉注射20%氨基甲酸乙酯麻醉,仰卧固定。
2.颈部手术:分离气管、左侧颈动脉及右侧颈外静脉。气管插管。耳缘静脉注射肝素1000U/kg抗凝。右侧颈外静脉插管,导管通过三通管连输液瓶和压力换能器,用来测定中心静脉压(CVP)和输液。在测压前,阻断压力换能器侧管,使导管与输液瓶相通,缓慢滴注生理盐水(5~10滴/分),保持静脉通畅。左侧颈总动脉插管,接上三通管,记录血压。经气管插管描记呼吸。
3.输尿管插管:手术及插管方法见第三章第八节“输尿管插管术”。
4.肠系膜微循环观察:腹正中沿腹白线作约150px长的纵行切口,打开腹腔后,在腹腔内可见淡粉红色、肠壁较饱满的盲肠,找到盲肠游离端后,将盲肠轻轻提起,沿盲肠系膜轻轻地将一段游离度较大的回肠和肠系膜拉出腹外(注意!找盲肠时切忌乱翻和用力牵拉,以免肠系膜血管收缩,血流停止)。用止血钳夹住腹部切口,以防肠管外溢。然后将兔向右侧卧位固定,将肠系膜放置在BI2000微循环恒温灌流盒内,在显微镜下观察肠系膜微循环。BI2000医学图像分析系统使用方法参见第二章第六节“七”。
5.将电极分别插入肢体踝部皮下。导联线连接方法参见第二章第六节有关心电图标准导联部分。
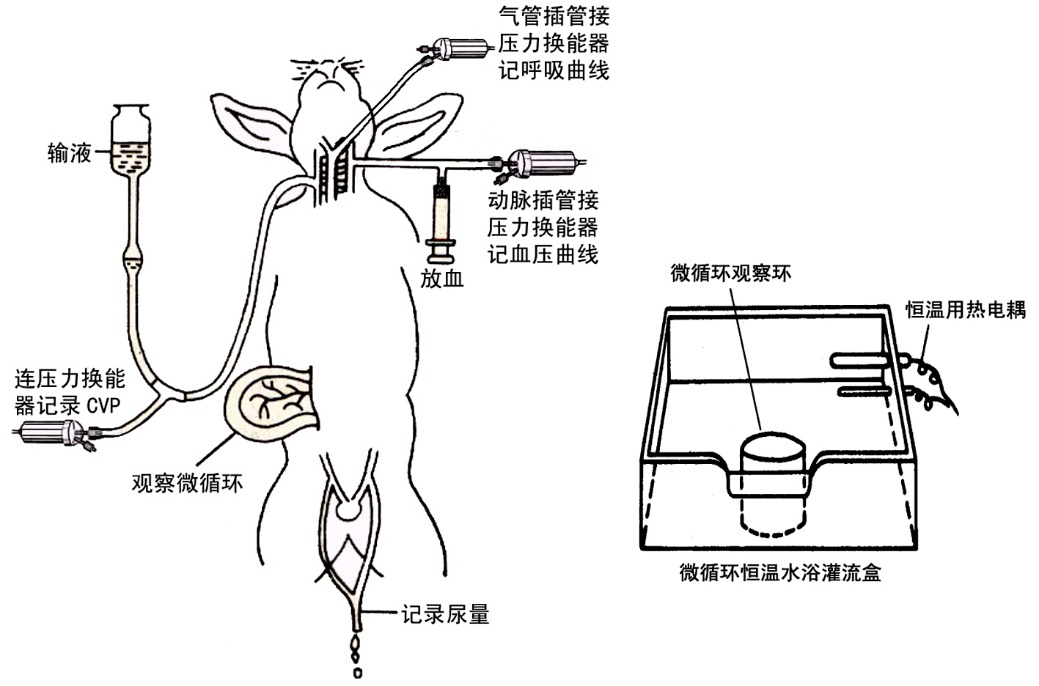
图7-2实验装置连接示意图
(二)仪器连接与调试(如图7-2所示)
1.BL-420生物信号采集与处理系统连接及软件使用
(1)选择“输入信号”菜单中的“1通道”菜单项,选中“张力”,描记呼吸。
(2)选择“输入信号”菜单中的“2通道”菜单项,选中“压力”,描记血压。
(3)选择“输入信号”菜单中的“3通道”菜单项,选中“压力”,描记CVP。
(4)选择“输入信号”菜单中的“4通道”菜单项,选中“心电”,描记心电图。
(5)用鼠标器左健单击工具条上的“开始”命令按钮。
(6)在控制参数调节区,1通道增益为1000,时间常数(t)为DC,高频滤波(F)为30Hz。2通道增益为50,时间常数为DC,高频滤波为30Hz。3通道增益为200,时间常数为DC,高频滤波为30Hz,速度选择50ms/div。4通道增益为1000,时间常数为0.1-0.01s,高频滤波选择100Hz,速度选择50ms/div。
(7)在增益、标尺调节区,将血压、呼吸、中心静脉压波形调节到适当大小。
2.BI2000医学图像分析系统连接及软件使用见第二章第六节。
(三)观察指标
皮肤粘膜颜色,血压、呼吸、心率、中心静脉压、心电图、尿量、肠系膜徽循环。
【观察项目】
1.记录处理前的上述指标。
2.放血:打开颈总动脉插管与注射器相连的侧管,使血液从颈总动脉流入注射器内,一直放血到5.33kPa(40mmHg)时,调节注射器内放出的血量,使血压稳定在该水平。维持血压在5.33kPa(40mmHg)20min,观察注射器中血量的增减、失血期间动物各项指标改变。如果时间允许则可继续延长时间进行观察。
3.抢救:同一实验室分四组进行抢救,将液体或血液倒入输液瓶内,快速输液(50滴/分)进行抢救。输完后再次测定前述各项指标。也可根据现有条件自行设计抢救方案进行抢救。
(1)失血量等量的生理盐水+失血全血+去甲肾上腺素0.75mg/kg体重。
(2)2倍失血量生理盐水+失血全血+654-2(山莨菪碱)lmg/kg体重。
(3)2倍失血量生理盐水。
(4)失血全血。
输液、输血后再观察记录抢救过程中各项指标变化。
【实验结果】
打印同步记录的血压、ECG、呼吸、CVP等曲线,绘制三线表填入所测各项指标的数据。
【注意事项】
1.麻醉要深浅适度,过深,可严重抑制呼吸;过浅,动物疼痛挣扎,影响观察,甚至引起神经源性休克。
2.牵拉肠袢要轻,以免引起严重低血压,外周循环衰竭。
3.尽量减少手术出血,可在同一实验室不同组之间适当分工以减少手术创伤,如有的小组只观察微循环和血压。
4.动脉套管中,插管前先加入一定量的肝素溶液。静脉导管一经插入,应立即缓慢滴注生理盐水。在插管前,动脉套管、静脉导管、与输液瓶相连的管道内应充满液体。
5.本实验因手术较多,宜分工协作,以保证实验成功率。
6.观察微循环时,要分清动脉、静脉及毛细血管,选好标志血管,固定视野。
实验流程:
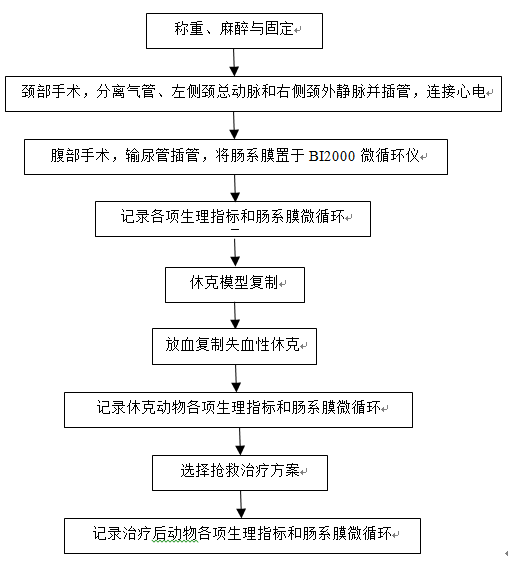
【要求及思考】
1.学生课前应复习《休克》的内容。
2.本实验是否造成休克动物模型,根据何在?
3.讨论第十一章病例五、六、八、九,各实验组安排同学作课堂发言。
【作业题】
1.以本实验结果说明失血性休克的发生发展。
2.结合理论知识,除了本实验对动物采用急性放血方法造成休克之外,请你设计出几种简便易行复制休克动物模型的方法。
附录 肠系膜微循环观察
1.向恒温水浴灌流盒内注入38℃左右灌流液。该灌流液由台氏液加入1%明胶配成。
2.选择一段游离度较大的小肠袢,从腹腔拉出后,放入恒温灌流盒的小浴槽内,使肠系膜均匀平铺在有机玻璃凸形观察环上,压上固定板,调整灌流液平面,使液面刚覆盖过肠系膜,用透射光源或侧射光源在显微镜下观察。
3.在显微镜下直接观察和记录放血前后肠系膜微循环的状况:
分清肠系膜各种血管,包括动脉、静脉和毛细血管(仅能通过一个红细胞的微血管),观察血流速度,血管口径(可用测微器测定)及视野下某一固定区域内毛细血管袢数目,找出标记血管,以便固定视野作动态的前后比较。
(1)选取一支微动脉与微静脉(从血流方向加以区分),观察二者口径大小和口径比值,并注意相应区域内的毛细血管开放数目及血流速度,血流速度可用线状流(最快),线粒流(快),粒线流(较快),粒流(较慢),粒缓流(慢),粒摆流及血流停滞来记述。这一区域选一根血管作标记,移动观察时,仍可找到。
(2)注意有无红细胞聚集?如有聚集,聚集程度可用3~5个红细胞相连成串(轻度),呈缗钱状排列(中度),呈絮状(重度)等记述。
(3)除上述观察血管口径、血流速度及红细胞聚集程度外,还可观察到以下变化:
①血浆流:失血后部分毛细血管内红细胞消失,仅见血浆流动。
②白细胞附壁:失血早期,血流缓慢时在小静脉壁上可见白细胞滚动和附着。
③微血管周围斑点状出血:在失血晚期可观察到毛细血管周围有出血灶。


