纳米组装漆酶传感器
Electrochemistry of Nanoscale Assembled Catalase and Investigation on Its Catalytic Behaviors
实验目的:
(1) 掌握多壁碳纳米管@壳聚糖生物模拟膜的制备方法;
(2) 了解漆酶−多壁碳纳米管@壳聚糖修饰膜分别对溶解氧的电催化还原机理;
(3) 掌握基于流体动力学的恒电位安培i~t曲线检测技术;
(4) 测定漆酶酶促反应催化对苯二酚的电化学表观米氏常数;
(5) 比较蛋白质层层静电自组装和包埋法的优缺点。
实验原理:
漆酶(Laccase,简称Lc)在结构上是一种结合4个铜离子的蛋白质(如下图所示)[1],属于铜蓝氧化酶,蓝色,分子量约12万(120 kDa),存在于菇、菌等菌类微生物及植物中。其在功能上是借助氧将对苯二酚(氢醌)氧化成对苯醌的酚氧化酶的一种,亦称为对苯二酚氧化酶。田彦六郎(Rokuro, 1883)在漆树的树液中发现能使“树漆”氧化硬化的酶,后来贝特兰德(Gabriel E. Bertrand, 1894)详细地研究了东南亚地区产漆中的酶,并统一命名为漆酶。漆酶可存活于空气中,将存在于漆树永延液汁中的漆酚、氢化漆酚氧化为黑色物质,反应的唯一产物就是水,因此本质上是一种环保型酵素。由于这几年环保意识逐渐被人所重视,因此近年来漆酶也成为众多学者的研究对象。
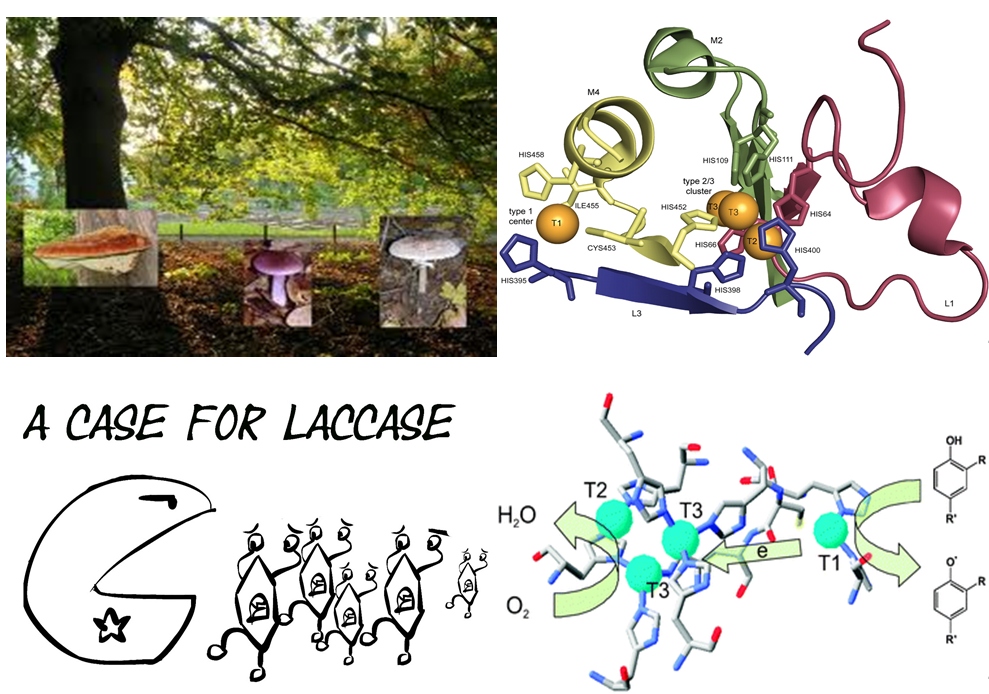
漆酶独特的酶催化反应特性使其在生物检测中有广泛的应用,并成为多样化的生物传感器的高效识别元件用于酶促反应底物、辅酶、抑制剂等待测成分分析的有效手段。目前,漆酶构成的生物检测器主要有两种:漆酶生物电极和漆酶生物标记。然而,由于漆酶作为蛋白质分子空间结构庞大,其电活性中心不易暴露,以及在电极表面的吸附畸变而导致电极表面钝化,使其在一般固态电极上的异相电子传递速率很低,导致电子传递受阻。有关生物蛋白酶电化学性质的研究,不仅能获得与蛋白质或酶的热力学和动力学性质等重要信息,为研制新型生物传感器件或生物反应器提供理论依据,而且对了解它们在生命体内的电子转移和信号传导机制和生理作用原理也有非常重要的意义。因此,许多研究者都致力于电子传递媒介体、促进剂和特殊电极材料的研究以加速漆酶分子的电子传递速率、改善它的电化学行为。纳米科技的发展为研究漆酶的电化学催化活性提供了一个全新而强有力的支撑。
碳纳米管(carbon nanotube,简称CNT)的尺寸处在以原子、分子为代表的微观物体与宏观物体交界的过渡区域,使它既是非典型的微观系统又是非典型的宏观系统,从而具有可观的表面效应、体积效应、量子效应和宏观量子隧道效应[2]。由于管壁中存在大量的拓扑缺陷,CNT表面本质上比其它的碳同素异形体和石墨异构体具有更大的反应活性;由于管壁屈曲,CNT中电子传递更快;管壁更可以便捷地修饰上−COOH等功能性官能团,这些基团的引入能有效降低某些反应的过电位。因此,CNT修饰电极在基础研究和分析应用方面都引起了人们的广泛关注[3]。Davis等用多壁碳纳米管(multi-walled carbon nanotube,简称MWCNT)固定蛋白质和酶,发现固定在羧基化MWCNT (MWCNT−COOH)上的蛋白质或酶没有变性,为蛋白质的固定提供了一个新方法[4]。此外,静电层层组装技术也为蛋白质的有序纳米组装提供了一种新技术[5]。
本实验利用稀硝酸氧化处理MWCNTs,在MWCNTs表面引入亲水性的−COOH和−CHO等极性含氧官能团,再将天然生物多糖—壳聚糖(chitosan,简称chit)分散并包裹MWCNTs管壁,使之成为MWCNTs@chit生物亲和界面,在pH 7.0的磷酸盐缓冲溶液(phosphate buffer saline,简称PBS)中实现固定化Lc的电化学。同时研究了Lc-MWCNTs@chit和Lc-MWCNTs层层静电自组装膜修饰玻璃碳电极(glassy carbon electrode,简称GCE)对溶解氧的电催化行为以及催化机理,最后测定了Lc催化对苯二酚的电化学表观米氏常数(KMapp)。
参考文献
[1] You J.; Ding W. P.; Ding S. J., et al. Direct Electrochemistry of Hemoglobin Immobilized on Colloidal Gold− Hydroxyapatite Nanocomposite for Electrocatalytic Detectionof Hydrogen Peroxide. Electroanalysis 2009, 21, 190−195.
[2] Kim S. N.; Rusling J. F.; Papadimitrakopoulos F. Carbon Nanotubes for Electronic and Electrochemical Detection of Biomolecules. Advanced Materials 2007, 19, 3214−3228.
[3] Tu W. W.; Lei J. P.; Ju H. X. Functionalization of Carbon Nanotubes with Water−Insoluble Porphyrin in Ionic Liquid: Direct Electrochemistry and Highly Sensitive Biosensing of Trichloroacetic Acid. Chemistry−A European Journal 2009, 15, 779−784.
[4] Davis J. J.; Green M. L. H.; Hill H. A. O., et al. The Immobilisationof Proteins in Carbon Nanotubes. Inorganic Chimica Acta 1998, 272, 261−266.
[5] Zhao H. T.; Ju H. X. Multilayer Membranes for Glucose Biosensing via Layer−by−Layer Assembly of Multiwall Carbon Nanotubes and Glucose Oxidase. Analytical Biochemistry 2006, 350, 138−144.
[6] 鞠熀先.电分析化学与生物传感技术. 北京: 科学出版社, 2006, 184−187.
实验内容:
本实验构建的漆酶生物传感器的检测原理如下。根据漆酶对酚类化合物的特异性识别和酶促反应:
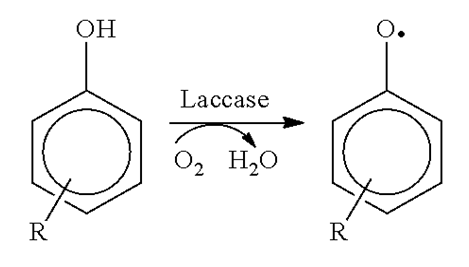
以上反应需消耗检测溶液中的氧气(溶解氧)。
另一方面,O2可以通过电化学催化还原为H2O,如在中性条件下
O2 + 2H2O + 2e− → 2H2O2+ 2OH−
H2O2 + 2e− → 2OH−
O2在纳米碳材料如MWCNTs表面有较强的吸附,同时酸化氧化的MWCNTs表面的各类含氧官能团也进一步促进O2的吸附,从而有利于电催化氧还原反应(oxygenreduction reaction,简称ORR)的发生。MWCNTs自身良好的电子传递特性也加速了O2的电催化还原。
然而,酶促反应消耗氧的速率快于电催化氧还原的反应速率,导致O2分子在MWCNTs修饰电极表面扩散层内的浓度减少,对应的直接电化学信号下降。该信号下降幅度与酶识别催化底物之间存在线性关系,从而建立起检测信号与分析物之间的信号传导和转换,这就是所制备的漆酶生物传感器的工作原理。
实验步骤:
(1) 可溶性多壁碳纳米管的制备
称取20 mg MWCNTs于50 mL圆底烧瓶中,加入30 mL 30% HNO3并加热回流4 h。冷却至室温,在1000~2000 rpm下离心3 min分离出MWCNTs沉降物,并用去离子水反复洗涤、离心直至上清液pH值达到5~6之间。放于110 ºC烘箱中干燥过夜,取出后在红外灯下、干燥器中继续烘干至恒重。通过FT−IR光谱表征,与未经酸处理的MWCNTs比较管壁的官能基团种类。
(2) 玻璃碳电极的预处理和电化学表征
GCE先后用0.3 μm和0.05 μm的α-Al2O3悬浊液抛光,然后依次用无水乙醇及二次水超声洗净、晾干。在电解池中加入1.0 mM K3Fe(CN)6 (以0.1 M KCl溶液为支持电解质),装配好三电极体系。以不同扫描速率:10、40、60、80、100、200 mV/s,分别记录从+0.6 V ~ −0.20 V电位范围的单扫描循环伏安图。
(3) 纳米组装漆酶传感器的构建
称取20 mg chit超声溶解于2.0 mL1% (v/v)的冰醋酸水溶液(pH ~5.0),而后将1 mg水溶性MWCNTs和4.0 mg Lc加入上述配制的1.0 mL chit溶液中。低频率下超声并震荡分散成黑色悬浮物MWCNTs@chit。将10 μL Lc-MWCNTs@chit分散液滴涂于电极表面,室温自然晾干制得Lc-MWCNTs@chit修饰电极。作为对照,不加MWCNTs以相似方法制得Lc修饰电极。
(4) 多壁碳纳米管@聚二甲基二烯丙基氯化铵的制备
将1.0 mL 0.5 mg/mL羧基化的MWCNTs (MWCNTs−COOH)分散在1.0 mL 0.2% (w/v)的PDDA中,再加入0.0585 g NaCl,振荡,使其溶解,将所得混合悬浊液超声30 min,使MWCNTs−COOH和PDDA通过静电相互作用组装(MWCNTs@PDDA),得到黑色溶液。在~2000 rpm下离心5 min,用微量移液枪弃去上层清液,留下黑色沉淀,再加入2 mL二次水,超声分散并振荡洗涤,如此重复离心洗涤三次除去过量的PDDA。最后黑色沉淀分散在1 mL二次水中得到0.5 mg/mL的MWCNTs@PDDA溶液。
(5) 多壁碳纳米管@聚二甲基二烯丙基氯化铵与漆酶层层自组装
将3 μL 0.5 mg/mL MWCNTs@PDDA溶液滴涂在电极表面,于室温静置并自然晾干,得到MWCNTs@PDDA修饰电极。用二次水荡洗除去未牢固吸附的MWCNTs@PDDA,然后插入4.0 mg/mL Lc溶液中静置15 min,荡洗电极除去未牢固吸附的Lc,形成Lc/MWCNTs@PDDA修饰电极。重复上述步骤,即可完成多层膜的自组装(如下图),形成(Lc/MWCNTs@PDDA)n修饰电极。
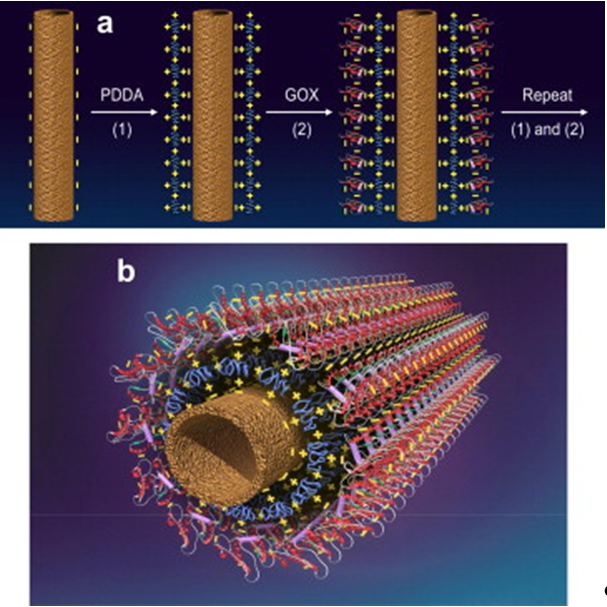
(6) 过氧化氢的催化和米氏常数的测定
分别应用上述两种修饰电极,在电化学测量池中加入10 mL 0.1 M pH 7.0 PBS,通O2 15 min后,采用流体动力学安培i~t曲线技术,在平稳转速和足够长的检测时间尺度下,于恒定电位−0.50 V,依次滴加不同溶度的氢醌溶液:0、0.001、0.002、0.005、0.008、0.01、0.025、0.05、0.10、0.15、0.20、0.25 mM等直到催化电流停止下降为止,记录各浓度连续的稳态台阶曲线图。
注意事项:
实验大纲、实验教材和实验安全(含注意事项)的撰写,具体注意事项如下:
[1] 裸GCE表面须抛光处理干净,否则会阻碍生物修饰膜的电子传递;
[2] Lc-MWNTs@chit的超声频率不易高且不能持续过长时间,否则会使Lc失活;
[3] 通气前清洁输气软管内外壁,通气时将输气管插入液面以下,通气完毕再提升到液面上方并关闭钢瓶阀门(防止倒吸),保持检测体系的气密性;
[4] 酚类化合物暴露在空气中易被氧化成醌类物质并变色,相应的溶液需新鲜配制,称量固体时须快速。
考核要求与方法:
(1) 数据处理
[1] 比较酸化处理前后MWCNTs的FT−IR谱图并解释水溶性原因。
[2] 有关电极粗糙度因子的计算:
由于1.0 mM K3Fe(CN)6 + 0.1 M KCl溶液在玻璃碳电极(glassycarbon electrode,简称GCE)上的直接电化学过程是可逆的,因此利用下列公式可计算电极的有效面积:
ip = 2.69 × 105 × n3/2 × D1/2 × υ1/2 × c × A
式中ip为峰电流,n为电子转移数,D为K3Fe(CN)6扩散系数,c为K3Fe(CN)6浓度,υ为电位扫描速率,A为电极有效导电面积(又称表观电化学面积),其与电极的宏观几何面积之比即是电极粗糙度因子。
[3] 比较Lc-MWNTs@chit和Lc@chit修饰电极催化对苯二酚电流大小。
[4] 米氏常数的测定及其意义。
Michaelis−Menten系数,简称米氏常数(KM)是研究酶促反应动力学重要的常数,其数值的物理意义为酶促反应最大速率一半时对应的酶催化底物浓度[S],表示酶和底物之间的特异性亲和力,KM值越小,亲和能力越强,反之亦然。在稳态条件下,类似于酶促反应的电催化过程,根据Lineweaver−Burk方程可得下列等式:
1 / ip = KM / ip,max × [S] + 1 / ip,max
从1 / ip对1 / [S]的作图可得一条直线,其斜率是KM / ip,max,在纵轴上的截距为1 / ip,max,二者做商即可计算出KM的数值。由于该系数由电化学方法所获得,鉴于电化学技术的表观(apparent)特性,所得KM值实质是一个生物界面平均化的数值,故称之为电化学表观米氏常数(KMapp)。
(2) 分析讨论
[1] 常见CNTs水溶性处理方法的比较;
[2] 比较蛋白质层层静电自组装和包埋法的优缺点;
[3] 探讨Lc对对苯二酚的亲和能性,并阐明KM的生物学意义。


