纳米颜料的制备及其钾元素传感应用
Preparation of Prussian Blue Film Modified Electrode and Its Application in Linear Sweep Voltammetry for the Detection of Potassium Cations
实验目的:
(1) 学会使用循环伏安仪;
(2) 学会测量峰电流和峰电位。
(3) 学会用循环伏安法电沉积制备纳米靛蓝传感器;
(4) 学会用线性扫描伏安法测定电解质溶液中的钾离子;
(5) 学会测量峰电位并掌握电位分析方法。
实验原理:
第一部分:循环伏安法判断电极过程
(1) 电极过程指的是溶液和电极界面上一系列变化的总和,包括物质输运(传质)、界面吸附/解吸(脱附)以及异相电子的传递过程。
(2) 研究电极过程常用方法有线性扫描伏安法(Linear Sweep Voltammetry,简称LSV)和循环伏安法(Cyclic Voltammetry,简称CV)。
[1] 线性扫描伏安法:在电极上施加一个线性扫描电位,如下
E = Ei – υ× t
其中E代表电位,υ表示扫描速率,其单位一般为V∙s−1,t为时间。记录这一过程中的电流−电位关系就得到单扫描伏安曲线。
峰的形成(如图):在电位向负扫描的过程中,电极表面氧化态物质初始被还原,形成阴极电流,随着电位的负移,电流迅速增加;当电极表面氧化态物质浓度接近0时,电流达到峰值;随后由于浓度梯度的形成、扩散层厚度的增加,在溶液本体的电活性物质向电极表面扩散传质的速率远远赶不上电极反应的电子传递速率,导致电极表面电活性物质来不及补充,出现“贫乏效应”,电流减小,从而形成一个还原峰。由此可读取峰电位和峰电流。
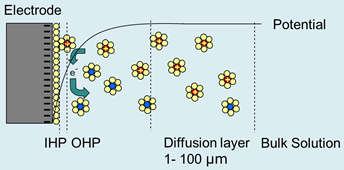
峰电流值的读取:峰顶点所对应的电流绝对值不是峰电流,必须先做基线电流的切线,再从峰顶做纵轴的平行线或横轴的垂线,即可求得峰电流强度。
[2] 循环伏安和线性扫描伏安法类似,循环伏安法是当线性扫描电位达到一定值时,回扫到初始电位值,所得的电流-电位曲线就称作循环伏安图,可作为一种基础的电分析手段。
施加在电极上的电位与时间关系如下图所示:
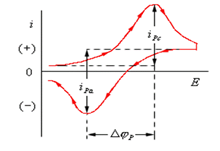
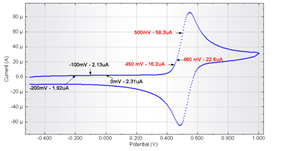
当电位扫向初始电位的负方向时,若溶液中存在电活性物质的氧化态(O),其电极上将发生还原反应:
O+ Z·e−↔R
反向扫描时,电极上生成的对应还原态(R)物质将发生氧化反应:
R− Z·e−↔O
从循环伏安图上可以获得峰电流ip,c、ip,a和峰电位Ep,c、Ep,a等重要参数信息,从而可以判断电极过程的可逆性。
根据Randles−Sěvčik方程,峰电流可以表达为:
ip = K × Z3/2× D1/2 × A × υ1/2 × c
其中,K为热力学常数,Z为电荷数,D为电活性物质在特定溶液中的扩散系数,A为电极面积(严格意义上是表观电化学反应面积),υ表示扫描速率,c代表电活性物质在溶液本体的摩尔浓度。
峰电流ip的影响因素包括:液相传质过程包括扩散、对流和电迁移,上述峰电流公式是基于扩散过程为动力学决速步(速控步)推导的,是扩散电流,所以在进行电化学实验前必须消除对流电流和电迁移电流的影响:
[1] 消除对流电流的方法是将溶液在室温下静置一段时间;
[2] 消除电迁移电流可以通过加入大量支持电解质(阴阳离子淌度相当,如KCl、KNO3、KClO4、(C4H9)4NClO4等)来消除。
(3) 判断电极过程的可逆性,必须同时满足以下四个判据:
[1] ip,c和ip,a都与υ1/2成线性关系;
[2] | ip,c / ip,a| ≈ 1
[3] ΔEp = Ep,a − Ep,c≈ 0.058V / Z (~25 °C);
[4] ΔEΘ= (Ep,a + Ep,c) / 2的理论值与实验值相吻合。
形式电位(简称式电位,又称条件电位,ΔEΘ)是两个峰电位和的一半,它与参比电极指示电位的准确性有关。
第二部分:电沉积铁氰化钾制备钾离子选择性电极
(1) 普鲁士蓝及普鲁士蓝电沉积简介
普鲁士兰(Prussian Blue,简称PB),又称滕式蓝(Turnbull’s Blue,简称TB),分子式为Fe4[Fe(CN)6]3,六氰合铁酸铁,是一种古老的蓝色染料(如图),也是文献上最早报导的金属混合价配位化合物。


PB修饰电极的方法很多,主要有双组分法和单组分法。单组分法是在同时含有金属离子和金属氰根配合物的条件下才能进行。这里我们采用从单组分K3Fe(CN)6酸性溶液中“一步法”电化学沉积PB薄膜。该种方法的优点是快速方便,PB薄膜结构致密,厚度可控制在纳米级。
(2) 普鲁士蓝电沉积机制
当电极电位较负时,[Fe(CN)6]3− (俗称赤血盐)被还原成[Fe(CN)6]4− (俗称黄血盐)(反应方程式1),它与从K3Fe(CN)6中解离出的极少量的Fe3+络合生成PB (反应方程式2)。
[Fe(CN)6]3− + e− → [Fe(CN)6]4− (1)
xK++ xFe3+ + x[Fe(CN)6]4− → KxFex[Fe(CN)6]x (2)
或者溶液中的Fe3+被还原成Fe2+ (反应方程式3),再与溶液中的K3Fe(CN)6络合生成PB (反应方程式4)。
Fe3+ + e− → Fe2+ (3)
xK+ + xFe2+ + x[Fe(CN)6]3−→ KxFex[Fe(CN)6]x (4)
问题:为什么上一章“循环伏安法判断电极过程”中没有生成PB?
(3) 溶液pH的作用
在pH 1.6的K3Fe(CN)6溶液中PB的沉积速度最大。当pH < 1.6时电极表面析氢影响,PB的沉积量减少;而pH > 1.6时,PB的沉积速度则急剧降低。
(4) 钾离子(K+)选择电极
这里我们所采用的电化学技术是LSV。当电位向负扫描的过程中,PB被还原生成普鲁士白(Prussian White,简称PW),金属阳离子在这里起到电荷平衡的作用。PB的晶格通道半径大约是1.6 Ǻ (如图),K+的水合半径大约是1.25Ǻ,所以PB对钾离子有一定的选择性。
值得一提的是,在水溶液中,黄血盐与Fe3+,赤血盐与Fe2+反应都生成狼色的沉淀,分别称为PB和TB,过去都被用作蓝色染料。所对应的两个显色反应也常被用于Fe3+和Fe2+的鉴别。现代X射线衍射的晶体结构分析证明,二者是同一种物质,不仅具有完全相同的化学组成,其结构也完全相同:Fe3+和Fe2+分别占据顶点、−C≡N−占据棱边。其中,N原子与Fe(III)键连、C原子与Fe(II)键连,K+则间隔的填隙于立方体中心。K+充填饱和时K : Fe : (CN)的化学计量比为1 :2 : 6。鉴于PB中存在价态不同的铁离子,视其为一种同素异价化合物。
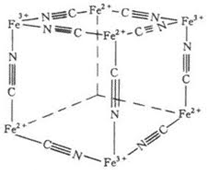

对应的电极反应方程式如下:
4K+ + 4e− + Fe4[Fe(CN)6]44−→ K4Fe4[Fe(CN)6]4
不同浓度K+的线性扫描伏安曲线中,峰电位的移动符合经典的Nernst方程。Nernst方程推导为
E = EΘ + (RT/4F) × ln([PB] × [K+]4 / [PW]) = EΘ + (RT/F) × ln[K+]
其中,因为[PB]和[PW]为固态,活度为1,可以约去。所以峰电位E与log[K+]有线性关系,理论斜率为0.058 V / Z,据此可通过在裸玻璃碳电极上电沉积纳米PB膜简易制备K+离子选择性电极(IonSelective Electrode,简称ISE)。
考核要求与方法:
[1] 测定裸电极在K3Fe(CN)6溶液中循环伏安扫描所得ip,a、ip,c和Ep,a、Ep,c值;
[2] 分别以ip,a和ip,c对υ1/2作图,阐明峰电流与扫描速率间的关系;
[3] 计算| ip,c / ip,a|、EΘ和ΔEp (尽可能≤ 100 mV)的具体数值;
[4] 综合上述实验结果,判断K3Fe(CN)6在KNO3溶液中的电极过程是否可逆;
[5] 记录在裸玻璃碳电极表面电沉积K3Fe(CN)6制备纳米PB的循环伏安图,比较PB膜修饰电极制备过程中的第1圈和第50圈循环伏安曲线,阐明峰电流和峰电位的变化;
[6] 记录纳米PB修饰玻璃碳电极在不同浓度KNO3标准溶液中的线性扫描曲线,提取各曲线的峰电位值,做出峰电位E− [K+]的标准曲线;
[7] 记录纳米PB修饰玻璃碳电极在未知K+溶液的线性扫描曲线,读出其中的峰电位值,并代入标准曲线,确定未知溶液中K+的浓度。


