第39-40课时 实验项目6-3 滴定操作技能考核
6-3-1 邻苯二甲酸氢钾的精确称量
一、能力目标
1、考核学生对溶液移取和定容操作的实验技能
2、考核学生对称量操作的实验技能的掌握程度
3、考核学生对滴定操作的实验技能的掌握程度
4、考核学生对实验数据的处理能力
二、实验原理
NaOH与KHP(邻苯二甲酸氢钾)发生酸碱中和反应:
KHP + NaOH = KNaP + H2O
204.22 g 1mol
m ![]()
推导出NaOH溶液浓度计算公式:
C = 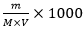 =
= 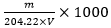 (mol/L)
(mol/L)
公式中:C——NaOH溶液浓度,mol/L;
V——消耗NaOH溶液体积,mL;
204.22—— 邻苯二甲酸氢钾摩尔质量,g/mol;
三、仪器与试剂
1、仪器
50mL聚四氟乙烯滴定管、250mL锥形瓶、250mL容量瓶、25mL移液管
2、试剂
固体NaOH(分析纯)、邻苯二甲酸氢钾(基准试剂)、0.5%酚酞指示剂
四、实验步骤
1、邻苯二甲酸氢钾(KHP)基准试剂的称量
在精密电子天平上,用递减称量法,从称量瓶中准确称取0.5000克邻苯二甲酸氢钾(KHP)基准物质置于250mL锥形瓶中,平行称取三份,要求邻苯二甲酸氢钾的质量范围在0.49~51克内。
要求:
(1)称量邻苯二甲酸氢钾敲样时,不能有试剂颗粒洒出锥形瓶外,称量瓶口不能附着试剂颗粒。
(2)称取的邻苯二甲酸氢钾的质量范围在0.49~0.51克内。
(3)用手机拍摄递减称量法称取邻苯二甲酸氢钾的操作过程,并上传视频,提交作业。
实验方案下载:


