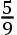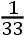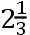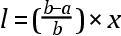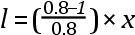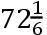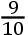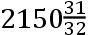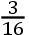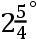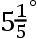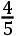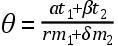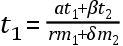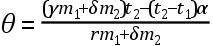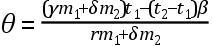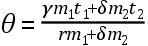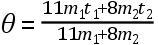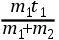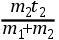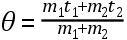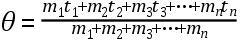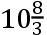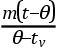(三)热学
十八世纪对热进行的科学研究最显著的特点体现在量热术的实验工作中。约瑟夫·布莱克在这类研究中处于领先地位,不过由于他没有发表自己的著作,因此一些历史学家把这份荣誉归诸瑞典物理学家约翰·卡尔·维尔克(1732—96),后者在这研究领域的工作要迟些时候。布莱克的实验工作后来由拉瓦锡和拉普拉斯加以发展,他们两人从布莱克的发现中所获甚多,尽管他们似乎不愿意承认曾受惠于他。十八世纪中,还开始对热膨胀进行精密测量。此外,朗福尔德伯爵在热与功的关系的研究上作出了贡献,不过,直到焦耳在十九世纪进行研究,他的努力才最终结出硕果。
一、热质说
十八世纪的热学实验工作基本上独立于关于热的本性的终极理论。这领域的一些第一流的实验人员对十七世纪时曾为人所深感兴趣的这种理论持冷漠态度。例如,拉瓦锡和拉普拉斯就是这样。然而,这种理论乃是所做工作的基础所在。有些研究者,特别是布莱克完全明白这一点。这理论可以称为热质说。热质 [1] 被认为是一种无所不在的无重量的具有高度弹性的流体,其微粒为物质吸引,彼此之间却相互排斥。该理论认为,当两个不同温度的物体相互接触时,热质从较热物体流向较冷物体,直至在物质微粒和热质微粒两个系统中达致平衡。当因受热而产生膨胀时,这膨胀被归因于加热时进入膨胀物体的热质微粒的相互排斥。物体被压缩时(因摩擦)产生热,被解释为或是由于被摩擦损伤的物体的微粒失去了容纳热质的部分能力,从而释放出热质,使物体呈现为热的;或是因为摩擦和压迫把被压物体中潜在热质挤压出一部分,从而使物体变得令人感觉是热的。在燃素为化学家们接受的时代(参见第十三章),物理学中出现热质说也许是很自然的事。但是,它比燃素说存在到更晚的时期,十九世纪中叶以前一直支配着关于热的科学。这主要归因于布莱克的很有价值的实验工作。正像科学史上屡见不鲜的事例那样,对于一个机灵的科学家来说,任何可实行的假说,即使是虚妄的假说,也总比一无所有要好。
二、热容量
在布莱克之前,人们普遍认为,为使任何物体的温度升高所需的热量与该物体的密度成正比,或用现代的术语来说,等重量的一切物体的热容量总是相等的。大约在1760年,布莱克开始仔细考虑这种见解。他知道,华伦海特曾在各种温度下把水和水银混合起来,发现水银的加热和冷却效应仅为同体积水的三分之二,而水银的密度却是水的十三倍。伯尔哈韦曾报告了这一结果。布莱克考虑了这一结果,得出结论:“不同物质为了达到彼此平衡而降温或同等程度地升温时所必须接受的热量并非与每种物质的量成正比,而是广泛地与其他多种因素成正比。”华伦海特的实验当时启发布莱克把其他物质的加热和冷却效应与一定量水的加热或冷却效应进行比较。这种方法导致现代的比热制。布莱克把如此对于各种物质得到的值称为“对于热的容量”。鲁宾逊这样描述布莱克的方法:“布莱克博士通过混合两个温度不同但质量相等的物体,估算了这种容量;然后指出,它们的容量与每个物体因混合而发生的温度变化成反比。例如,1磅温度为150°的金被突然与一磅温度为50°的水相混合,水温升高到接近55°。于是,金的容量与等量水的容量之比就是5∶95,即1∶19;因为金失去了95°而水得到了5°。”(Lecturse,I,p.506)
今天所用的混合法即是由这种方法发展而来的,只是现在质量是不同的,并且引入了许多技术上的改良。从本质上说,作为一种精密的科学程序的量热术是由布莱克创始的。名为“对于热的容量”的“比热”观念实质上也是他提出的。
三、潜热
布莱克

图88—布莱克
布莱克最著名的发现是“潜热”。这发现是他通过关于流动性问题的研究而作出的。他说,在他那个时代,“人们普遍认为,流动性的产生是由于当一个物体被加热到了其熔点时,它原有的热量又增加了少许的缘故。当通过减少很少量的热,使它冷却到原来的温度后,它就又回复到固态;当一个固体变为流体时,它原有的热所得到的增加并不多于熔解后温度计指示的温升所量度的热;当这熔化物体由于热的减少而又冻凝时,热的损失也不会多于简单地用这温度计量它所指示的热。
“这就是我所知道的,1757年我在格拉斯哥大学开始演讲时关于这个问题的公认见解。然而,经过仔细考虑,鉴于同许多明显的事实相悖,我很快发现有理由拒斥这种见解;我力图表明,这些事实令人信服地证明,流动性是热按一种完全不同的方式所产生的。……
“如果我们留心观察在露置于温暖房间空气里的冰雪融化或者融霜继而结冻的方式,那么我们很容易发现,不论它们起先可能多么冷,它们也都会很快被加热到熔点,即其表面很快开始变成水。如果这公认见解根据充分,如果它们之完全变成水只需要再加很小量的热,那么,即使块体很大,也应在不多几分钟甚或几秒钟之内全部熔化掉,因为热在继续不断地从周围空气中传来。若果真如此,那其后果在许多场合将是非常可怕的。因为,即如目前的情形,大量冰雪的融化将在寒冷国家或发源于这些国家的江河中引起洪水泛滥。可是,如果冰雪融化果真必定骤然突发,如果前述关于热的熔化作用的见解果真确有根据,那么,洪水泛滥将更势不可挡,令人可怖。它们将势如破竹,席卷一切,人类在劫难逃。然而,这样突发的液化实际上并未发生。冰块和积雪的融化是一个缓慢的过程,需要很长时间。如果它们体积庞大,例如某些地方冬季形成的连绵冰山雪原,那就更其如此。从开始融化起,须有数星期温暖天气,它们才能完全融化成水。冰的融化如此缓慢,使我们能够在夏季很容易地把冰保藏在一种叫做冰窖的结构中。冰一放入冰窖,便开始融化;但是,由于这建筑仅有很小的表面暴露于空气,顶上还有厚厚的草覆盖,外界空气进入内部的通路也被尽可能地堵塞,所以,热以一种缓慢的过程穿透冰窖。同时,冰本身又倾向缓慢融化。这样,冰的全部液化过程就变得很长,以致在夏末仍有一部分冰被保存下来。许多高山上的积雪在整个夏季中情形也是这样。雪一直处于融化状态,但融化得很慢,以致整个夏季也不足以使积雪全部融化。
“冰雪融化得如此缓慢,令我感到,这与关于物体液化时热的变态的公认见解大相径庭。”
布莱克还观察到,如果人把手放在一块冰上,那冷的感觉表明,冰受热的速度是很快的。但是,如果用一支温度计去测量从融化冰块上滴下的水,则它显示,这水和冰的温度相同。他说:“因此,融化着的冰中所进入的大量的热或热物质仅仅产生使它得到液化而没有使它增加明显的热量;看来这热被吸收和隐藏在水之中,所以,用温度计也发现不了。”
可见,在布莱克时代之前,人们一直认为,当热施加于冰时,热全部体现为温度的上升。而布莱克现在表明,在这样的或类似的变化中,大量的热被吸收而同时未发生温度变化,或者用布莱克的话来说,“被变成为潜在的”。他根据下述假设解释这些(以及类似的)事实:热物质与冰结合而形成水——水是由冰和热物质结合形成的一种化合物,似乎
冰+热物质=水,以及
水+热物质=水蒸气。
在他的实验中,他用了两个玻璃球,里面分别装有等重量(5盎司)的(1)温度33°F的水和(2)温度32°F的冰,把它们置于一个具已知均匀温度的房间里。然后观察,冰的融化和水从33°F上升到室温各需多少时间。冰的融化共用了10.5小时;水从33°F上升到40°F,用了半个小时。这样,前者花了21个小时,后者花了1个小时。布莱克论证说,因此,冰吸收了21×(40-33),也就是21×7,亦即147“热度”;但是,其中8“热度”用来把生成的水升温到最终温度40°F。所以,冰的融化本身共需139“热度”。换算成摄氏温标,这相当于值
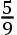 ×139,即77,很接近于现在公认的值80。
×139,即77,很接近于现在公认的值80。
布莱克还用已知质量的冰和已知温度的热水做了些实验,观察它们混合后的温度。这些实验给出了相似的结果。后来,他又研究了水转变成水蒸气时发生的类似变化。他把温度为50°F的水盛于扁平罐头中,放在红热的金属板上。4分钟后水开始沸腾,20分钟后水全部煮干。因此,水变成水蒸气所需的热为(212-50)×20/4=162×5=810“热度”。其他实验得到的结果是830和750。布莱克又让蒸汽流经一个冷凝器,得到了739的值,考虑到实验误差,他把这个值提高到“不低于774度”。按布莱克的单位制,正确的值应当是967“热度”。如果用现代单位来表示这些数字,他得到的值是450,而正确的数字是538。但是,用此法进行这样的测定时,其准确度不如冰融实验。除了让蒸汽流经冷凝器的实验是(与欧文一道)在1764年做的之外,上述其他实验全都是1762年做的。布莱克把他用这种方式测到的热称为“潜热”。(参见布莱克的Lectures on the Elements of
Chemistry,J.Robison编,Edinburgh,1803,Vol.I,pp.116ff. ,157ff.
,171ff.)
1764年,在布莱克和欧文对水汽化的潜热进行实验测定后过了几个星期,瓦特用一个较小但更合宜的设备进行了类似实验,“这些实验得到的包含于蒸汽中的热的平均值为825°”(布莱克:Lectures,I,p.173)。布莱克写道,后来“瓦特先生告诉我,他已观察到变成在蒸汽中潜在的热与从蒸汽出现的热恰如所希望的那样严格一致;从能耐受寻常大气压的蒸汽所获得的热不低于华氏900°,但不超过950°”(同上,p.174)。瓦特的实验是在他研究蒸汽机的过程中做的。
布莱克还解释了水的过冷现象,即水冷却到其凝固点(32°F)以下而又不发生凝固的现象。当水在不与外界完全接触并且不受任何机械扰动的条件下被小心冷却时,水可冷却到凝固点之下7、8度,甚至10度,而又不凝固。“如果现在用一根结晶形成的纤细的冰针或一个干雪片轻轻地与水接触,则它立即就会变成一根根美丽的冰刺,迅速成形而向四面八方飞散开来,而留在其中的温度计慢慢地上升到32°”(Lectures,I,p.130)。布莱克说,水在如此被小心翼翼地冷却而不受机械扰动的情况下,保持了它的潜热,但扰动——增加一片冰晶——“使部分潜热游离出来而变成了可感知的热,同时失去其潜热的那部分水就变成了冰。但是,这样一下子游离的热在数量上比普通冻凝过程中任何时刻所游离的热都要多,因此,前一种情形就更明显地表现出:突然非常显著地增加材料的可感知的热,限制了这样突然形成的冰的数量”(同上,p.130)。
欧文思考了布莱克的研究结果后认为,区分潜热和可感知热,是不必要的。每当物态发生变化,就会有热容量的突变,并且就会有相应数量的热进入或离开物质,而又对温度计读数不产生任何影响(Black:Lectures,I,p.194)。欧文进而又推想,物体的比热随温度升高而增加。他由此推论,水的比热应当比冰的比热高,并且若果真如此,则在融化过程中冰的温度为何不能升高的原因就得到了解释(Essays,pp.51—2)。欧文从实验中发现,冰的热容量仅是水的热容量的0.8,于是认为,这个实验结果是这一理论的有力证据。
克莱格霍恩应用他的热理论解释了不同的物质之间和同种物质的不同物态之间的热容量差异。他认为,不同物质以不同强度吸引热微粒,因而它们对热微粒的吸收也各不相同。一给定物体吸引热微粒,直到其吸引和热微粒间的相互排斥达致平衡,这时该物体就不再吸引更多热微粒了。然而,如果该物体——譬如水——突然转变成了蒸汽,那么,热微粒就被扩散到大大增加的空间之中,而它们之间的相互排斥也就大大削弱了。因此,既然水的每个微粒对热微粒的吸引并未减小,那么每个水微粒在热微粒彼此间的相互排斥与水微粒自己对它们的吸引相平衡之前,就可在这个较大空间中在自己周围聚集更多的热微粒(克莱格霍恩的Disputatio,etc. ,1779,以及布莱克的Lectures,I,pp.195—6)。在布莱克看来,欧文和克莱格霍恩的理论都不能令人满意,因为他们没有把熔解和蒸发中的热变化看作原因,而是把它们当作熔解和蒸发的结果(布莱克的上述著作)。
四、量热术的发展
拉瓦锡和拉普拉斯
在布莱克之后,接着有拉瓦锡和拉普拉斯做了重要的工作。他们合著的《论热》(Mémoire sur la
Chaleur)于1783年宣读,1784年发表于(提前的)1780年《皇家科学院备忘录》。两位作者开头便指出,物理学家们对热的本性的理解尚不一致。有些人认为,热是一种流体,无所不在,按物体包容它或与它结合的不同性质而被包容在物体之中或与其结合。另一些人则认为,它是物质微小组分做振荡运动的结果。他们自己也不对这些观点的哪一个进行辩护,因为有些事实同一种观点相一致,而另一些事实同另一种观点相一致。但是,物体作简单混合时chaleur
libre(即“自由热”,同潜热相对)的守恒却是独立于任何这类假说,为所有物理学家公认。
拉瓦锡和拉普拉斯把使1磅水升温1度的热量取为热的单位。因此,各种物质“对于热的容量”或“比热” [2] 就表达为使相等质量物质上升相等温度数所需的热量。他们认识到,“比热”不一定在温标的一切点上都是恒常的。但是,他们提议,可以认为比热在列奥弥尔温度计上从零度到八十度之间基本上是恒常的。他们以下面例子说明他们的方法。取0°的水银1磅,34°的水1磅。将两者混合。于是,产生了33°的均匀温度。水失去的热使水银温度上升33°。因此,使水银上升到某一给定温度,仅需为使同样质量的水上升到同样温度所需热量的
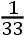 ;于是,水银的比热是水的比热的
;于是,水银的比热是水的比热的
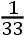 。这可推广为:设m代表两个物体中较热一个的质量(以磅计),a代表其温度,q代表使1磅该物体上升1度所需的热量。设另一物体的这些值分别为m′、a′、q′。设b为两物体混合并有一均匀温度时的温度。物体m所失去的热量为m·q·(a-b)。物体m′所得到的热量=m′·q′·(b-a′)。这两个热量是相等的。所以,mq(a-b)=m′·q′(b-a′)。由此可以得到q/q′=m′(b-a′)/m(a-b),这样,就无需知道q和q′了。
。这可推广为:设m代表两个物体中较热一个的质量(以磅计),a代表其温度,q代表使1磅该物体上升1度所需的热量。设另一物体的这些值分别为m′、a′、q′。设b为两物体混合并有一均匀温度时的温度。物体m所失去的热量为m·q·(a-b)。物体m′所得到的热量=m′·q′·(b-a′)。这两个热量是相等的。所以,mq(a-b)=m′·q′(b-a′)。由此可以得到q/q′=m′(b-a′)/m(a-b),这样,就无需知道q和q′了。
然而,在许多情况下,这种混合法是不切实际的,而且精确度也不高。例如,当两种物质的密度差异很大时,就很难保证每一部分都达到同样温度。此外,如果这两种物质产生了化学相互作用,那就必需应用一种中间参照物,有时还需要几种这样的中间物;这就增加了测定的次数,从而增加了误差。这种方法还不适用于测定化学反应以及燃烧和呼吸的热,而这些对于制定一个正确的热理论来说是最为重要的。
于是,他们宣称,他们发明了一种通过观察融化了多少冰而来测量热的新设备,即量热器(见图89)。
为了测定一个固体的比热,把它升温到一已知温度,然后迅速放进量热器,留在那里,直到它的温度降到零度。把所产生的水收集起来加以称量。用这水的质量除以该物体质量与该物体原先在零度以上的温度数的乘积,所得到的商与该物体的比热成正比。实际上,如此得到的值是单位质量该物体冷却1度时所融化的冰的数量。但是,如该论文后面所解释的那样,为得出所求的比热,还必须把这个值乘以60,所以乘以60是因为1磅水从60°冷却到零度时可以融化1磅冰。换言之,60是列奥弥尔温标上冰熔解的潜热的值。令人惊讶的是,拉瓦锡和拉普拉斯从未提到过“潜热”;他们借以证明这个乘数之合理的论证是在大兜圈子,令人感到,他们在竭力避免承认,他们的方法乃建基于布莱克的潜热发现。
拉瓦锡和拉普拉斯同样也表明了,如何测定液体的比热、化合热、某些盐溶液产生的冷却度、熔解热、呼吸和燃烧产生的热以及气体的比热。对流体的处理方式大致和对固体的相同,只是流体必须封闭在容器里,还必须考虑到在冷却过程中容器所失去的热量而加以修正。在测定几种物质的化合热时,这些物质和盛着它们的容器全都要冷却到零度。然后,把它们混合,放到量热器中保存,直到混合物冷却降到零度。所产生水便量度了热的增量。盐在溶解时所吸收的热量这样确定:把每种物质都提高到同一温度,把它们与量热器中的水混合,测量所融化的冰的量,然后,把混合物加热到一已知温度,再放进量热器中,使混合物冷却到零度,并再观察融化了多少冰。根据后者可以确定温度范围与融冰质量之间的比例,从而就可确定与实验第一部分中融冰质量所对应的温度。这一温度与各物体被提高到的温度之差就给出了这一过程中所吸收的热量。

图89—拉瓦锡和拉普拉斯的量热器
测定熔解热的方法如下所述。设m为被研究物体的熔点。把这物体加热到m-n度,然后把它放进量热器中。设该物体在冷却到零度的过程中所融化的冰的数量为a。把该物体加热到m+n′度,重复上述过程,设这时所融化的冰的数量为a′。把物体加热到m+n″度,再重复一遍。设这一次所融化的冰的数量为a″。因此,a″-a′就是当液体冷却了n″-n′度时该物体所融化的冰的量。由此可知,当物体从n′度开始冷却时,它融化的冰的量为n′(a″-a′)/(n″-n′)。于是,物体在固态从m度冷却时,将融化数量为ma/(m-n)的冰。设x为物体从液态过渡到固态过程中放出的热所融化的冰的数量。那么,当物体被加热到m+n′度后所融化的冰的总量将为n′(a″-a′)/(n″-n′)+x+ma/(m-n),而此式=a′。所以,x=(n″a′-n′a″)/(n″-n′)-ma/(m-n)。为准确起见,n和n′的均切不可大。两位作者指出,这种方法不仅给出x的值,而且给出这种物质在固态和液态时的比热的值。
测定燃烧热和呼吸热的方法是,在量热器中燃烧物质或让动物在其中呼吸,同时由一个适当装置从外部供给新鲜空气。这种实验要求的条件,是必须尽可能把可燃物或动物的温度降到零度。他们提出,为要测定气体比热,可让一股气流通过量热器内的一根螺旋管,在管道入口和出口处分别放一支温度计观测气体在这两处的温度。温度计指示气体温度的下降;量热器给出融化的冰的质量;所通过的气体的质量很容易加以测定;由这些数据就可计算出比热。
如此说明了量热的主要方法和结果以后,拉瓦锡和拉普拉斯注意到:这些结果并未给出关于物质中时热的绝对数量的信息,而只是给出为把一些种类物质升温同样度数所需热的相对数量。换言之,比热仅仅是绝对热的微分之比;认为这些微分与绝对热成正比,那是没有根据的。显然,温度计的零度并不排除相当数量绝对热的存在。还差得远哩。拉瓦锡和拉普拉斯试图至少测定一种物质在零度时的绝对热和它温度上升1度时所增加的热两者之间的关系。这种尝试乃根据对两种物质化合时放出的热的研究。但是,所得到的各个结果是相互矛盾的,不能令人满意。
论文的最后一部分讨论了关于燃烧和呼吸中放出的热的实验。作者把一些数量已称量过的木炭和体积已测定的“纯粹空气”(氧气)放在一个倒置于水银上的钟罩中燃烧。他们测定了所产生的“固定空气”的数量(方法是用强碱吸收它,观察其体积的缩小)以及剩余“纯粹空气”的数量。他们事先已在量热器中燃烧了已知重量的木炭,并测定融化的冰的质量。他们把这些结果加以综合而表明,燃烧1盎司木炭消耗3.3167盎司“纯粹空气”,形成3.6715盎司“固定空气”;在这样的燃烧中,1盎司“纯粹空气”的变化可融化29.547盎司冰;而1盎司“固定空气”形成要融化26.692盎司冰。他们在提出这一结果时还告诫说:这种实验只做了一次,他们主要意在把他们的方法告诉物理学家,而实验的结果则是次要的。值得注意的是,他们在谈到这实验结果时说,这是“1盎司纯粹空气在木炭燃烧过程中发生的变化所释放的热的量”。另一次让磷在“纯粹空气”中燃烧的类似实验表明,1盎司“纯粹空气”被磷吸收时融化68.634盎司冰。“纯粹空气被磷吸收时所放出的热几乎是它转变成固定空气时放出的热的
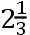 倍。”这事实使他们颇感惊讶。用以表达这结果和讨论其结论的语言乃基于拉瓦锡的理论:空气和蒸气的气态乃起因于它们结合了大量热,他认为,“纯粹空气”即氧气包含巨量的热。当它转变为固结态时,例如在金属煅烧以及磷、硫等等物质燃烧时,就几乎失去了全部的热,——但在“固定空气”中还保留相当一部分热。在“纯粹空气”与“亚硝空气”燃烧的场合,则是明显的例外——只释放极小量的热。因此,在硝酸(产品)和硝石中肯定含有大量的这种热——,这些热后来在爆炸时便显现了出来。这样,在拉瓦锡看来,这些变化中所放出的热乃被包含在“纯粹空气”之中,并由在化合中呈固态的这种空气释放出来。现在我们知道,如此放出的热的量只是这些化学反应的热的一部分——拉瓦锡还根本不知道化学能。
倍。”这事实使他们颇感惊讶。用以表达这结果和讨论其结论的语言乃基于拉瓦锡的理论:空气和蒸气的气态乃起因于它们结合了大量热,他认为,“纯粹空气”即氧气包含巨量的热。当它转变为固结态时,例如在金属煅烧以及磷、硫等等物质燃烧时,就几乎失去了全部的热,——但在“固定空气”中还保留相当一部分热。在“纯粹空气”与“亚硝空气”燃烧的场合,则是明显的例外——只释放极小量的热。因此,在硝酸(产品)和硝石中肯定含有大量的这种热——,这些热后来在爆炸时便显现了出来。这样,在拉瓦锡看来,这些变化中所放出的热乃被包含在“纯粹空气”之中,并由在化合中呈固态的这种空气释放出来。现在我们知道,如此放出的热的量只是这些化学反应的热的一部分——拉瓦锡还根本不知道化学能。
两位作者还对呼吸进行了类似实验。他们把豚鼠放在置于水银之上的钟罩中,里面容有“普通空气”和“纯粹空气”,用苛性碱收集所产生的“固定空气”,苛性碱的重量在实验前和实验后均加以称量。经过数次实验,他们得到了10小时里平均产生224谷 [3] “固定空气”的结果。根据以前做的燃烧木炭的实验,他们计算出,224谷“固定空气”的形成可融化10.38盎司冰。“因此,这个融冰量就代表了一只豚鼠10小时呼吸所产生的热。”此外,这种动物一直保持几乎恒定的体温,所以,它们在实验开始和结束时都有着相同的热。因此,所融化的冰就代表了这动物所失去的热,而这热在这期间由动物的生命机能所补充。“我们可以认为,呼吸引起的‘纯粹空气’变为‘固定空气’这变化所放出的热乃是动物热守恒的主要原因;如还有其他也有助于维持这热的原因,那它们的效果也是很小的。”“因此,呼吸就是一种燃烧,尽管速度非常缓慢,但在其他方面都与木炭的燃烧完全相似。这种燃烧发生在肺里,不发出可看见的光,因为火的物质一释出就立即被器官的潮湿吸收掉了。这种燃烧所产生的热被传送到流经肺的血液之中,然后播散到动物全身。这样,我们所呼吸的空气起着对于我们生存来说同等必需的两个作用;把固定空气的碱从血液中清除出去,因为过量的碱有很大危害;这种化合在肺中放出的热则补偿我们因向大气和邻近物体供热而不断损失的热。”
五、绝对零度
欧文从测定冰的比热中产生了一个独创性的想法,即尝试计算温度的绝对零度。下面是他对这方法的描述:“如果一个物体的固态和液态的热量x完全相等,即在发生物态变化时〔在测温液体中〕产生同样的膨胀,或者说,它们的凝固点处于同样可感热度〔温度〕上,那么,该物体在物态变化时变热或变冷〔绝对热函变化〕的度数即为固液两态的热容量之比。现设两物态的热量为100。如果固态的热容量与液态的热容量之比……为1∶2,则该物体在液态时的热必定两倍于冷〔固态〕时的热,即必定有100度的热变成了潜热。如果热容量之比为1∶3,则该物体在液态时的全部热必定为300,其中潜热为200。……一般地说,如果固态时的全部热为100,那么,在液态时的潜热将等于固液两态热容量之差除以表示固态热容量的数,再乘以固态时的全部热。”(Essays,pp.117—118)欧文的儿子把这一命题用数学式表达了出来:若a和b分别为水和冰的比热,l为冰熔解的潜热,x为“用度数表示的固体的绝对热”,则有
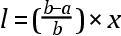 (Essays,p.122)。用欧文自己采用的冰的比热的值(0.8)代入,我们有
(Essays,p.122)。用欧文自己采用的冰的比热的值(0.8)代入,我们有
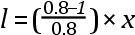 ,由此可得x=-140×4=-560,它给出绝对零度为-528°F,——欧文没有提到过这个结果,他只给出他父亲所得到的数字-900°(Essays,pp.127和137)。很可能他是从对冰的比热的其他测定结果中得出这个数字的。欧文还把这一方法应用于溶解和化学反应中的热,他认为这样的热也是潜热。他还根据向水中加入硫酸时所放出的热以及这两种物质的比热得出了和冰与水的情形里相同的绝对零度值-900°F(Essays,p.127)。
,由此可得x=-140×4=-560,它给出绝对零度为-528°F,——欧文没有提到过这个结果,他只给出他父亲所得到的数字-900°(Essays,pp.127和137)。很可能他是从对冰的比热的其他测定结果中得出这个数字的。欧文还把这一方法应用于溶解和化学反应中的热,他认为这样的热也是潜热。他还根据向水中加入硫酸时所放出的热以及这两种物质的比热得出了和冰与水的情形里相同的绝对零度值-900°F(Essays,p.127)。
克劳福德还把这种方法应用于获得“脱燃素空气”和“可燃空气”燃烧时的热数据,得到了绝对零度的值为-1500°F(Experiments and Observations on Animal
Heat,2nd ed. ,1788,p.267)。
小欧文所引用的冰的比热值为0.9(Essays,p.55),他存疑地把这个数值归之于克劳福德,并用这个数据计算出冰在32°F时的绝对热为1260°(同上书,p.122)。
加多林也研究了这个问题。他根据布莱克对冰溶解的潜热的估值147°F和维尔克对融雪吸收的潜热的估值
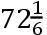 ℃进行计算,并取
℃进行计算,并取
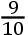 为冰的比热,结果发现,按照这些数据,温度的零度应当是-817℃或-722℃,而他的实验则表明-800.6℃。但是,后来他估计雪的比热是0.52,这样,温度的零度似乎是-170.6℃,而用蜡进行的类似测定显示温度的零度值为-480℃(Nova Acta
Reg.Soc.Sci.Upsala,1792,Vol.Ⅴ,I)。加多林从这些结果的不一致得出结论:这种方法是不能令人满意的,物质的比热可能随其温度而变化,但不与它们的总热量成比例。
为冰的比热,结果发现,按照这些数据,温度的零度应当是-817℃或-722℃,而他的实验则表明-800.6℃。但是,后来他估计雪的比热是0.52,这样,温度的零度似乎是-170.6℃,而用蜡进行的类似测定显示温度的零度值为-480℃(Nova Acta
Reg.Soc.Sci.Upsala,1792,Vol.Ⅴ,I)。加多林从这些结果的不一致得出结论:这种方法是不能令人满意的,物质的比热可能随其温度而变化,但不与它们的总热量成比例。
六、热膨胀的测量
固体和液体的热膨胀的精确测量提出了一些问题,它们吸引了十八世纪的许多研究者。
布鲁克·泰勒表明(Phil.Trans.
,1723),测温液体的膨胀与环境浴中热的增加成正比。他使用一种亚麻子油温度计,管茎上精心标上了分度标志,使各分度给出相等的容积;他在这实验中还用了两个薄的锡容器,它们的大小和形状都相同,每个容器的容量都是1加仑。“然后(每次试验时均注意,在向容器中注水之前,各容器应当是冷却的,而那个测量热水用的容器应已被充分加热)我相继向各容器注入1、2、3等份热沸水,余下那个注入冷水;最后完全注入热沸水。每次都把温度计浸入水中,观察水上升到哪个标志,并为准确起见,每次试验都在两个容器中进行。在首先观察了温度计在冷水中处于哪个刻度以后,我发现,温度计从该标志开始的上升,即亚麻子油的膨胀,与这混合物中热水的数量,即热度精确地成正比。”
约翰·埃利科特研究了固体的线膨胀(Phil.Trans.
,1736)。他发明了“一种测量金属受热膨胀程度的仪器”。在这种仪器中,一根金属杆的膨胀相对一根同样热度的标准铁杆的膨胀来测量,这被测杆就放在标准铁杆上面。借助适当连接的杠杆和滑轮,这两根杆的差膨胀操纵一根指针在刻度盘上移动,这有点像人们熟悉的课堂演示实验。1/7200英寸的膨胀使指针移动一个分度。
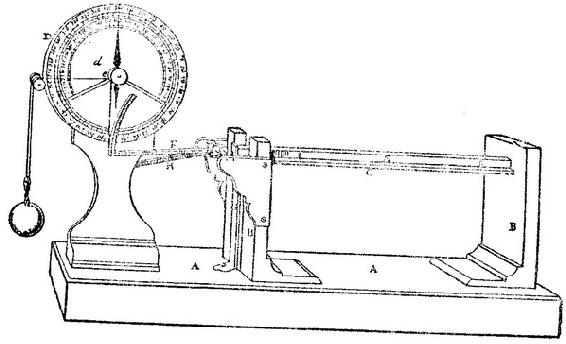
图90—埃利科特测量热膨胀的仪器
斯米顿发明了一种型式与埃利科特的仪器相似的“新式高温计”(Phil.Trans. ,1754,p.608f.)。在这种仪器中,把任意给定金属制的杆的膨胀与一根标准黄铜杆或“基准”相比较,这根标准杆在某一给定温度范围里的膨胀又通过同一根标准木杆(松木或杉木制)加以一次性检定。所用的杆长2英尺4英寸(图91)。黄铜杆构成仪器的永久性基座,两端点是支持被测杆用的两个竖立支柱。两根杆都可被浸入一个水浴中,这水浴被许多灯加热到所需的温度,由一支温度计读出。木杆两端包覆了黄铜,以免受潮湿和蒸汽的影响。整个木杆都涂上清漆,并完全用“粗亚麻”包裹起来。用一个灵敏的测微螺旋来测量基座和杆在一个给定温度范围里的膨胀差;基座在该范围里的膨胀加上或减去这个差,便得到相对标准木杆测得的杆的总膨胀。这木杆只是在需要时才放到仪器旁边,并且总是放在水浴的外面。与金属杆的膨胀相比,木杆的膨胀是很小的。不过,这一点已经考虑到了:从木杆被置于工作位置到取得读数之间的时间间隔用一个秒表或用其他方法记录下来;经过一段相等的时间间隔之后,进行第二次测量度,如此对第三个和第四个时间间隔进行测量。这四次测量结果的三个差被发现几乎就是一个几何级数的三个项,由这级数可以知道其前项,并可以之作为校正值;当把这级数应用于第一次测量时,则可把这次测量结果还原为假如在这次测量期间木杆没有膨胀而本来会有的值。斯米顿声称,他的结果可以重复,误差不到二万分之一英寸。他从实验得到了铁、钢、锑、铋、铜、黄铜、铅、锡、锌、各种合金和玻璃的膨胀系数值。
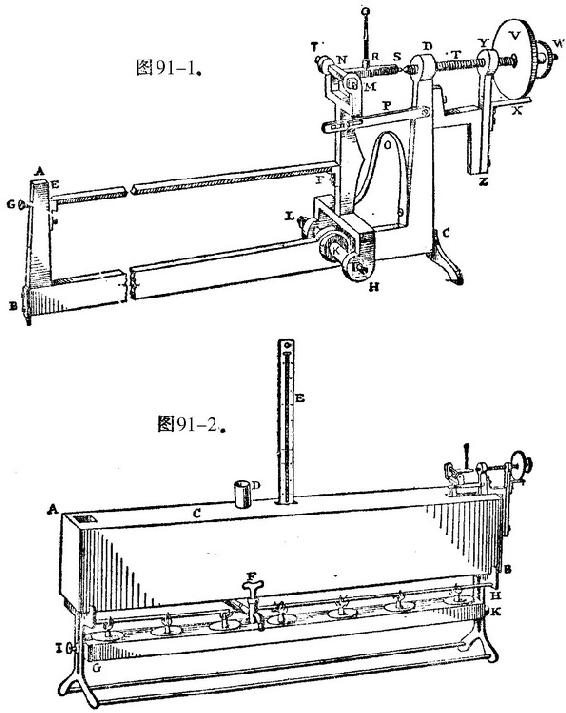
图91—斯米顿的高温计
拉姆斯登发明了一种测量一根金属杆相对于一些维持一定温度的标准杆的膨胀的方法。他的装置曾被罗伊用于测定一些标杆的膨胀,它们用来量度豪恩斯洛石南丛林的一条基准线(Phil.Trans. ,1785)。这种装置有三个平行的槽(图92),每个5英尺多长。两个在外侧的槽中各有一根铁杆,借助于充填捣碎的冰,使它们保持恒温;中间那个槽必要时可从下面加热,它包含被测杆,后者一端被固定。中间这根杆的长度变化用下述光学系统测定:外侧杆A的两端各固定着一个带有十字准线的目镜;中间杆的两端则各固定着透镜,它们用作A上目镜的物镜。外侧杆B的两端均有十字准线,由镜从后面照明。当三个放着金属杆的槽中都充填上冰时,由A上的两个目镜和中间杆上的两个物镜所形成的两个望远镜系统就加以调节,以使B两端的十字准线的像与A上目镜的十字准线重合。然后,用热水替换中间槽中的冰,并用槽下的灯使水保持恒温。于是,这根杆就膨胀,其自由端向外移动,同时带动附加的物镜。当条件稳定时,将杆A端头上的目镜移动,直至像和十字准线再度重合,所移过的距离由附装的精密测微螺旋测得。然后,借助单比例就可计算出中间杆的长度在两个温度之间的增加量。
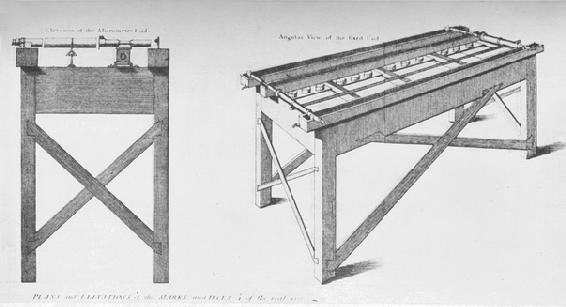
图92—拉姆斯登的高温计
七、热和重量
热质说之所以能盛行,主要是因为观察到了物体受热时膨胀和金属煅烧时重量增加这类现象。在这种情况下,认为热是某种物质实体,那是很自然的。因此,十八世纪中,人们作了种种努力,试图测定物体的温度和重量之间的相伴变化如果有的话。所得到的实验结果看来是相互矛盾的。有些实验者发现,一种物质在温度增加时,继之有重量上的少许增加;有些人则观察到重量有少许减少;另一些人则看不出在温度变化时重量有什么变化。朗福尔德所做的实验是这类实验中最为精致的。他的结果是否定的,这正是伯尔哈韦、布莱克和其他一些人所预料的。有关这类工作的几个最重要的阶段可按照年代顺序扼述如下。
伯尔哈韦用一块重5磅8盎司的铁进行实验(Elementa
Chemiae,Leiden,1732,I,pp.259—60;以及New Method of Chemistry,P.Shaw译,2nd ed.
,London,1741,I,p.285f.)。他先称量了冷时的铁块,当它赤热时重新称量,然后待其冷却后再进行称量。重量一直保持未变。在同样条件下,对一块铜进行试验,得到了相同结果。
布丰发现(Histoire
Naturelle,Supplement,Paris,1775,II,pp.11—13),一块“白热”的铁重49磅9盎司;但当它冷却到大气温度(当时接近凝固点)时,重量只有49磅7盎司。用其他铁块进行的实验,得到了类似结果。
罗巴克用较小的铁块和灵敏的天平重复了布丰的实验(Phil.Trans. ,1776,p.509)。他发现,1磅白热的铁在冷却时重量要减轻将近1谷;但是一块5英钱重的铁在冷却后要比烧热时稍重一些;一块热铜重约1磅,冷却时要减轻4谷,不过这被解释为因金属锈皮损失所致;一块重55磅的熟铁从白热状态冷却经过22小时,重量增加了6英钱多;这种铁的锈皮在冷时要比热时重,每2盎司8英钱增加5谷;而纯银块(热时约重2磅10盎司)冷却时重量增加5谷。
怀特赫斯特也未能证实布丰的结果(同上书,p.575)。当金或铁被加热到赤热时,会有数英钱的微量损失;但被冷却后,金又回复到原来的重量,而铁则有少许增加。他的结论是:在天平一侧的这些热金属使空气变得稀薄,而这可能引起一种向上的气流,从而导致所观察到的效应。而在布丰的实验中,大的热金属块可能致使天平的两个相对臂产生不均等的膨胀,这就引起了所观察到的差异。福代斯发现,冰块在融化为水时重量有所减轻(同上书,1785,p.361)。他从新河取1700谷水,盛在一个重451谷的玻璃容器中。密封起来后,设备和内盛物在32°F下总重
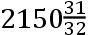 谷。在内盛物渐次部分凝固的过程中,总重量不断增加,直到全部凝固,重量总增加量略微超过
谷。在内盛物渐次部分凝固的过程中,总重量不断增加,直到全部凝固,重量总增加量略微超过
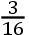 谷,温度下降到12°F。当温度上升到32°F,冰又全部融化后,这设备又回复到原来的重量。
谷,温度下降到12°F。当温度上升到32°F,冰又全部融化后,这设备又回复到原来的重量。
布莱克的关于热没有重量的观点(Lectures,Vol.Ⅰ,pp.48f.)主要建基于他对怀特赫斯特和福代斯获得的实验结果所作的解释。
朗福尔德又注意起这个问题(Phil.Trans.
,1799,p.179)。他选用了两个尽可能相似的细小玻璃烧瓶,一个里面装着蒸馏水,另一个里面装着等重量的淡酒精。两个烧瓶密封起来,在一个温度为61°F的房间里把它们悬挂在一架天平的两臂上。然后,把这套装置移到一个29°F的比较冷的房间里。48小时后,水冻结了,这时要添上0.134谷方可恢复天平平衡。然后,再把这套装置移回温度为61°F的房间里。当冰融化后,朗福尔德发现,原始重量又恢复了。实验后重新测试表明,那架天平仍然相当准确。
他所能想到的唯一解释是,水在凝固时失去了大量潜热。于是,“如果潜热损失,增加一个物体的重量,那它一定对另一物体也会产生同样效应。因此,潜热数量的增加一定——在一切物体中和在任何情况下——使它们的视重量减轻。”然而,当他把酒精换成水银,在61°F和34°F温度上复做前述实验时,却发现重量没有什么变化,尽管水失去的热比水银多得多,因为它们的比热之比为1000比33。这时,朗福尔德怀疑,可能是某种偶然因素(例如大气湿气在烧瓶上淀积,或者因微小温差而引起的局部微弱气流)造成了第一次实验中的表观重量增加。因此,他又取了三个烧瓶,瓶里分别盛有等重量的水、酒精和水银。密封后,把它们放在一个温度61°F的温暖房间中,放置24小时。由固定在烧瓶中的小温度计测得,水和酒精的温度相同。然后,把烧瓶表面的湿气仔细地全部擦去。接着,对它们进行称量,给较轻的烧瓶的瓶颈上缚上几根银丝,以达致平衡。然后,把它们全都移到一个温度30°F的冷房间中。放置48小时后发现,它们全都达到了同样温度(29°F),而重量并没有任何变化。并且,当它们又被移回温暖房间后,重量仍然相同。这个实验被重复了多次,得到的结果都一样。朗福尔德现在满意地看到,他最初的结果肯定是由于他所猜想的那些偶然因素造成的。
朗福尔德说:“既然已确定,当水从流动性状态变为冰或者反过来时,水并未获得或损失重量,所以我现在就可以与一个长期纠缠着我,给我带来许多痛苦和烦恼的课题最后告别了;既然(由于上述实验结果)已经完全相信,如果热实际上是一种实体或物质——如所假想的那样,是一种自成一类的流体——这种从一个物体转入另一物体并被累积起来的流体就是我们在加热物体中所观察到的诸现象的直接原因(然而,关于这一点,我还不能不抱有怀疑),那么,它肯定是一种无限稀疏的东西,以致我们想发现它的重量的一切努力,都将是徒劳的,即使在其最凝聚的状态下也是如此。再者,如果我们许多最有才干的哲学家们所采取的见解,即热无非是受热物体各构分的内部振动的观点确有充分根据,那么,显然,物体重量当绝不可能受这种运动影响。”
如果热是一种实体,并且具有重量,那么朗福尔德的实验应比其他任何实验都更易于检测出这种重量。因为,水在凝固时失去的140°F将把同质量的金从凝固点升温至140×20即2800°(一种炽热),这是由于金的比热是水的二十一分之一。朗福尔德下结论说:“因此,我的实验清楚地证明,相当于把4214谷(即约9.75盎司)金从水的凝固点升温到赤热状态所需的热量,对一架可示出该物体重量的百万分之一这样小的变化的天平没有产生什么明显的影响。如果金在从水的凝固点被加热到炽热状态时,其重量尚未增加或减少百万分之一,那么,我认为,我们就可以有把握地得出结论:任何试图发现物体视重量会受热影响的努力都将是徒劳的。”
八、热的动力说
朗福尔德
继布莱克、拉瓦锡和拉普拉斯关于热的实验工作之后,本杰明·汤普森爵士,即朗福尔德伯爵(1753—1814)又对之作出了重要贡献。

图93—朗福尔德
汤普森出生在马萨诸塞州,从在塞勒姆的一个商人那里做学徒开始了他的生涯。后来,他在哈佛大学听过课,此后当了教员。他曾任职于朗福尔德(现在叫康科德)的一所学校,与当地的一个治安官的遗孀结婚。于是,他定居该地经营如此归属于他的田产。他一直对机械发明深感兴趣,这时他进入了一个研究火药性质的时期。独立战争期间,他曾因同情英国政府而遭监禁。最后,他横渡大西洋去到英国,任职于殖民部。在伦敦,他对科学的兴趣使他赢得了约瑟夫·班克斯爵士的友谊。1779年,他被选为皇家学会会员。1784年,在美国担任了为时不长的军职后,汤普森(这时已是爵士)便开始服务于巴伐利亚选帝侯。其后在慕尼黑度过的十一年中,他积极致力于改组巴伐利亚军队,并热心于解决贫民问题,试图采取一种激进但又人道的解决措施——设立国家济贫院。1791年,汤普森被封为这个帝国的伯爵,他是凭他在美国的田产取得爵位的。1795年他曾离开慕尼黑,一度特别关注爱尔兰的社会问题。但不久他又被召回巴伐利亚。当时由于法国和奥国两军对峙,巴伐利亚的中立受到威胁。汤普森在这场危机中始终统率着慕尼黑守军。组建皇家研究院是朗福尔德的又一项事业。但是,1805年他与化学家拉瓦锡的遗孀结了婚,因而他在法国的奥特伊尔度过最后几年,直到1814年去世。在慕尼黑监督镗削炮筒期间所进行的一些观察促使他从事热的研究。他经过研究而相信,热是一种“运动模式”(mode of motion)。朗福尔德创设了皇家学会的“朗福尔德勋章”,授予在热和光的应用方面作出卓越贡献的人,他本人因在燃料节约烟囱设计等等方面的贡献而第一个获得了这种荣誉。
他在慕尼黑从事镗削炮筒工作期间,惊讶地观察到,镗削刀具对炮筒的作用产生了大量的热。按照热质说的解释,这是因为在镗削过程中,金属碎屑的热质被挤压出来,致使碎屑的热容量减小,这时这热质表现为可感知的热。然而,量热测验表明,与杆金属的热容量相比,金属碎屑的热容量并未发生什么变化。在1798年进行的一次镗削生热的实验中,让一个黄铜圆筒顶住钢镗刀转动(图94)。这圆筒放在一个木箱里面,木箱中盛有1834磅水。这构成了一个量热器,因为可以通过观察水温的上升来测量所产生的热量。水温从60°F开始经2.75小时上升到沸点(212°F)。用朗福尔德的话来说:“当在场的人目睹没有用火便把这么多水实际上加热到了沸腾时,他们脸上现出了无法形容的惊异神色。”这热显然是仅仅由机械手段本身产生的。但是,朗福尔德却对热的由来感到疑惑。他说:“鉴于这个实验所用的机械用一匹马的力量就可以容易地使之转动……所以,这些计算进一步表明了,不用火、光、燃烧或化学分解,仅仅用这匹马的力量,就可借助适当的机械装置产生多大的热量。这个装置浸没在水中,所以,热显然不是来自空气。”量热测量表明,碎屑的热容量并未发生变化。所以,如果热质说是正确的话,那么,给定质量的金属可产生的热量就应当有一个限度。然而,这里并没有看到什么限度。于是朗福尔德写道:“在就这个问题进行的推理中,我们切莫忘记考虑那个最值得注意的条件,即这些实验中摩擦生热的源泉显然是用之不竭的。毋庸赘言,任何绝缘的物体或物体系如能无限地不断提供某种东西,那么,这种东西就不可能是物质实体。关于能像这些实验中热被激发和传送的方式一样地被激发和传送的东西,除了是运动之外,我认为,根本不可能或者至少极难形成任何别的明确观念。我根本没想妄称知道,这种据认为构成热的特定种类运动是如何以及通过何种手段或机械装置而在物体中被激发、延续和传播的”(Phil.Trans. ,1798,p.80)。

图94—朗福尔德的装置
戴维
朗福尔德的实验显然否定了热质说而支持热的动力解释。然而,他同时代科学家的理智却有很大惰性,足以抵制这种新观念。因此,热质说一直延续到了十九世纪中叶。不过,朗福尔德至少成功地使一位年轻的同时代人接受了他的热观念。这个青年注定后来要成为一个杰出人物。汉弗莱·戴维于1797—99年间,用冰块和别的物质进行了一些摩擦实验。实验结果使他确信,“热不能看做是物质”,而必须看作是一种“特殊的运动,也许是物体微粒的一种振动”(Works,ed.1839,Vol.Ⅱ,pp.11—14;原载Contributions to Physical and Medical Knowledge,T.Beddoes编,Bristol,1799,pp.16—22)。年轻戴维所进行的摩擦实验在设计和操作方面尚不能令人满意(参见Andrade,Nature,1935,p.359 ff.)。有些历史学家对青年戴维在这方面的功绩估价过高。
九、关于混合热的其他研究
正当布莱克在苏格兰进行他的物理研究时,约翰·卡尔·维尔克在瑞典也在对热现象进行类似研究。维尔克的方法和所得到的结果不如布莱克的那样有价值。但是,维尔克是完全独立于布莱克进行工作的,而且他的工作具有一定的历史意义。为了明白维尔克研究热现象的方式,有必要先考察一下其他几个大陆物理学家在这个特定研究领域中做过的工作。因为,他实际上是始自莫林而终于加多林的一系列研究者中的主要人物。
莫林
巴黎皇家学院的数学和天文学教授让·巴蒂斯特·莫林(1583—1656)曾试图发现关于同种液体的冷的和热的样品的混合物的最终温度的规律。当时,热和冷仍然被认为是确实的实体,尽管是相对立的;冷尚没有被认为只不过是低度的热。例如,笛卡尔认为,热乃由精细的类火微粒构成;伽桑狄则认为冷由“制冷”微粒构成。现在,莫林却深信,热和冷总是连带的,冷热两者在没有对方时哪一者也根本不存在,尽管它们能以各种比例共存。在混合的过程中,热和冷相互交换,而不是被消灭;作用和反作用仅仅发生在两种以较大程度对立的相反性质之间,而当以较小程度对立时,则它们变为被加强;一定数目“热度”的总“效力”等于同等数目“冷度”的“效力”。莫林认为,冷和热这两个性质都有某个不可超越的最高度,以及某个不可再降的最低度。他设想热的单位与冷的单位相加之和总是等于8。于是,当在一种物质中热和冷相等时,则冷和热各有4个单位存在。如果热超过冷,则可能有5个单位热和3个单位冷,或者,6个单位热和2个单位冷,或者,7个单位热和1个单位冷。如果冷超过了热,则可能有5个单位冷和3个单位热,或者,6个单位冷和2个单位热,或者,7个单位冷和1个单位热。当然,中间的分数比例也是可能的。但是,在莫林看来,不可能有例如6个单位热和3个单位冷等任何总数不等于8的比例。莫林自己从来没有说过这些话,但他的论证蕴涵着这一切意思。(参见D.Mckie和N.H.de
V.Heathcote:The Discovery of Specific and
latent Heats,London,1935,pp.55—59,149—51。)
现在设想,含有2个单位热和6个单位冷的给定量的水,与含有4个单位热和4个单位冷的同体积的水相混合。这混合物将有怎样的热度呢?它不可能只有2°的热,因为在这种情况下,较热的水中所含的4个单位热中有2个单位将未对较冷的水起任何作用就消失了。这混合物也不可能含有4°的热,因为在这种情况下,较冷的水中所含的6个单位冷中有2个单位将未对较热的水起任何作用就消失了。但是,在莫林看来,热和冷的单位都不会被消灭;它们只能改变比例。因此,这混合物一定含有多于2°而少于4°的热。可是,莫林并不认为,它将含有3°热。他解释说,如果这混合物含有3°热,因而含有5°冷,那么,较冷的水所含的6°冷将仅仅把较热的水中的4°热减少1°,而较热的水中所含的4°热将把较冷的水中的6°冷减少1°,而他认为这种不均衡是不可能的。因此,这混合物一定含有少于3°的热,以对较冷的水中的6°冷和较热的水中的4°热产生成比例的效应。由于两者的比例是3比2,所以,莫林最后得出结论:这混合物将含有
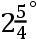 热和
热和
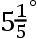 冷,结果,较冷的水所含有的超出较热的水中的4°冷的2°冷就将把较热的水的热减少了6/5度,而较热的水所含有的超出较冷的水中的2°热的2°热则将把较冷的水的冷减少
冷,结果,较冷的水所含有的超出较热的水中的4°冷的2°冷就将把较热的水的热减少了6/5度,而较热的水所含有的超出较冷的水中的2°热的2°热则将把较冷的水的冷减少
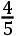 度。这样,这两个效应就将成3∶2的比例。(参见他的Astrologia Gallica,Lib.Ⅷ,Cap.Ⅹ Ⅴ,pp.158f.)如果莫林一以贯之地遵照他关于热和冷的单位仅仅相互混合而不相互消灭的假设,则他就会把两份水样品中的冷和热单位相加,即2+4的热和6+4的冷,这样他也就会得出3单位热对5单位冷的混合比例。这本来是正确的,至少就热度来说是这样。由于离奇地发挥才智,他错过了真理。然而,他还是有功绩的,使克拉夫特注意起这个问题。
度。这样,这两个效应就将成3∶2的比例。(参见他的Astrologia Gallica,Lib.Ⅷ,Cap.Ⅹ Ⅴ,pp.158f.)如果莫林一以贯之地遵照他关于热和冷的单位仅仅相互混合而不相互消灭的假设,则他就会把两份水样品中的冷和热单位相加,即2+4的热和6+4的冷,这样他也就会得出3单位热对5单位冷的混合比例。这本来是正确的,至少就热度来说是这样。由于离奇地发挥才智,他错过了真理。然而,他还是有功绩的,使克拉夫特注意起这个问题。
克拉夫特
格奥尔格·沃尔夫冈·克拉夫特(1701—54)当时在圣彼得堡当数学教授,后来当物理学教授,以后又到蒂宾根当教授。他做了各种热学实验,试图推广莫林关于不同温度的水的混合物的最终温度的公式。他完全只字不提冷的单位,局限于以华氏温度计量得的热度。他提出的一般公式如变换为现代记号,则可表示如下:
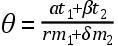 ……(A)
……(A)
式中θ是混合物的温度,m1和m2是水的两个数量,t1和t2为它们各自的温度,α、β、γ、δ是待定系数。于是,当t2=t1时,则θ=t1;上式便成为
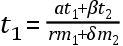 ,因而β=γm1+δm2-α,及α=γm1+δm2-β。将β的值代入原式,我们得到
,因而β=γm1+δm2-α,及α=γm1+δm2-β。将β的值代入原式,我们得到
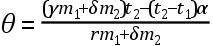 ……(B)
……(B)
同样,把α的值代入原式,我们得到
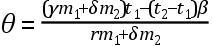 ……(B′)
……(B′)
再者,当热水(在t2上)的数量与冷水(在t1上)相比可以忽略地小的时候,则θ=t1,及γm1=α;如果反过来,则分别按(B)和(B′)式,有θ=t2和δm2=β。用这些值代替(A)式中的α和β,我们得到方程:
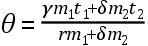 (C)
(C)
为了确定系数γ和δ的值,克拉夫特把温度分别为44°F和120°F的等量的水相混合。这混合物的温度为76°F。在这种情况下,m1=m2;t1=44;t2=120;θ=76。因此,根据(C)式,γ=11,δ=8及
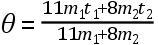 。他用不同温度的各种数量的水相混合,观察混合物的温度,由此反复证实了这个公式。(参见他的De Calore e Frigore Experimenta
Varia,载Comment.Acad.Sci.Imp.Petrop. ,1744—6,Vol.Ⅺ Ⅴ,p.218。)
。他用不同温度的各种数量的水相混合,观察混合物的温度,由此反复证实了这个公式。(参见他的De Calore e Frigore Experimenta
Varia,载Comment.Acad.Sci.Imp.Petrop. ,1744—6,Vol.Ⅺ Ⅴ,p.218。)
里希曼
在克拉夫特的结果发表之前,里希曼曾做过类似的工作,但其记录丢失了。读过克拉夫特的论文后,里希曼继续研究这个问题。格奥尔格·威廉·里希曼(1711—53)是圣彼得堡的实验哲学教授。就在那里,一场大雷雨中,因他自己的测量大气电的仪器放电,他被击身亡。
里希曼从一个明确的假设出发:一种物质的热,或至少一种液体的热,是在这物质中到处均匀扩散的。因此,一给定热量的强度将与它弥漫于其中的那物质的质量成反比。这样,如果质量为m1的某液体的热具有强度t1,并且还使它弥漫质量为m2的附加液体,那么,这混合物的温度必定为
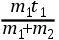 ,若假定这附加液体自己没有热。然后,设想相反的情形,即附加质量(m2)具有自己的温度,比如说t2,而m1自己没有热,那么,最后的温度将是
,若假定这附加液体自己没有热。然后,设想相反的情形,即附加质量(m2)具有自己的温度,比如说t2,而m1自己没有热,那么,最后的温度将是
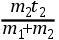 。但是,如果m1具有温度t1,m2具有温度t2,那么,根据类比,混合物的最后温度θ应为
。但是,如果m1具有温度t1,m2具有温度t2,那么,根据类比,混合物的最后温度θ应为
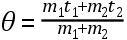 。里希曼由此得到了他的公式(这里对这个公式用较新的记号复述):
。里希曼由此得到了他的公式(这里对这个公式用较新的记号复述):
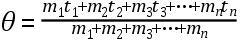 。
。
正如里希曼所深信的那样,这个公式形式上是可以扩张的,这样就可覆盖包括任何多种不同质量和温度的液体样品的混合物。它的最概括形式可表达为:
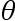
大家一定已经注意到,里希曼的公式是抽象先验思考的结果,而不是经验观察或实验的成果。它充其量是一种有待证实的尝试性假说。里希曼多少意识到了这一点,于是便寻求实验证实。起先,他为此援用关于克拉夫特实验的已发表的记录。他表明,若适当考虑到容器、温度计和空气所吸收(或者可能是给出)的热,克拉夫特的公式就不如他本人的公式符合观察结果。不过,他后来做了一系列实验,并将结果报告给圣彼得堡的帝国科学院。他仍然坚持认为,如果适当考虑到混合水样品的容器以及用来测量最终温度的温度计所吸收的热,与克拉夫特的公式相比,他自己的公式更密切地与实验结果吻合。然而,在作这些考虑时,里希曼并未试图独立地评估这些容差,而是把所观察到的实际温度与在假设容器和温度计不影响结果的情况下,按照他自己的公式混合物所应有的温度相比较,由此推出这些容差。他根本没有想到,这样的方法实际上是用未加证明的假定来作为论据。(参见里希曼关于“Formulae”等等的研究报告,载Nov.Comment.Acad.Sci.Imp Petrop.
,1747—48,Vol.Ⅰ,p.168ff.)
维尔克
约翰·卡尔·维尔克(1732—96)是斯德哥尔摩军事学院的实验物理学教授。在一生的最后十年里,他任了瑞典科学院的秘书。他对里希曼的工作很熟悉,并接受后者关于确定混合液温度的公式。由于一个幸运的机遇,他致力于热的实验研究。1772年初,斯德哥尔摩发生了一场暴风雪。维尔克想融化他庭院中的积雪。他原以为热水可以融化数量比热水自身重量多得多的雪。令他惊讶的是,事情并非如此。于是,他推测,里希曼关于液体混合物的定律并不适用于水和雪的混合物。他通过实验研究发现了一些问题。例如,温度在冰冷的水与温度为68℃的等量的水混合后,混合物的温度为34℃;而当把温度68℃的水灌注于等量的雪时,水温降到0℃,而且尚有一些雪仍未融化。于是,维尔克便开始进行了一系列漫长而又系统的实验,以发现关于水和雪的混合物的温度的规律。(参见K.Svenska Vet.Akad.Handl. ,1772,Vol.Ⅹ Ⅹ Ⅹ Ⅰ Ⅱ,p.97ff.)
他首先发现,给定重量的雪与等重量的各种温度的水相混合时,混合物的温度要比不用雪而用0℃的水时平均约低36℃。接着他观察到,当与雪混合的水重量加倍时,混合物的温度要比不用雪而用0℃的水时平均约低24℃。同样,当水的重量三倍于雪时,这平均损失约为18°;当水的重量四倍于雪时,这平均损失约为14.3℃;当水重五倍于雪时,平均损失约为12.125℃;当水重六倍于雪时,平均损失约为
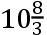 ℃;如此等等。维尔克立即看出,上述混合物温度的损失的数值都是72的分数;他就得出结论:把雪融化掉恰好需要72°的热,只有超出这72°的热才能帮助雪所化成的冰冷水升高温度。这样,维尔克独立于布莱克地发现了雪熔解的潜热,尽管他对潜热的估计值不如布莱克的精确,而且时间上也晚了10年左右。这里还应提到,维尔克还发现了下面这个包含给定重量的雪(n)与给定重量(m)和给定温度(t)的水的混合物的温度(θ)的一般公式:
℃;如此等等。维尔克立即看出,上述混合物温度的损失的数值都是72的分数;他就得出结论:把雪融化掉恰好需要72°的热,只有超出这72°的热才能帮助雪所化成的冰冷水升高温度。这样,维尔克独立于布莱克地发现了雪熔解的潜热,尽管他对潜热的估计值不如布莱克的精确,而且时间上也晚了10年左右。这里还应提到,维尔克还发现了下面这个包含给定重量的雪(n)与给定重量(m)和给定温度(t)的水的混合物的温度(θ)的一般公式:
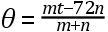
发现了雪在融化时吸收72℃的热而同时并不发生升温的现象之后,维尔克很自然地就联想到:水冻结时,要放出72℃的热;如果认为冰冷水仅仅部分地冻结,则这水便把72℃的热给予其余的水,而所形成的冰与原来作为冰冷水的状态相比并不发生降低温度。但是,他未能成功地用实验来证实这一思想。同时,他也没有意识到他的失败的含义所在,即较冷物体并不把热传给较热物体。只要再敏锐一些,维尔克就有可能看到热力学第二定律的线索。
维尔克发现,雪在转化成冰冷水时吸收了温度计所不能直接测出的热。他觉得,既然这样,就可以着手解决困扰他同代人的那个问题,这就是比热问题。当时已经观察到,如果把体积和温度都相同的两种物质(例如金和锡)浸入具有同样较低温度的等量的水之中,则水温的增加与被浸物质的密度成正比地变化。因此,看来较密的物质比较疏的物质含有更多的热,尽管这是一种用温度计不能直接检测到的热。经过对多种物质进行了大量实验,维尔克得出结论:不同物质的热一般不与它们的体积或密度本身成正比,不过,每种物质都吸收、保留和放出一定量的热,而这热与水或某种其他标准物质的热的比就可称为它的比热。他又进一步解释说,任何一种物质的比热可看作是,与同温度的水(或某种其他用作比较标准的物质)的一个微粒所含有的热量相比,该物质的一个微粒所含有的热量。维尔克的比热概念多少有些类似于潜热的概念,所以,他很自然地力图利用他在水和雪的混合物的温度研究中所获得的知识,以确定各种物质的比热。他尝试过各种方法。最简单的乃基于下述发现:要测定一个物体含有的热量,可先确定把该物体从某给定温度冷却到凝固点所需要的雪量,而为此所需之雪量可以间接地测定。这种方法可简述如下。其比热待确定的物质(譬如一块金)先被加热到一定温度,继之被浸入等重量的0℃的水中,再记下最后温度。然后,用里希曼的公式(见第221页)计算,为给出当加上等质量的0℃的水时所观察到的温度之上的混合物,需要多少处于被测物质温度的水。最后,应用维尔克自己的公式(见第223页)来计算为把上述混合物的温度降低到0℃必需多少雪。这样,维尔克以水的比热为单位,确定了下列物质的比热:金(0.050)、铅(0.042)、银(0.082)、铋(0.043)、铜(0.114)、铁(0.126)、锡(0.060)、锌(0.102)、锑(0.063)、玻璃(0.187)。(参见K.Svenska Vet.Akad.Nya Handl.
,1781,Vol.Ⅱ,pp.49ff.)布莱克在比热方面的工作要先于维尔克二十年左右,维尔克通过第二手材料对之略有所闻。在结束这一部分之前,还可以再就加多林对这一科学分支的贡献说几句。
加多林
约翰·加多林(1760—1852)出生于芬兰,是柏格曼的门生,舍勒的朋友。他是一位杰出的化学家,发现了一种稀土物质——氧化钇,稀有金属钆(gadolinium)即是为纪念他而命名的。这里,我们只谈他在热学方面的工作。他看来是最早引入适当考虑到比热的混合物温度公式的人之一,如果不是第一个人的话。从里希曼的公式
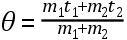 出发,加多林指出,当相混合的物质属不同种类时,用这公式就不能正确计算出混合物的最后温度;必须考虑到它们在比热上的差异。于是,加多林给出了下列公式:s1∶s2∶∶m2(θ-t2)∶m1(t1-θ)式中s1和s2表示两种被混合物质的比热,其余符号的意义与里希曼公式中的符号相同。当然,加多林的公式可以扩充,以便适合于两种以上不同物质的混合物。此外,与里希曼不同,加多林认真尝试得出研究混合物温度时所必须考虑的混合物传给容器的热的正确的独立估计值,取得了相当的成功。他得出了一个公式,用以估算对混合物温度产生相当于容器影响的液体的质量。他的公式为
出发,加多林指出,当相混合的物质属不同种类时,用这公式就不能正确计算出混合物的最后温度;必须考虑到它们在比热上的差异。于是,加多林给出了下列公式:s1∶s2∶∶m2(θ-t2)∶m1(t1-θ)式中s1和s2表示两种被混合物质的比热,其余符号的意义与里希曼公式中的符号相同。当然,加多林的公式可以扩充,以便适合于两种以上不同物质的混合物。此外,与里希曼不同,加多林认真尝试得出研究混合物温度时所必须考虑的混合物传给容器的热的正确的独立估计值,取得了相当的成功。他得出了一个公式,用以估算对混合物温度产生相当于容器影响的液体的质量。他的公式为
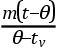 式中m代表混合液的质量,t代表混合液的温度,θ为液体和盛此液体的容器的温度,tv为空容器的温度。(参见J.Gadolin和N.Maconi:Dissertatio chemicophysica de Theoria Caloris Corporum Specifici,Äbo,1784。)
式中m代表混合液的质量,t代表混合液的温度,θ为液体和盛此液体的容器的温度,tv为空容器的温度。(参见J.Gadolin和N.Maconi:Dissertatio chemicophysica de Theoria Caloris Corporum Specifici,Äbo,1784。)
十、不可见的辐射热
始于十七世纪的关于不可见辐射热的研究在1682年后的大约八十年中一直没有什么进展。然而,这段时期却为这个问题的进一步研究间接地作了准备。因为,在这几十年中,取火镜和透镜大大改进,温度计在结构和分度方面也大有进步。这些改良的仪器是这个领域里的重要工具。因此,在十八世纪后半期关于这些问题的工作恢复以后,就取得了进展。
沃尔夫描述过一些抛物取火镜以及霍夫曼用这些镜所做的某些实验(Phil.Trans.
,1769,p.4)。有一个实验中,把火的热聚集于一面凹镜的焦点上。在另一个实验中,把燃烧着的煤放在一面凹镜的焦点上,再利用两面反射镜,把位于另一面镜焦点上的燃料点燃。用一个强加热的火炉重复这个实验,并且仍把燃料点着。托马斯·扬在他的《自然哲学讲演录》(Lectures on Natural
Philosophy)(1807年)(I,p.637)中说,霍夫曼第一个以这种方式即利用一面或几面镜的反射,把炉火发出的不可见热收集起来。布丰给出了比霍夫曼更加令人满意的证明(Histoire
Naturelle,Supplément,1774,I,p.146)。“我用一面取火镜接收了相当强烈的热而没有任何光,方法是在明亮的火和镜之间放上一块铁板。一部分热被射到镜的焦点,而其余的热则全都穿透这镜。”(霍夫曼似乎没有注意将他用的热源——火炉的光的踪迹完全消除。)在同一本书中,布丰还写道:“似乎……应当认识到有两种热,一种是发光的……另一种是隐蔽的。”他的实验证明,具有不可见热的物体发射出能够像光线那样反射的不可见射线。
第一个在这领域进行系统实验的是舍勒。他力图调和理论和实验。他提出了一种关于辐射热和光的理论,它既符合既有事实,又不与流行的燃素说相悖。他在《关于空气和火的化学论文》(Chemical Treatise on Air and
Fire)(乌普萨拉,1777年;英译本:L.Dobbin,伦敦,1931年,p.120)中提到一个实验。放在一面金属凹镜焦点上的“明亮的赤热木炭”的热可以在另一面类似的镜的焦点上加以收集,在那里这时可把燃料点燃起来。他问道:这效应究竟应归因于热还是光,还是这两者。在为解答这问题的实验中,他仔细区分了辐射热和对流热,对前者进行研究。舍勒所用的热源是一个开口炉。炉子辐射出的热不受炉口上方强烈对流的影响。然后,他在自己面孔和炉子之间放上一块大玻璃板,这样,他就感觉不到任何热了。接着,他研究涂银玻璃的和金属的平面的和凹面的镜对射线的反射。用涂银玻璃实验时,他发现,光被玻璃反射,而热被吸收。用金属镜实验时,光和热都遵循同太阳光线一样的反射定律。在火炉的射线穿过一块玻璃板后,即使用透镜或镜聚集,这些光线也不产生热。
舍勒用放在火炉前2厄尔 [4] 处的一面金属凹镜造成一个点燃磷的焦点。他还注意到,镜并未变热,但如果把镜放在燃烧的蜡烛上方被烟灰熏黑,然后再放到炉子前面的这个位置上,没过几分钟,它就灼烫手了。金属镜和金属板与热物体接触时就变热——但不是来自火炉的热。当把火炉顶端的烟道堵住,热空气就要从火炉打开的门向上逸出,而若把金属凹镜或金属板放在这上升的热之中,则这热并不反射,但金属变热了。
因此,舍勒推论出辐射热的某些性质。他写道:“由这些实验可知,同炉中空气一起上升而通过烟道的热实际上是与通过炉门进入房间的热不同的;热从其发源处出发直线地行进,又被抛光金属以等于入射角的反射角反射;它不与空气相结合,因而,除了在生成开始时接受的方向外,它不可能再从气流得到任何其他方向。”(上引书,p.123)他还说:“这些都是属于光的性质。”但他不认为光是这些现象的原因,因为(1)火光与太阳光相比实在太弱;(2)当燃用木材并烧成“明亮的赤热木炭”时,用引燃磷来检验的一个焦点的热比较强,因而发出的光较弱;(3)用玻璃镜可以把火的热和光分开,玻璃镜反射光而保留热。
因此,舍勒得出结论:辐射热具有光的某些性质,但它尚未成为光,因为它受玻璃表面的反射不同于受金属表面的反射——“一个值得注意的事实!”他写道(上引书,p.123)。于是,他把这种热称为“辐射热”,并以此回答他最初提出的问题,即为什么从赤热木炭反射的射线能引燃燃料,指出这要归因于“这种不同于火的不可见辐射热”(上引书,p.125)。
在进一步对光进行的实验中,舍勒宣称,他业已证明,辐射热的点火力不是由于辐射热中的光;但是,只有火的辐射热才是这样,太阳光线的辐射热则并不如此,而如马里奥特所已表明的那样,太阳的光和热同样好地穿过玻璃。他的结论是:辐射热是一种物质实体,火、空气和燃素的一种化合物,而光则是一种含较多燃素的类似化合物。
于是,舍勒引入了“辐射热”这个术语,并描述了这种热的一些主要性质,还把它与光区分开来。他的实验要比他的理论思辨更有价值得多,而这些思辨往往是错误的。例如,他认为,紫色和紫红色含有的燃素较少,因为它们较易被棱镜吸引(即它们被较厉害地折射);因此,既然辐射热含有的燃素更少,它就应当更易被吸引。所以,不可见的热射线似乎就处于光谱紫端之外。他大概没有用实验检验这一点。
J.H.兰伯特提出了两个证据(参见Pyrometrie,1779,§378),证明火的热不是以光的形式,而是以隐蔽热的形式存在:(1)因为透明玻璃保护了面孔,使其不受极强火的热的影响,直到玻璃本身变热,和(2)因为由一面取火透镜聚焦在手上的极强火的像也丝毫不令人感觉到热。这样,玻璃和其他透明物体就把火的光和热分离了开来——让光透射,而将热吸收。火的热不能为透镜所聚集,但却可由镜来聚集。(有人说,早在1685年察恩就已在维也纳表明了这一点,但似乎查无实据。)兰伯特成功地重复了这些实验。放在一面凹镜(焦距18英寸)焦点上的木炭火发出的射线,被放在对面的、相距20到24英尺的一面较小凹镜(焦距9英寸)收集了起来;把放在焦点上的火绒等物点燃。这些镜显然是金属的。兰伯特说,这个结果完全是由隐蔽热所致,尽管光也被聚集在焦点上。兰伯特的实验支持舍勒的结论。
克里斯提到(Annales de Chimie et de
physique,1809,71,158)一部著作,题为《关于安德列·格特纳新发明的木质抛物镜及其惊人作用的说明》(An account of parabolic wooden mirrors and their
surprising action,newly invented by André
Gaertner)(1785年),其中描述了一个实验,该实验演示了从一个被烧热了的铁火炉发出的隐蔽热的反射。当在10到12步之外用抛物镜把它的热聚集起来时,其热等于在两倍于此距离之外明火的热。格特纳还描述了,如何在他的镜的焦点上放上冰,结果在10到12步之外产生十分明显的冷。
德索絮尔认为(Voyages dans les
Alpes,1786,II,pp.353f.),兰伯特的实验还不是决定性的——热源应当是不发光的。所以,他就用一只很热的但并非赤热的铁丸同皮克泰一起在后者的仪器上重复做了那些实验。两面大小和焦距相同的凹锡镜相对地放置,隔开12英尺2英寸。铁丸先被加热到赤热,然后待其冷却到在黑暗中已不可见时,把它放在第一面镜的焦点上。另一面镜的焦点上放上一支温度计的泡,这样这温度计所指示的温度比仅仅直达射线产生的温度高8°,后者用一支恰在焦点外面的温度计指示。做实验的房间里此外便没有别的热源;而且,用不同的温度计在不同的日子都得到了同样的结果。只要把温度计稍稍移开焦点,就会使温度显著下降,几乎降到室温。所以,对于隐蔽热的反射来说,这些实验是令人满意的。至于这种隐蔽热的本性,德索絮尔认为,它是物体中热流骚动引起的热振动的反射,这种振动能像声波那样被反射。他提出了一种测量其速度的实验。这实验后来由皮克泰进行,如这里将要说明的。
德吕克认为(Idées sur la
Météorologie,1786—87),热的反射为下述事实证明:盛有水的金属锅在外侧磨光时比外侧带有灰垢时要花费更长的时间才能烧沸水,因为火微粒是按照适用于一切回跳物体的反射定律(入射角=反射角)而从抛光表面反射的。他还认为,太阳光线本身并不是热的,而是由于跟存在于大气中的一种物质相结合才变热的,这种物质使太阳光线失去发光的性质。因此,德吕克反对迪卡拉的见解。后者在其《完全的火》(Feu
Complet)中把太阳光线的发光能力和发热能力归因于一种共同的动因。
1788年,爱德华·金描述了一些实验(Morsels of
Criticism,Ⅰ,99),其中沸水发出的不可见热被凹镜反射并由一面凸透镜折射到一个焦点上。但是,值得怀疑的是,根据他的实验中可观察到的微小效应,他是否有理由得出热流体具有同光线一样的可反射性和可折射性的结论。在后来利用金属凹镜的实验中,他让火的热被反射,并注意到“金属在作此用途时要比玻璃灵验得多”。
M.A.皮克泰于1790年指出(Essais de Physique,英译本:An Essay on Fire,W.B.译,1791),“释出的火”(即辐射热)“是一种遵循某些定律并以某速度运动的不可见射气”(英译本,p.8)。他把它与光相比。因为没有光照样可以得到热,没有热也照样可以得到光,所以,他断言,两者的关系如同一个整体之于一个部分。至于这种“释出的火”的本性,根据它的简单性,他赞成这样的理论:它是一种实在的射气,而反对这样的观点:它是无所不在的、完全弹性的热流体的简单振动。他用一只热铁球重复他以前与德索絮尔一起做过的(关于隐蔽的热的反射的)实验(如前所述),证明一支小蜡烛也产生同等的效应,但用一块玻璃板就可把热削减三分之二。为进一步证明不可见热的反射,皮克泰又用一小烧瓶沸水进行实验。这是一个令人满意地、不发光的热源。两面镜相距10英尺6英寸,结果2分钟后水银温度计就上升了3.125°F,而且一当把烧瓶从焦点移开,温度就下降。他表明,纯粹的热像光一样也可被黑体吸收,因为当他把温度计泡涂黑后,温度计上升4.125°F,而且上升得更快。当把一块玻璃板放在两面镜之间时,大部分热都被吸收了。
由于热按同光一样的定律反射,所以皮克泰便把烧瓶中沸水的热用一面凹锡镜反射到一面凸透镜上,凸透镜的焦点处有一支温度计,以此来测验折射。他用了三个不同的透镜,但在焦点处并未发现比其他地方有更多的热,因此问题仍然悬而未决。他还试图按照德索絮尔提出的方法测量辐射热的速度。一只在黑暗中不可见的热铁球被放在第一面锡镜的焦点上,并用一块厚厚的屏把它与另一面镜屏蔽开。在第一面镜对面69英尺处放一面镀金的大镜,其焦点处有一支灵敏的空气温度计。这一切都就绪后,把屏移开,温度计立即就上升,没有任何令人觉察得到的时间间隔。因此,皮克泰得出结论:他所称的“释出的火”“向一切方向以相当快的速度——或许像声甚或像光一样迅速——直线地”运动;而且他在此也称之为“辐射热”(英译本,p.113)。
皮克泰还尝试对冷的反射进行了实验。两面锡镜相距10.5英尺地放置;一个充满雪的烧瓶放在第一面镜的焦点上,一支灵敏空气温度计的泡放在第二面镜的焦点上。结果,温度立即降低了几度,而当把烧瓶从焦点处移开后,温度计便又上升了。当把硝酸注到雪上(以得到较低的温度)时,产生了更为明显的效应。皮克泰对这些事实的最后解释乃遵照我们现在就要讲到的普雷沃理论。
1791年,普雷沃发表了他关于辐射热通过不断交换而平衡的理论(Observations sur
la
physique,1791,38,314)。这一理论的基础是德吕克的热理论(认为热是一种离散流体,其微粒处于不断运动之中)以及皮克泰对冷的表观反射的演示。实际上,普雷沃理论的目的主要就是为了解释这一令人费解的现象。普雷沃从比较光与辐射热(“完全自由的火”)出发,得出了这样的结论:实验证据尽管有限,但仍证明了这样的结论:光和辐射热在性质上是相似的,特别就它们传播的直线性和即时性而言。因此,他认为,热和光是相似的离散流体。以空间中具有相同温度的两相邻部分为例,他坚持认为,这两个部分之间通过辐射不断交换热。这些交换是等同的,因而这两部分处于相对平衡,它们的温度保持恒定。这样,如果某一部分变热,则它将给出的热多于它从别的部分接收到的热,直到在更高的温度上达到新的平衡。
这一理论对冷的表观反射给出了十分令人满意的解释;因为一个冷物体在一个焦点上比一个较热物体在另一个焦点上发出较少的热,这使较热物体冷却下来,由于它接收的辐射热比发出的少。可见,温度计上的效应不是因为冷的反射,而是因为热沿反方向的反射。皮克泰立即接受了这种解释。
詹姆斯·赫顿重复了舍勒的关于玻璃片对火发出的射线的效应的实验,发现热并未完全被吸收,而只不过在强度上有所减弱罢了(Dissertation on the Philosophy of Light,Heat and
Fire,Edinburgh,1794)。他谴责了“隐蔽热”的观念,说“设想热离开物体而运动,或者热按照光的定律反射,这无疑是一个玷污科学的观念”。他认为,这些效应倒是起因于不可见的光,这种光因为太微弱而不能使人眼感觉到,但其强度却足可传送热。
于是,及至1800年,存在着不可见热射线的观念已为人们公认。当时已经知道,这种射线几乎瞬时地直线传播,并按照和光线一样的定律反射。人们还猜想,这种不可见热射线也能像光线那样折射。这些同光的相似性导致人们猜测,两者是相联系的。赫顿甚至论证说,不可见热射线实际上就是不可见的光。但是,由于玻璃对火的热和光射线呈现不同的吸收效应,所以大多数科学家都暂不表示决定性的意见,把这种不可见热射线称为“隐蔽热”或“辐射热”。当时提出了两种理论,即(1)不可见热射线是一种物质的射气,和(2)它们是一种无所不在的热流体的振动。其中前一个受到较为广泛的支持。冷的反射已得到了演示和解释。实验主要是定性的,但已为定量研究准备好了活动场地。
(参见D.McKie和N.H.de V.Heathcote,The Discovery of Specific and Latent Heats,London,1935;EäMach,Prinzipien der Wärmelehre,Leipzig,1923;E.S.Cornell,“Early Studies in Radiant Heat”,Annals of Science,1936,Vol.Ⅰ,p.217;以及第181—182页上所列有关物理学的一般书目。)
[1] 德莫尔沃、拉瓦锡、贝尔托莱和富尔克罗在《化学命名法》(Methóde de Nomenclature Chimique)(巴黎,1787年,p.30f.)中用“热质”(caloric)这个术语代替了“热的物质”(matter of heat)的旧用语。
[2] “比热”(Chaleur
specifique)这一术语最早出现在马热朗的《略论关于火素和物体的热的新理论》(Essai sur la Nouvelle
Théorie du Feu
Élémentaire
et de la Chaleur des
Corps,1780)中,文中用它表示单位质量某物质在给定温度下的总热量。
[3] 谷(grain),重量单位,等于64.8毫克。——译者
[4] 厄尔(ell),古尺名,英国=4.5英寸。——译者注