-
1.1前 言
-
1.2医学免疫学实验课的目的和要求
-
1.3医学免疫学实验室守则
-
1.4第一章 固有免疫实验
-
1.4.1实验1 溶菌酶的溶菌作用
-
1.4.2实验2 中性粒细胞吞噬功能实验
-
1.4.3实验3 硝基四氮唑蓝(NBT)还原实验
-
1.4.4实验4 巨噬细胞吞噬功能实验
-
1.4.5实验5 巨噬细胞移动抑制实验
-
1.4.6实验6 NK细胞活性测定
-
1.5第二章 抗原抗体参与的实验
-
1.5.1实验7 直接凝集反应
-
1.5.2实验8 间接凝集实验
-
1.5.3实验9 间接凝集抑制实验
-
1.5.4实验10 类风湿因子乳胶凝集实验
-
1.5.5实验11 人类ABO血型鉴定实验
-
1.5.6实验12 单向免疫扩散实验
-
1.5.7实验13 双向琼脂扩散实验
-
1.5.8实验14 对流免疫电泳
-
1.5.9实验15 火箭免疫电泳
-
1.5.10实验16 免疫电泳
-
1.5.11实验17 免疫印迹技术
-
1.6第三章 补体参与的实验
-
1.6.1实验18 溶血空斑实验
-
1.6.2实验19 补体结合实验
-
1.6.3实验20 总补体活性测定
-
1.6.4实验21 循环免疫复合物的检测
-
1.7第四章 淋巴细胞检测实验
-
1.7.1实验22 B淋巴细胞膜表面免疫球蛋白(SmIg)测定
-
1.7.2实验23 SPA花环实验
-
1.7.3实验24 外周血淋巴细胞分离法
-
1.7.4实验25 E花环形成实验
-
1.7.5实验26 T淋巴细胞亚群的检测
-
1.7.6实验27 淋巴细胞转化实验
-
1.7.7实验28 抗体介导的细胞毒实验
-
1.7.8实验29 微量淋巴细胞毒实验
-
1.7.9实验30 混合淋巴细胞培养法
-
1.7.10实验31 细胞毒性T细胞杀伤功能测定
-
1.8第五章 免疫标记技术
-
1.8.1实验32 免疫荧光技术
-
1.8.2实验33 酶联免疫吸附实验
-
1.8.3实验34 生物素-亲和素技术
-
1.8.4实验35 斑点金免疫渗滤实验
-
1.8.5实验36 斑点免疫层析实验
-
1.8.6实验37 酶免疫组化技术
-
1.8.7实验38 酶标免疫定量测定
-
1.8.8实验39 放射免疫分析技术
-
1.9第六章 免疫分子检测实验
-
1.9.1实验40 SPA协同凝集实验
-
1.9.2实验41 免疫浊度实验
-
1.9.3实验42 辛酸-硫酸铵法提取血清中的IgG抗体
-
1.9.4实验43 白细胞介素-2活性测定
-
1.10第七章 超敏反应实验
-
1.10.1实验44 植物血凝素皮肤实验
-
1.10.2实验45 豚鼠速发型过敏反应
-
1.10.3实验46 豚鼠结核菌素实验
-
1.10.4实验47 小鼠DNFB实验
-
1.10.5实验48 小鼠DTH实验
-
1.10.6实验49 肥大细胞脱颗粒实验
-
1.11【附录Ⅰ】 显微镜的结构、使用与保护
-
1.12【附录Ⅱ】 流式细胞术简介
-
1.13【附录Ⅲ】 实验动物的抓取、固定和注射方法
-
1.14【附录Ⅳ】 免疫学实验常用试剂的配制
-
1.15【附录Ⅴ】 常用玻璃器皿及玻片洗涤法
-
1.16【附录Ⅵ】 常用实验小鼠简介
-
1.17【附录Ⅶ】 常用生物制品介绍
-
1.18【附录Ⅷ】 免疫血清的制备
-
1.19【附录Ⅸ】 溶血素的制备
-
1.20【附录Ⅹ】 兔抗人血清的制备
-
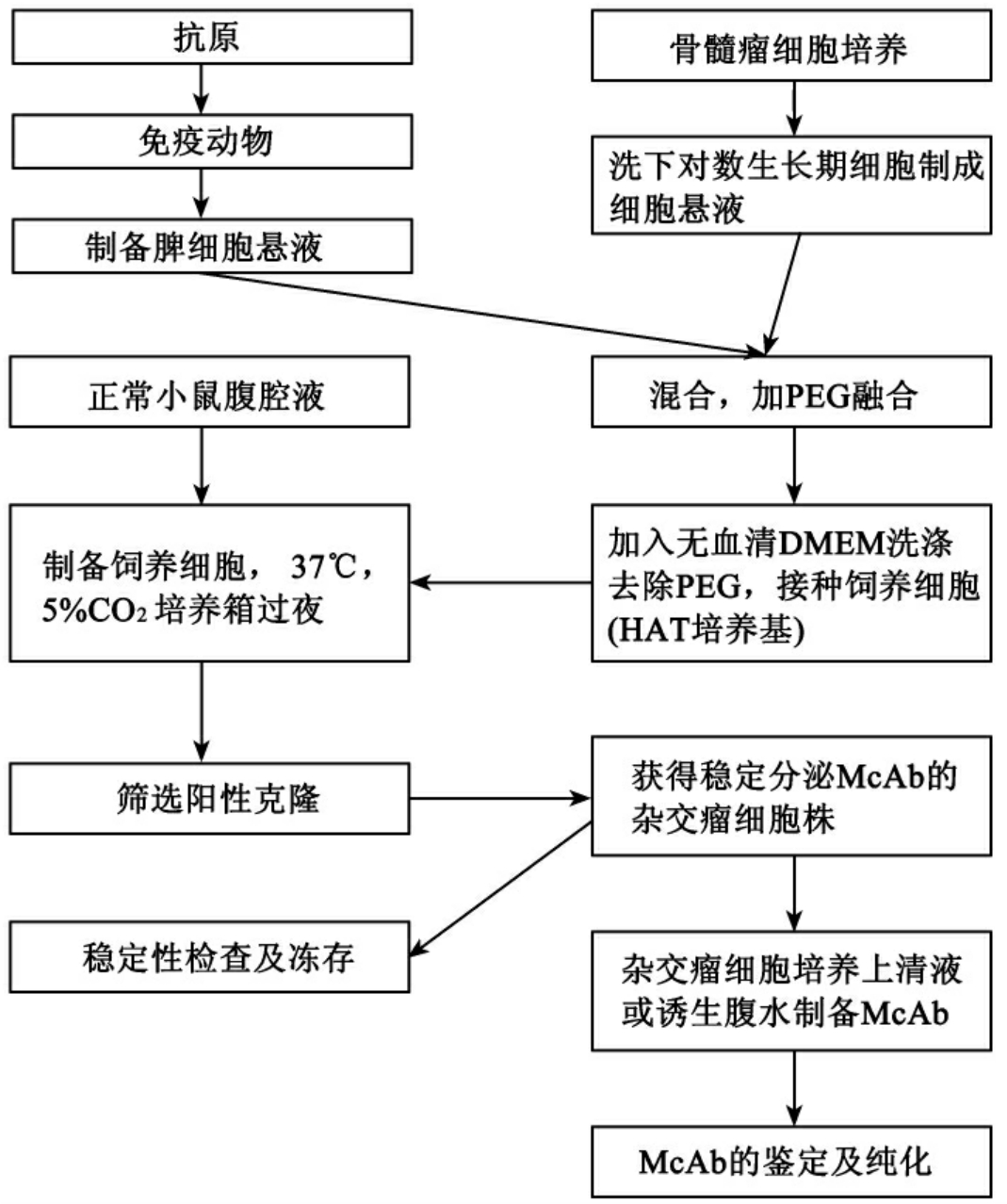
1.21【附录Ⅺ】 单克隆抗体的制备
-
1.22主要参考资料
1
医学免疫学实验教程