无机化学
-
1.1编委会
-
1.2前言
-
1.3目录
-
1.4项目1 实验室常识及数据表达
-
1.4.1任务1.1 遵守实验室规则
-
1.4.2任务1.2 注重实验安全
-
1.4.2.11.2.1 实验室安全守则
-
1.4.2.21.2.2 实验室事故处理
-
1.4.2.31.2.3 实验室废液处理
-
1.4.2.41.2.4 培养良好的学风
-
1.4.3任务1.3 测量误差与有效数字
-
1.4.3.11.3.1 误差与偏差
-
1.4.3.21.3.2 误差的种类及其产生原因
-
1.4.3.31.3.3 提高测量结果准确度的方法
-
1.4.3.41.3.4 有效数字
-
1.4.4任务1.4 化学实验中的数据表达与处理
-
1.5项目2 原子结构与元素周期表
-
1.5.1任务2.1 原子核外电子的运动状态
-
1.5.1.12.1.1 人类对原子结构的认识
-
1.5.1.22.1.2 原子的组成
-
1.5.1.32.1.3 同位素
-
1.5.1.42.1.4 电子的波粒二象性
-
1.5.2任务2.2 原子结构的近代概念
-
1.5.2.12.2.1 波函数和量子数
-
1.5.2.22.2.2 电子云
-
1.5.3任务2.3 原子中核外电子的排布
-
1.5.3.12.3.1 核外电子排布规律
-
1.5.3.22.3.2 基态原子电子构型和价电子构型
-
1.5.3.32.3.3 原子结构和性质的周期性规律
-
1.5.3.42.3.4 元素周期表的意义及应用
-
1.6项目3 分子结构
-
1.6.1任务3.1 离子键
-
1.6.1.13.1.1 离子键的形成
-
1.6.1.23.1.2 离子键的特征
-
1.6.1.33.1.3 离子键的本质
-
1.6.1.43.1.4 离子键的离子性成分
-
1.6.2任务3.2 共价键
-
1.6.2.13.2.1 现代价键理论
-
1.6.2.23.2.2 杂化轨道理论
-
1.6.3任务3.3 金属键
-
1.6.4任务3.4 分子间作用力与氢键
-
1.6.4.13.4.1 分子的极性
-
1.6.4.23.4.2 分子间作用力
-
1.6.4.33.4.3 氢键
-
1.7项目4 溶液
-
1.7.1任务4.1 分散系
-
1.7.1.14.1.1 分散系的概念
-
1.7.1.24.1.2 分散系的分类
-
1.7.2任务4.2 溶液浓度的表示方法
-
1.7.2.14.2.1 溶解
-
1.7.2.24.2.2 溶液组成标度
-
1.7.2.34.2.3 溶液组成标度之间的换算关系
-
1.7.3任务4.3 稀溶液的依数性
-
1.7.3.14.3.1 蒸气压下降
-
1.7.3.24.3.2 沸点升高
-
1.7.3.34.3.3 凝固点下降
-
1.7.3.44.3.4 溶液的渗透压
-
1.7.4任务4.4 胶体和表面现象
-
1.7.4.14.4.1 溶胶的性质和结构
-
1.7.4.24.4.2 溶胶的稳定性和聚沉
-
1.7.4.34.4.3 高分子溶液
-
1.7.4.44.4.4 表面现象
-
1.8项目5 化学平衡
-
1.8.1任务5.1 可逆反应与化学平衡
-
1.8.1.15.1.1 可逆反应
-
1.8.1.25.1.2 化学平衡
-
1.8.2任务5.2 标准平衡常数
-
1.8.2.15.2.1 实验平衡常数
-
1.8.2.25.2.2 标准平衡常数
-
1.8.2.35.2.3 平衡常数的书写
-
1.8.3任务5.3 标准平衡常数的应用
-
1.8.3.15.3.1 判断反应程度
-
1.8.3.25.3.2 预测反应方向
-
1.8.3.35.3.3 平衡组成的计算
-
1.8.4任务5.4 化学平衡的移动
-
1.8.4.15.4.1 浓度对化学平衡的影响
-
1.8.4.25.4.2 压强对化学平衡的影响
-
1.8.4.35.4.3 温度对化学平衡的影响
-
1.9项目6 酸碱反应
-
1.9.1任务6.1 酸碱的解离理论
-
1.9.1.16.1.1 酸碱的定义
-
1.9.1.26.1.2 酸碱反应
-
1.9.1.36.1.3 酸碱的强度
-
1.9.1.46.1.4 酸碱的其他理论
-
1.9.2任务6.2 水溶液中酸或碱的解离平衡
-
1.9.2.16.2.1 水的离子积和溶液的pH
-
1.9.2.26.2.2 解离理论中的常数
-
1.9.2.36.2.3 一元弱酸、弱碱的解离平衡
-
1.9.2.46.2.4 多元弱酸的解离平衡
-
1.9.3任务6.3 同离子效应和缓冲溶液
-
1.9.3.16.3.1 同离子效应
-
1.9.3.26.3.2 缓冲溶液
-
1.9.4任务6.4 盐类的水解
-
1.9.4.16.4.1 弱酸强碱盐
-
1.9.4.26.4.2 弱碱强酸盐
-
1.9.4.36.4.3 弱碱弱酸盐
-
1.9.4.46.4.4 影响盐类水解的因素
-
1.10项目7 氧化还原反应
-
1.10.1任务7.1 氧化还原反应的基本概念和配平
-
1.10.1.17.1.1 氧化数
-
1.10.1.27.1.2 氧化还原反应的基本概念
-
1.10.1.37.1.3 氧化还原反应方程式的配平
-
1.10.2任务7.2 电极电势
-
1.10.2.17.2.1 电极电势的产生
-
1.10.2.27.2.2 标准氢电极和甘汞电极
-
1.10.2.37.2.3 标准电极电势
-
1.10.2.47.2.4 影响电极电势的因素——能斯特(Nernst)方程
-
1.11项目8 配位化合物
-
1.11.1任务8.1 配合物的组成、命名和异构现象
-
1.11.1.18.1.1 配合物的组成
-
1.11.1.28.1.2 配合物的命名
-
1.11.1.38.1.3 配合物的分类
-
1.11.2任务8.2 配位平衡
-
1.11.2.18.2.1 配离子在水溶液中的解离平衡
-
1.11.2.28.2.2 配位平衡的移动
-
1.11.3任务8.3 配位化合物的应用
-
1.11.3.18.3.1 配合物在元素分离和分析化学中的应用
-
1.11.3.28.3.2 配合物在冶金工业中的应用
-
1.11.3.38.3.3 配合物在工、农业领域中应用
-
1.11.3.48.3.4 配合物在生物科学和医药领域中应用
-
1.12项目9 实训
-
1.12.1实训1 化学实训安全教育及认识
-
1.12.2实训2 溶液的配制
-
1.12.3实训3 凝固点降低法测定葡萄糖相对分子质量
-
1.12.4实训4 溶胶的制备和性质
-
1.12.5实训5 化学反应速率和化学平衡
-
1.12.6实训6 粗食盐的提纯与质量检验
-
1.12.7实训7 解离平衡和沉淀反应
-
1.12.8实训8 缓冲溶液的配制和性质
-
1.12.9实训9 氧化还原反应与电极电势
-
1.12.10实训10 配位化合物的组成和性质
-
1.13附录
-
1.13.1附录1 化学实训须知
-
1.13.1.1一、化学实训学生守则
-
1.13.1.2二、化学实训安全守则
-
1.13.1.3三、化学实训室事故处理
-
1.13.2附录2 无机化学实训常用仪器介绍
-
1.13.3附录3 一些物理量的单位和数值
-
1.13.3.1一、基本国际制单位和符号
-
1.13.3.2二、一些导出国际制单位
-
1.13.3.3三、一些非国际制单位及其与国际制单位的换算
-
1.13.4附录4 常见弱酸、弱碱在水中的解离常数
-
1.13.4.1一、弱酸在水溶液中的解离常数(25 ℃)
-
1.13.4.2二、弱碱在水溶液中的解离常数(25 ℃)
-
1.13.5附录5 常见配合物的稳定常数
-
1.13.6附录6 常见无机化学试剂及其配制
-
1.13.6.1一、化学试剂的规格和选用选择
-
1.13.6.2二、市售常用酸碱试剂的浓度、含量及密度
-
1.13.6.3三、常用无机化学试剂及其配制
-
1.13.7附录7 常用缓冲溶液及其配制
-
1.13.7.1一、标准缓冲溶液及其配制
-
1.13.7.2二、常用标准缓冲溶液pH
-
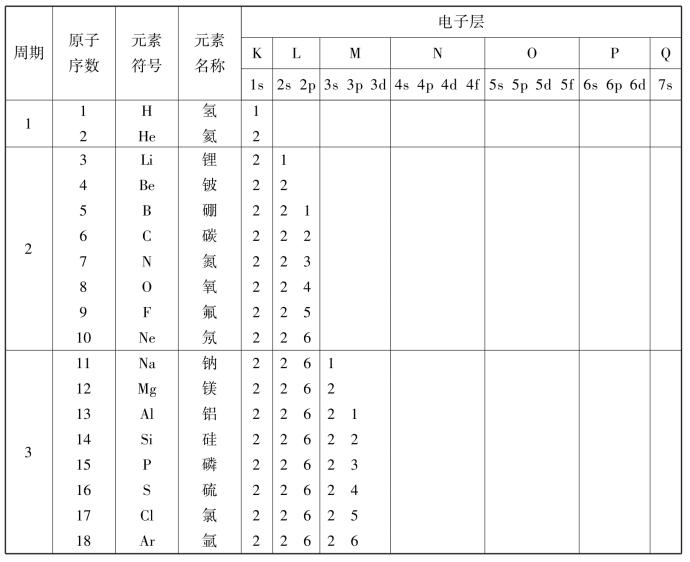
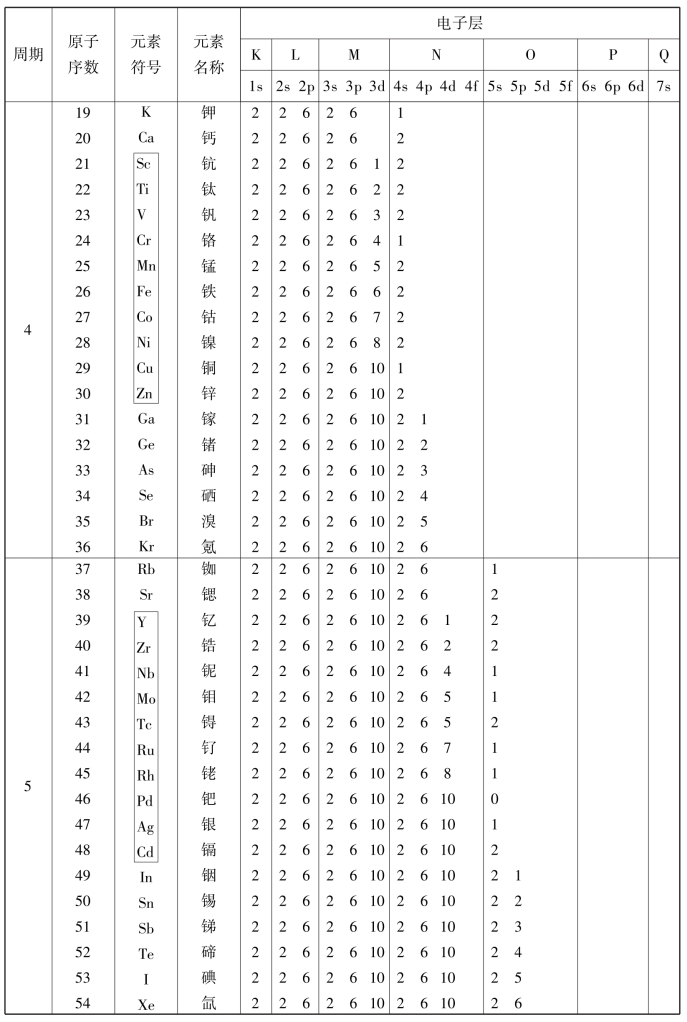
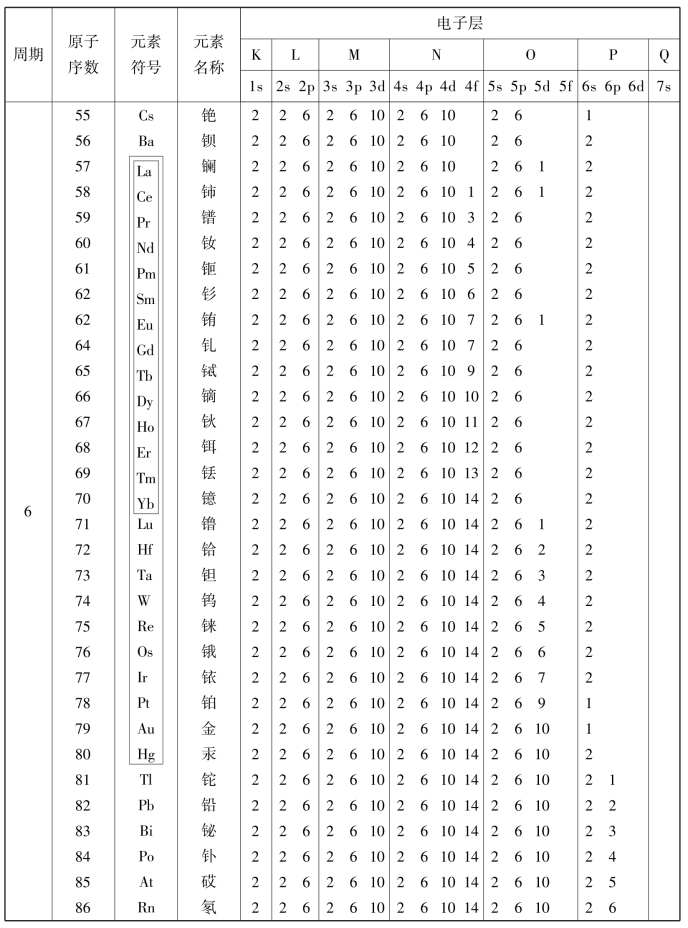
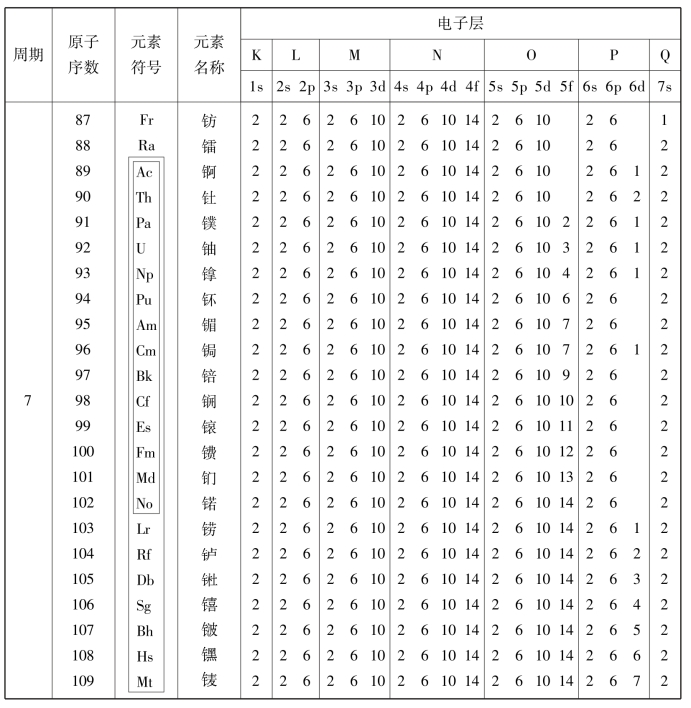
1.13.8附录8 元素周期表
-
1.14参考文献