第一节 分子病
分子病(molecular disease)是指由于基因突变使蛋白质的分子结构或合成的量异常,直接引起机体功能障碍的一类疾病。包括血红蛋白病、血浆蛋白病、受体病、膜转运蛋白病、结构蛋白缺陷病和免疫球蛋白缺陷病等。
Neel(1949)在研究一种呈常染色体隐性遗传的镰状细胞贫血病时,发现无症状的父母(杂合子)具有与患者相似的红细胞形态异常,只是其程度较轻。同年,后来曾两度获得诺贝尔奖医学奖或生理学奖的著名学者L.Pauling认为这可能是由于血红蛋白分子的缺陷所致,并提出了分子病这一概念。事实上,随着现代医学进入分子医学时代,许多非遗传性疾病也列入分子病之中。
一、血红蛋白病
血红蛋白(hemoglobin,Hb)是存在于红细胞中具有重要生理功能的蛋白质。血红蛋白分子合成异常引起的疾病称血红蛋白疾病(hemoglobinopathy),习惯上分为血红蛋白病和地中海贫血(thalassemia)两类。血红蛋白病表现为血红蛋白分子的珠蛋白肽链结构异常,如发生在重要功能部位的氨基酸被替代,将影响到血红蛋白的溶解度、稳定性等生物学功能;地中海贫血的特征是珠蛋白肽链合成速度降低,导致α链和非α链合成的不平衡,在临床上表现为溶血性贫血。分子遗传学研究表明,不管是血红蛋白病还是地中海贫血,其分子基础是共同的,都是珠蛋白基因的突变或缺陷所致。
全世界至少有1.5亿人携带血红蛋白病或地中海贫血的基因,他们主要分布于非洲、地中海地区和东南亚人群中。血红蛋白病在我国的总发生率为0.24%~0.33%,以云南、贵州、广东、广西壮族自治区和新疆维吾尔自治区等地最高,而α地中海贫血和β地中海贫血的发生率分别为2.64%和0.66%,它们多见于华南、西南和华东地区。
(一)血红蛋白分子的结构及在发育阶段时的变化
1.血红蛋白分子的结构 血红蛋白是红细胞的主要成分,是血液中红细胞携带、运输氧气和二氧化碳的载体。血红蛋白是一种结合蛋白,蛋白质部分称为珠蛋白(globin),辅基为血红素,结构为2对单体(亚基)组成的球形四聚体(图5-1),其中1对由2条类α珠蛋白链(α链或ζ链)各结合1个血红素组成;另1对由2条类β珠蛋白链(ε、β或δ链)各结合1个血红素组成。α链由141个氨基酸组成,β链则由146个氨基酸组成。在人个体发育的不同阶段,类α链和类β链的不同组合,构成了人类常见的几种血红蛋白(表5-1)。
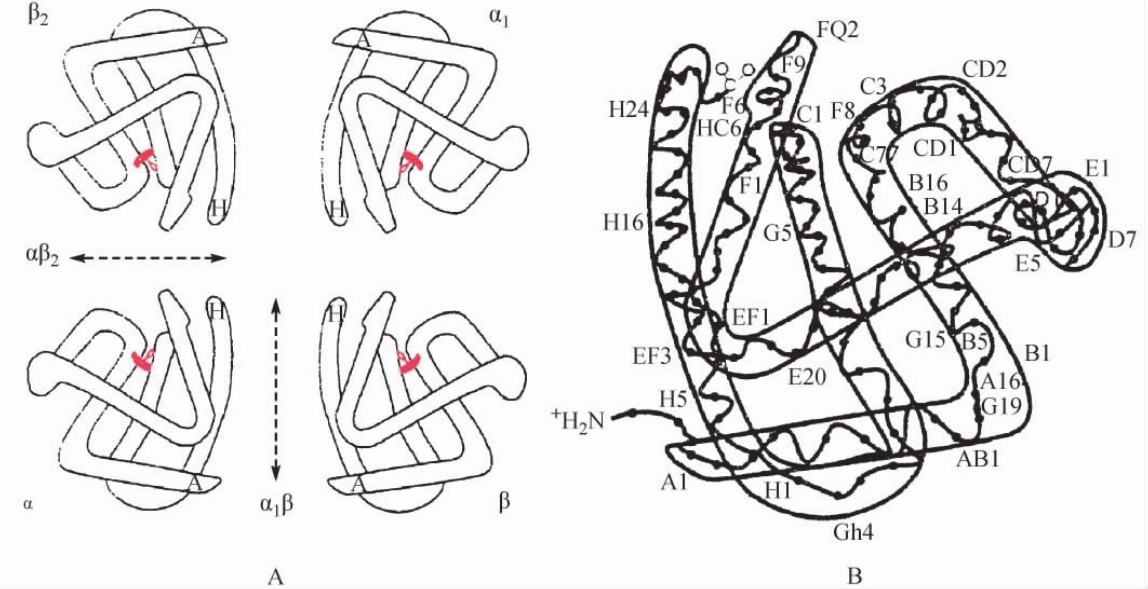
图5-1 血红蛋白的结构示意图
表5-1 正常人体血红蛋白
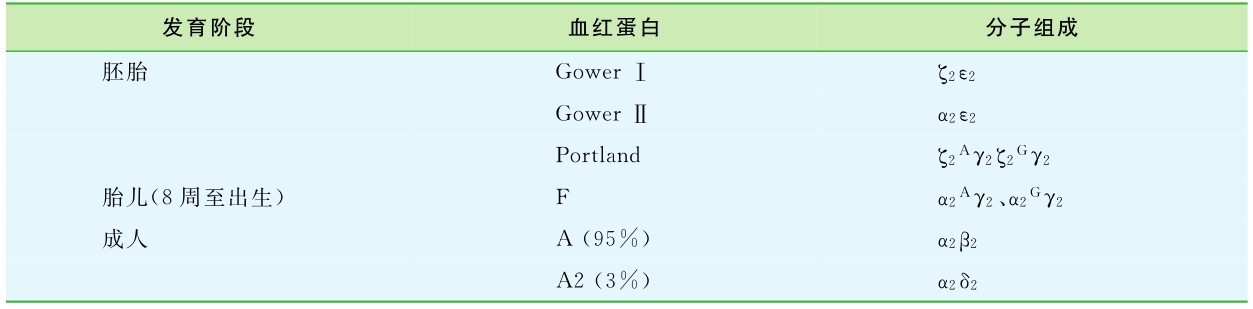
2.珠蛋白基因及其表达特点 人的6种珠蛋白链各由相应的珠蛋白基因编码,包括类α珠蛋白基因和类β珠蛋白基因两类,它们各含数个相同或相似的基因,紧密排列在DNA的特定区段,构成了基因簇。人的类珠蛋白基因簇中存在着一些拟基因(pseudogene),如ψα、ψζ、ψβ。
类α珠蛋白基因簇定位于16pter-pl3.3(OMIM#141800),按5′→3′方向排列顺序为:5′-ζ2-ψζ1-ψα1-α2-α1-3′(图5-2),总长度为30kb。每条16号染色体有2个α基因(正常人的α基因用αA表示),正常的二倍体细胞有4个α基因,每个α基因表达的α珠蛋白数量相同。类α珠蛋白基因的排列顺序与发育过程中表达顺序相一致。即发育早期是5′端ζ表达,正常成人主要是3′端的α基因表达。
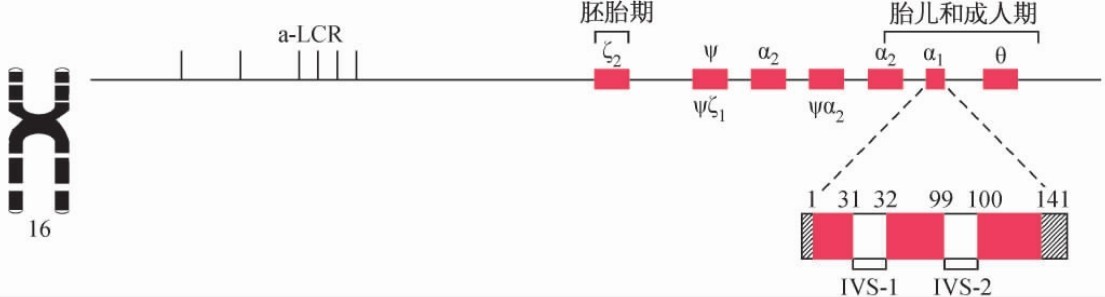
图5-2 类α珠蛋白基因簇和α珠蛋白基因的结构
人的类β珠蛋白基因簇定位于11p15.5(OMIM#141900),按5′→3′方向排列顺序为:5′-ε-Gγ-Aγ-ψβ1-δ-β-3′(图5-3),总长度为60kb。每条11号染色体只有1个β基因(正常人的β基因用βA表示),正常的二倍细胞有2个β基因。类β珠蛋白基因的排列先后与发育过程的表达顺序相关,发育早期是5′端ε、γ基因表达,成人期主要为3′端β基因表达。
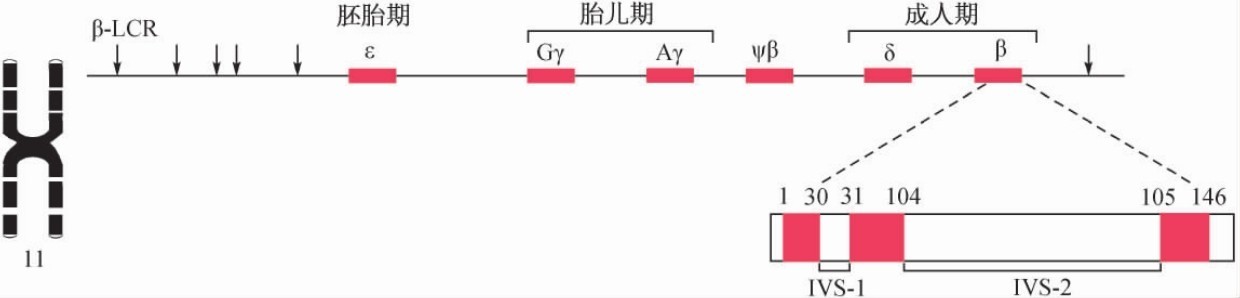
图5-3 类β珠蛋白基因簇和β珠蛋白基因的结构
各种珠蛋白基因均含有3个外显子(E)和2个内含子(I)。α珠蛋白基因的I1位于31位和32位密码子之间,由117bp组成。I2位于90位和100位密码子之间,含140bp(见图5-2)。β珠蛋白基因中的I1位于30位和31位密码子之间,为130bp;而I2位于104位和105位密码子之间,约850bp(见图5-3)。
珠蛋白基因的表达受到精确的调控,表现出典型的组织特异性和时间特异性。胚胎早期(妊娠3~8周),卵黄囊的原始红细胞发生系统中,类α珠蛋白基因簇中的ζ、α基因和类β珠蛋白基因簇中的ε、γ基因表达,进而形成胚胎期血红蛋白(Hb Gower I、Hb Gower II、Hb Portland)。胎儿期(妊娠8周至出生),血红蛋白合成的场所由卵黄囊移到胎儿肝脾中,类α珠蛋白基因簇的表达基因由ζ全部变成α基因,而类β珠蛋白基因簇基因的表达由ε全部转移到γ基因,形成胎儿期血红蛋白(Hb F/α2γ2)。成人期(出生后),血红蛋白主要在骨髓红细胞的发育过程中合成,主要是α基因和β基因表达,其产物组成血红蛋白A(Hb A)(α2β2)(图5-4)。
从类α珠蛋白基因簇和类β珠蛋白基因簇的组成可知,每个二倍体个体带有4个α基因和2个β基因,但通过特殊的调控机制,正常人体中α珠蛋白和β珠蛋白的分子数量相等,正好构成血红蛋白A(HbA)(α2β2)。说明β基因的表达效率是α基因的2倍。类α珠蛋白和类β珠蛋白的平衡是人体正常生理功能的需要。
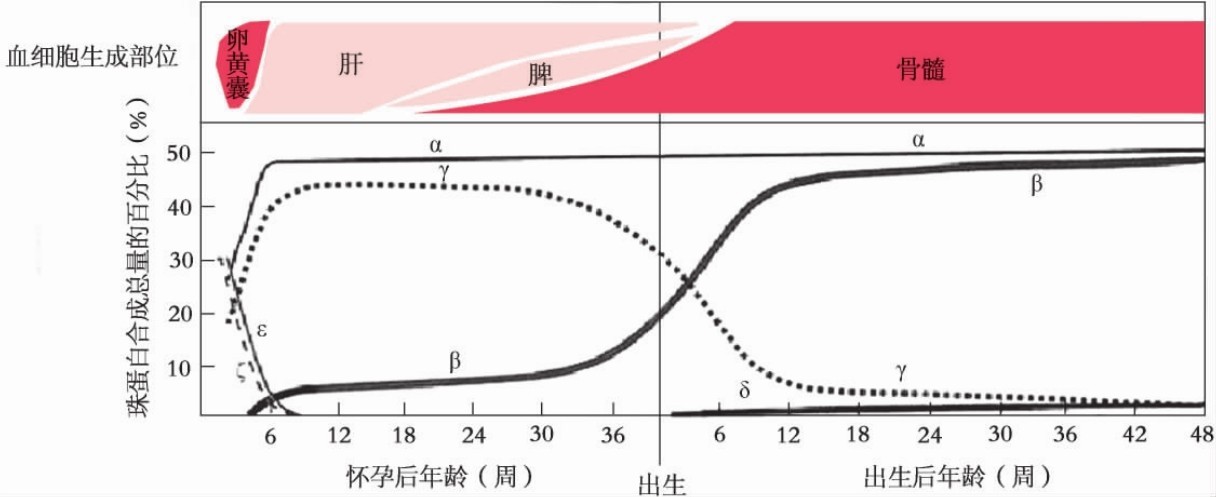
图5-4 人体不同发育时期珠蛋白基因的表达
(二)珠蛋白基因突变的类型
无论是血红蛋白病还是地中海贫血,都是以珠蛋白结构异常为特征,由珠蛋白基因突变所致,包括碱基置换、移码突变、融合基因等多种类型。
1.单个碱基替代 这是血红蛋白疾病最常见的一种突变类型,见于绝大多数血红蛋白病和β地中海贫血。
2.移码突变 由于珠蛋白基因中发生1、2个碱基的丢失或嵌入,致使后面的碱基排列依次位移,导致重新编码,使珠蛋白肽链的结构或合成速率改变。例如,Hb Wagne是由于α珠蛋白基因第138位的丝氨酸密码子TCC(mRNA为UCC)丢失1个C,导致其后的3′端碱基向5′端依次位移,重新组合及编码,结果使原来142位的终止密码子UAA变成可读密码子AAG(赖氨酸),使翻译至下一终止密码(147位)才终止,α链延长为146个氨基酸。
3.密码子的缺失和嵌入 业已发现有一些异常血红蛋白缺失或嵌入部分氨基酸。这是由于在细胞减数分裂时,同源染色体发生错配和不等交换,导致编码密码子的DNA三联碱基缺失或嵌入。
4.无义突变 无义突变是指突变使正常密码子变为终止密码子,因此蛋白质链的合成提前终止,导致地中海贫血。例如,Hb Mckees-Rock,其α链正常,β链缩短为144个氨基酸。原因是β珠蛋白基因第145位酪氨酸密码子TAT突变成终止密码子TAA(T→A),对应的mRNA变化为UAU→UAA,使肽链合成提前终止。
5.终止密码子突变 由于编码终止密码子(UAA、UAG或UGA)的DNA序列发生突变,珠蛋白链的合成不在正常的位置上终止,而继续合成至新的终止密码子,因此生成了延长的异常珠蛋白链。例如,Hb Constant Spring是由于α珠蛋白基因第142位终止密码子TAA变为谷氨酰胺密码子CAA(T→C),对应的mRNA变化为UAA→CAA,结果α链合成完141个氨基酸时并不停止,而是继续合成到下一个终止密码子(173位)才终止,使α链延长为172个氨基酸。该突变基因转录的mRNA不稳定,易降解,导致α链合成减少,从而引发一种典型的非缺失型α地中海贫血。
6.基因缺失 由于缺失的基因及部位不同,导致不同的珠蛋白肽链合成异常和不同类型的地中海贫血。
7.融合基因融合 突变的实质是两种不同基因局部片段的拼接。这种由两种不同基因局部片段拼接而成的DNA片段称为融合基因,它们可编码融合蛋白。例如,Hb Lepore,其α链结构正常,但非α链是由δ和β链连接而成,其N端像δ链,C端像β链,称为δ-β链。与此相反,另一种融合链的异常血红蛋白Hb anti-Lepore,其N端像β链,C端像δ链,称为β-δ链。这是由于染色体的错误联合和不等交换,形成了融合基因δ-β和β-δ,合成了融合链的异常血红蛋白。β和δ基因的融合意味着β基因的减缺,合成β链减少,表现为β地中海贫血的临床症状。
(三)常见的血红蛋白疾病
1.镰状细胞贫血症(镰状细胞血红蛋白) 镰状细胞贫血症(sickle cell anemia,OMIM#603903)是因β珠蛋白基因缺陷所引起的一种疾病,呈常染色体隐性遗传。患者β珠蛋白基因的第6位密码子由正常的GAG突变为GTG(A→T),使其编码的β珠蛋白N端第6位氨基酸由正常的谷氨酸变成了缬氨酸,形成血红蛋白S(Hb S)。这种血红蛋白分子表面电荷改变,出现一个疏水区域,导致溶解度下降。在氧分压低的毛细血管中,溶解度低的Hb S聚合形成凝胶化的棒状结构,使红细胞变成镰刀状。镰变细胞引起血黏性增加,易使微细血管栓塞,造成散发性的组织局部缺氧,甚至坏死,产生肌肉骨骼痛、腹痛等痛性危象。同时镰状细胞的变形能力降低,通过狭窄的毛细血管时,不易变形通过,挤压时易破裂,导致溶血性贫血(图5-5)。杂合子(Hb A/Hb S)不表现临床症状,但在氧分压低时可引起部分细胞镰变。
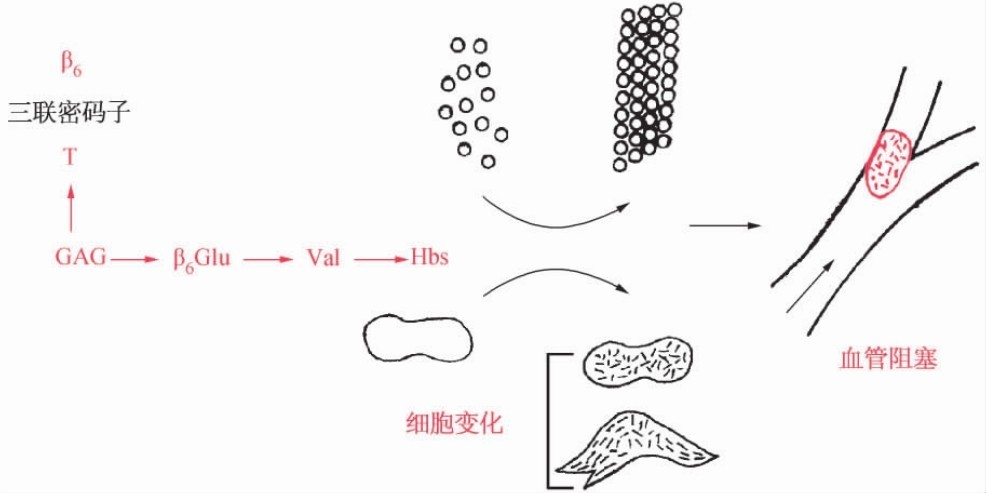
图5-5 镰状细胞贫血症的发病机制
本病主要分布在非洲,也散发于地中海地区,在东非某些地区Hb S基因频率高达40%。因此镰状细胞贫血症成为世界范围内最严重的血红蛋白病。Saiki等于1986年将PCR技术首先应用于镰状细胞贫血症的基因诊断并获得成功(图5-6),标志着对于镰状细胞血红蛋白和其他血红蛋白疾病的基因诊断进入了一个新的时期。
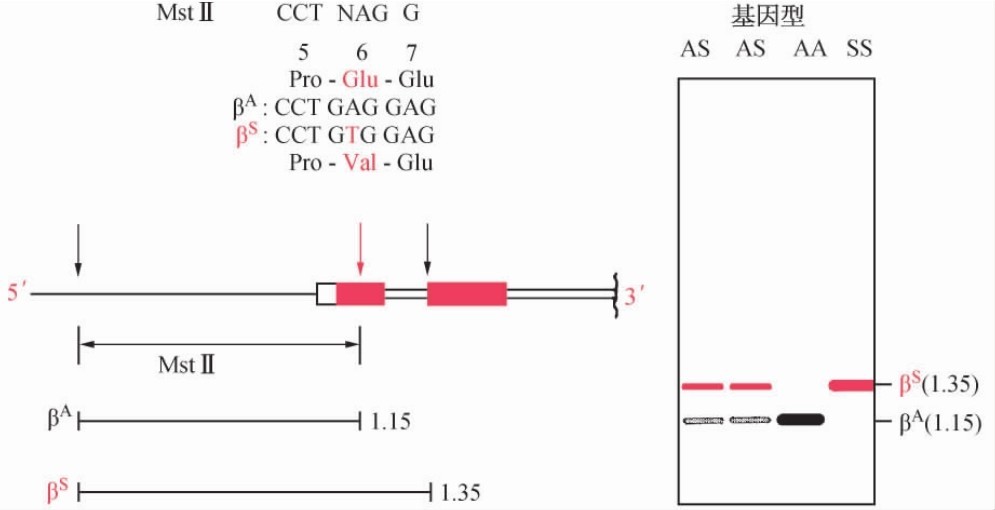
图5-6 镰状细胞贫血症的基因诊断
2.血红蛋白M病 本病又称为高铁血红蛋白症。正常血红蛋白(Hb A)血红素中的铁原子与珠蛋白链上特定的组氨酸连接(α87His,β92His)和作用(α58His,β63His),保证二价铁离子(Fe2+)的稳定,以便结合氧。血红蛋白M(Hb M)患者的珠蛋白基因中,由于上述某个氨基酸的密码子发生碱基置换,使珠蛋白链与铁原子连接或作用的有关氨基酸发生替代,导致部分血红素的Fe2+还原成高价铁离子(Fe3+),形成高铁血红蛋白(methemoglobin),影响携氧能力,使组织细胞供氧不足,产生发绀症状。血红蛋白M病呈常染色体显性遗传,杂合子Hb M的含量通常在30%以内,可出现发绀症状。
3.地中海贫血 患者由于某种或某些珠蛋白链合成速率降低,造成一些肽链缺乏,另一些肽链相对过多,出现肽链数量的不平衡,导致溶血性贫血,称为地中海贫血。按照合成速率降低的珠蛋白链类型,可以把地中海贫血区分为多种不同的类型:α珠蛋白链合成减缺的称为α地中海贫血,β链合成减缺的称为β地中海贫血,γ链合成减缺的称为γ地中海贫血,δ和β链合成减缺的称为δβ地中海贫血,以此类推。
按照珠蛋白链合成速率降低的程度,地中海贫血可以区分为不同的类型。例如,α地中海贫血,如果同一条16号染色体上的2个α珠蛋白基因均不能表达,使α链的合成完全缺乏,称为α0地中海贫血(过去称为α地中海贫血1);如果只有1个α珠蛋白基因表达,使α链部分合成,称为α+地中海贫血(过去称为α地中海贫血2)。由这两种地中海贫血基因可以组合成各种不同的综合征:α0地中海贫血基因纯合子(α0/α0)完全不能合成α链,而合成Hb Bart's(γ4),可导致死胎、死产或新生儿死亡,称为血红蛋白Bart's胎儿水肿综合征;α0和α+双重杂合子(α0/α+)只有少量α链合成,多余的β链聚合成Hb H(β4),导致一种溶血性贫血病,称为血红蛋白H病。同样,完全不能合成β链的称为β0地中海贫血,能部分合成β链的称为β+地中海贫血。β0地中海贫血基因纯合子(β0/β0)及β0和β+地中海贫血基因双重杂合子(β0/β+)都表现严重的溶血性贫血症状。对地中海贫血的分子生物学研究表明,患者珠蛋白链合成的缺乏是由于相应的珠蛋白基因缺失或者发生点突变所致。
(1)α地中海贫血:α地中海贫血主要分布在热带和亚热带地区。该病在我国也相当常见,尤其是在南方,发病率很高。因此,α地中海贫血已成为一个较严重的公共健康问题。根据临床表现,本病可分成不同的类型。不同类型的α地中海贫血患者,体内缺失(或缺陷)的α珠蛋白基因数目各不相同,缺失的α基因越多,病情越严重。常见的α地中海贫血有以下几种:
1)Hb Bart's胎儿水肿综合征:患儿发病于胎儿期,基因型为α0地中海贫血基因纯合子(--/--),4个α珠蛋白基因全部缺失。由于不能合成α链,γ链便聚合为γ四聚体(γ4)。γ4首先发现于St.Bartholomew医院,故命名为Hb Bart's。这种胎儿全身水肿,肝脾大,四肢短小,腹部因有腹水而隆起,故名Hb Bart's胎儿水肿综合征。Hb Bart's(γ4)具有很高的氧亲和力,在氧分压低的组织中,不易释放出氧,造成组织缺氧,故Hb Bart's水肿胎儿多于妊娠30~40周时死亡或早产,且早产儿于产后半小时内即死亡。如果胎儿父母为α0地中海贫血基因杂合子(--/αα)或已生育过一胎Hb Bart's水肿胎儿者,在妊娠中期孕妇有妊娠高血压和严重水肿,B超检查见胎儿异常,常提示为该病胎儿。
2)Hb H病:患者为α0地中海贫血基因和α+地中海贫血基因的双重杂合子,基因型为(--/-α)。由于4个α珠蛋白基因中有3个缺失或缺陷,使α链的合成受到严重影响,大量的β珠蛋白链过剩而聚合为β四聚体Hb H(β4)。Hb H的氧亲和力为Hb A的10倍,在正常的生理条件下不易释放出氧。更为重要的是Hb H是一种不稳定的四聚体,其β链上的巯基(-SH)易被氧化,导致β4的解体,生成游离的β4链。游离β链不能稳定地存在于红细胞内,结果沉淀聚积,形成H包涵体,附着于红细胞膜上,使红细胞膜受损,红细胞失去柔韧性,易被脾脏破坏,导致慢性溶血性贫血。Hb H病患儿在出生时几乎无明显的症状,只有轻度贫血,但Hb Bart's的相对含量可高达25%。在发育过程中Hb Bart's逐渐被Hb H替代,至1周岁左右便出现Hb H病的临床症状。这时患儿有贫血,贫血的程度可以是Hb含量在70~100g/L的轻度或中度,多数患者伴有肝脾大及轻度黄疸。少数患者病情较重,Hb含量可低至30~40g/L,并有骨骼变化及特殊贫血面容。感染和服用氧化性药物及妊娠均可使贫血加重。
3)标准型α地中海贫血:患者可能为α0地中海贫血基因的杂合子,基因型为(--/αα);或是α+地中海贫血基因的杂合子,基因型为(-α/-α),均缺失2个α基因。前一种类型在我国较多见,基因分析可呈现出东南亚型α珠蛋白基因缺失,后一种类型多见于黑种人。由于能合成相当量的α珠蛋白链,所以仅表现出轻度溶血性贫血或无症状。
4)静止型α地中海贫血:该类型为α+地中海贫血基因的杂合子,基因型为(-α/αα),缺失1个α基因。由于只有一个基因缺失或突变,故临床上无症状,仅在出生时血液中含有l%~2%的Hb Bart's,可以通过血红蛋白电泳检出。
(2)β地中海贫血:β地中海贫血是一组以血红蛋白β珠蛋白肽链(β链)合成减少(β+)或缺失(β0)为特征的遗传性血液病。本病在世界范围内广为流行,全世界至少有1.5亿人携带β地中海贫血基因。β地中海贫血好发于地中海沿岸国家和地区,如意大利、希腊、马耳他、塞浦路斯等,以及东南亚各国的广大地区。临床上根据患者溶血性贫血的严重程度,将β地中海贫血分为重型、中间型和轻型3种类型。
1)重型β地中海贫血:患者可能是β0/β0、β+/β+或δβ0/δβ0(δβ0为融合基因)等纯合子,也可能是β0和β+地中海贫血基因的双重杂合子(β0/β+)。其共同特点是患者不能合成β链,或合成量很少,结果α链过剩而沉降到红细胞膜上,引起膜的性能改变,发生严重的溶血反应,同时它们可与代偿性表达的γ链组合成Hb F(α2γ2)。患儿出生后几个月便可出现溶血反应。由于组织缺氧,促进红细胞生成素分泌,刺激骨髓增生,骨质受损变得疏松,可出现鼻塌眼肿、上颌前突、头大额隆等特殊的“地中海贫血面容”。
2)中间型β地中海贫血:一般是β+地中海贫血基因的纯合子,患者的基因型通常为β+(高F)/β+(高F)或β+/δβ+。前者为β地中海贫血变异型的纯合子,伴有Hb F(α2γ2)的明显升高。后者为两种不同变异型地中海贫血的双重杂合子。患者的症状介于重型和轻型之间,故称为中间型。
3)轻型β地中海贫血:发生于β0或β+地中海贫血基因的杂合子,无任何临床症状,需通过实验室检查才能确诊。患者主要是β+/βA、β0/βA或β0/δβA等杂合子,都带有1个正常的β基因βA,所以可以合成相当量的β珠蛋白链。患者的Hb A2(α2δ2)和Hb F(α2γ2)可代偿性增高。
大量研究资料表明,β地中海贫血除极少数是由于基因缺失引起以外,绝大多数是由于β珠蛋白基因不同类型的点突变(包括单个碱基的取代,个别碱基的插入或缺失)所致。这些点突变分别导致转录受阻,mRNA前体剪接加工错误,翻译无效,或合成不稳定的珠蛋白链而阻碍α-β二聚体形成,使珠蛋白链不平衡等。
4)遗传性胎儿血红蛋白持续症(hereditary persistence of fetal hemoglobin,HPFH):是指由于出生后γ珠蛋白链的合成不能转变为β珠蛋白链的合成,导致γ珠蛋白链过量持续合成。2分子α珠蛋白与2分子γ珠蛋白形成Hb F,一直保持高Hb F至终身。因γ珠蛋白链实质性的增加,弥补了β或δ珠蛋白链的不足,使血红蛋白四聚体2条α链和2条非α链之间保持平衡。即Hb F代偿了Hb A的缺陷,所以HPFH患者一般无明显的临床症状和血液学改变。HPFH杂合子的Hb F为17%~35%,比δβ0地中海贫血杂合子的Hb F要高,后者一般为17%~18%。类β珠蛋白基因簇发生缺失或点突变导致γ基因高表达是某些HPFH发生的分子基础。
二、血浆蛋白病
在血浆蛋白病中以血友病(hemophilia)较常见。血友病是一组遗传性凝血功能障碍的出血性疾病,包括血友病A(即血友病甲,又称凝血因子Ⅷ缺乏症,即传统所称的血友病)、血友病B(即血友病乙,又称凝血因子Ⅸ缺乏症、PTC缺乏症)及血友病C(即血友病丙,又称凝血因子Ⅺ缺乏症、PTA缺乏症)。本组疾病在先天性出血性疾病中最为常见,尤其是血友病A,而血友病C较为少见。
(一)血友病A
血友病A(OMIM#306700)是指由于血浆中凝血因子Ⅷ(FⅧ)缺乏所致X连锁遗传的凝血缺陷疾病。男性发病率较高(1/6 000),约占血友病总数的85%。
血友病A在临床上主要表现为反复自发性或轻微损伤后出血不止和出血引起的压迫症状和并发症;一般多为缓慢持续性出血,大出血罕见;出血部位广泛,体表和体内任何部分均可出血,可累积皮肤、黏膜、肌肉或器官等;关节多次出血可导致关节变形,颅内出血可导致死亡。
根据患者FⅧ的促凝活性(FⅧ∶C)及症状严重程度,血友病A可分为3型:①重型,表现为FⅧ∶C<20U/L,患者在出生后即发病,有“自发性”肌肉、关节出血,发作频繁;②中间型,表现为20U/L<FⅧ∶C<50U/L,患者的发病年龄较早,出血倾向较明显;③轻型,表现为50U/L<FⅧ∶C<250U/L,患者的发病年龄较晚,无自主性出血,关节、肌肉出血发作较少。
研究表明,FⅧ是一种复合分子,由3种成分构成:①抗血友病球蛋白(AHG);②FⅧ相关抗原(Agn);③促血小板黏附血管因子(VWF)。血友病A是因AHG遗传性缺乏所致。AHG基因位于Xq28,长约186kb,几乎占X染色体的0.1%,由26个外显子和25个内含子组成,编码2 351个氨基酸。
(二)血友病B
血友病B是凝血因子Ⅸ缺乏或其凝血功能降低而导致的一种X连锁遗传性出血性疾病。其临床症状与血友病A基本相同。血友病B发病率为1/10万~1.5/10万,占血友病疾病总数的15%~20%。该病的分子病因是位于X染色体上的FⅨ基因突变所致,故该病的遗传方式与血友病A相同,呈X连锁遗传。
人类FⅨ基因定位于Xq27.1-q27.2,全长35kb,由8个外显子和7个内含子构成。完整的人FⅨ基因的c DNA长度为2 802bp,编码序列的长度为1 383bp,应用各种限制酶和FⅨ基因探针进行DNA分析,可以对血友病B进行基因诊断。近年来,血友病B的基因治疗也取得了一些突破。
(三)血友病C
血友病C是血浆凝血因子Ⅺ缺乏引起的凝血障碍疾病,遗传方式为常染色体隐性遗传,基因定位于15q11。该病症状较血友病A和血友病B轻。
(四)血管性假性血友病
血管性假性血友病也称von Willebrand病。该病的发生主要是由于血浆中的一种大相对分子质量的糖蛋白von Willebrand因子(v WF)缺乏。v WF基因定位于12pter-p12,长度为180kb。v WF由血管内皮细胞分泌,为FⅧ的载体,并可增强FⅧ的稳定性。v WF缺乏会降低FⅧ的活性;同时由于血小板中也含有v WF,v WF缺乏也影响血小板的凝血功能。因此该病患者有明显的出血倾向,但症状较轻。
三、结构蛋白缺陷病
构成细胞的基本结构和骨架的蛋白的遗传性缺陷可导致一类结构蛋白缺陷病。这类分子病包括胶原蛋白病(inherited disorders of collagen)、肌营养不良症等。
(一)胶原蛋白病
胶原(collagen)约占人体蛋白质总量的20%以上,在不同的组织中分别由成纤维细胞、平滑肌细胞、成骨细胞、软骨细胞和某些上皮细胞合成分泌。胶原蛋白分子由3条相同或不同的α多肽链(α1、α2、α3)组成。α链的氨基酸残基约有1 000个,特点是甘氨酸、脯氨酸及羟脯氨酸丰富,不含或很少含有色氨酸、酪氨酸及甲硫氨酸。
目前已发现组织中的胶原类型有19种,分别具有不同的化学及免疫学特性,是不同结构基因的产物。Ⅰ、Ⅱ、Ⅲ型胶原合称为间质胶原(interstitial collagen)。Ⅰ型胶原主要由2条α1链和1条α2链组成,Ⅱ、Ⅲ型胶原都由3条α1链组成。3条α链均以右手超螺旋结构盘绕在一起形成原胶原分子,由原胶原分子组合成原纤维或微原纤维,再由原纤维黏合成胶原纤维(图5-7)。Ⅰ型胶原分布很广,主要存在于皮肤、肌腱和韧带中,具有很强的抗压能力。Ⅱ型胶原的分布局限于透明软骨、椎骨髓核及玻璃体中,具有较强的抗压能力。Ⅲ型胶原广泛分布于伸展性较大的组织,如结缔组织、血管壁及胎盘等处。Ⅳ型胶原由2条α1链和1条α2链组成,再聚合成交叉结构的巨分子,主要分布于各种基膜之中。
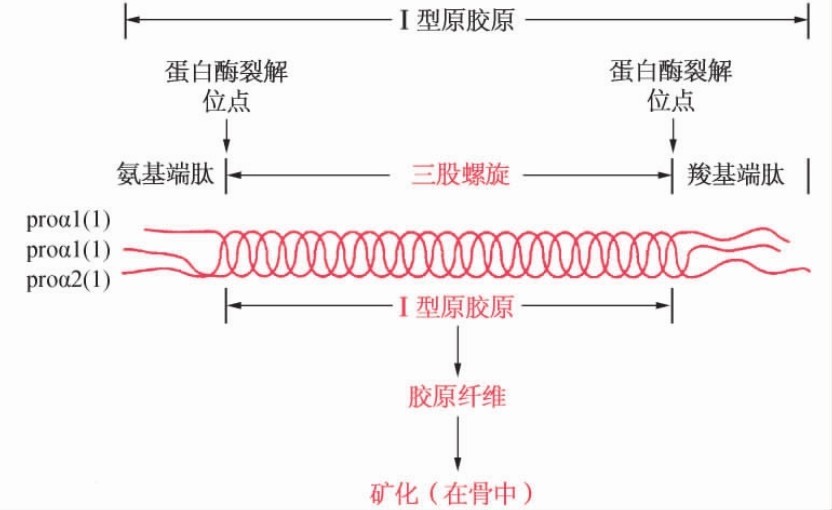
图5-7 Ⅰ型胶原的结构及其功能
胶原蛋白病也称为结缔组织遗传病(heritable disorders of connective tissue),主要包括成骨不全和Ehlers-Danlos综合征。
1.成骨不全 成骨不全(osteogenesis imperfecta,OMIM#166200)是一组因Ⅰ型胶原异常而引起的遗传异质性疾病,患者表现为骨质疏松、易骨折并伴有骨骼畸形等症状。该病的患病率约为1/15 000,是最常见的一种常染色体显性遗传病。成骨不全有多种类型,较常见的是Ⅰ型和Ⅱ型成骨不全(表5-2)。
表5-2 成骨不全的遗传与临床特征
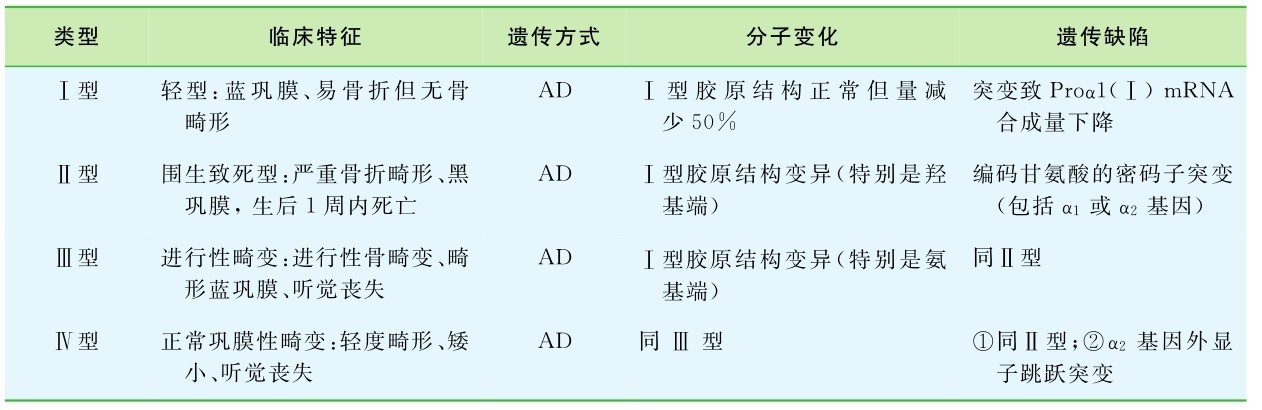
Ⅰ型成骨不全又称为蓝色巩膜综合征,病变累及骨骼、肌腱、韧带、筋膜、牙本质及巩膜等。主要临床表现为:患者骨质疏松致脆性增加而易反复发生骨折,巩膜呈蓝色;关节可过度活动而易于受伤并导致肢体畸形;牙齿生长不齐、畸形;伴传导性耳聋。多在青春期后发病。该病重症者身材矮小,X线显示多发生骨痂。Ⅰ型成骨不全基因定位于17q21.3-q22和7q 22.1,病因为胶原基因各种点突变导致的胶原成熟缺陷。例如,α1链胶原基因COL1A1,即胶原蛋白第178位氨基酸残基第1个碱基发生G→T的单碱基替换,导致甘氨酸被半胱氨酸替代。
Ⅱ型成骨不全又称先天性致死性成骨不全,其临床症状比Ⅰ型成骨不全严重得多,表现为:长骨短宽,宫内即可因骨质疏松、发脆而引起四肢、肋骨多发性骨折;蓝色巩膜;耳硬化性聋;身材矮小。患儿一般为死胎或生后早期死亡。存活者伴有进行性脑积水和长骨囊性变。Ⅱ型成骨不全的胶原基因突变比Ⅰ型更复杂、多见,主要涉及α1链胶原基因COL1A1和α2链胶原基因COL1A2上的甘氨酸密码子点突变或重排。例如,COL1A1即α1链94位上的甘氨酸被半胱氨酸替代,导致了Ⅱ型成骨不全表型;COL1A1 INS NT4088是在一个围生期致死型成骨不全患儿中发现的一个COL1A1 4088核苷酸5′端插入突变。
2.Ehlers-Danlos综合征 Ehlers-Danlos综合征(Ehlers-Danlos syndrome,EDS)包括各种临床亚型(EDSⅠ~EDSⅨ等),有的为常染色体显性遗传,有的为常染色体隐性遗传,患病率约为1/5 000,其中EDSⅣ型病情最为严重。典型的EDS综合征表现为皮肤可过度伸展,柔软脆弱易碎;皮肤受伤后愈合差,形成特殊的“香烟纸”疤;关节亦可过度伸展,导致髋、肩、肘、膝或锁骨关节易于脱位和受伤。
Ⅰ型Ehlers-Danlos综合征的分子病因可能是编码Ⅴ型胶原纤维α1链的基因COL5A1、COL5A2发生了突变;而其他类型的EDS的突变基因,Ⅳ型EDS:COL3A1;Ⅵ型EDS:赖氨酰羟化酶;Ⅶa及Ⅶb型EDS:COL1A1和COL1A2;Ⅶc型EDS:前胶原N-肽酶。
(二)肌营养不良症
较常见的肌营养不良症有Duchenne型肌营养不良症(Duchenne muscular dystrophy, DMD)、Becker型肌营养不良症(BMD)。DMD为X连锁隐性遗传,因此患者都为男性,群体研究显示平均每3 300个男婴中就有1例DMD患者,其中1/3为新突变。该病起病年龄为3~5岁,初始症状表现为爬楼梯困难,特殊的爬、起、站、立姿势;12岁左右时已无法行走;一般于20岁左右死于呼吸衰竭和心力衰竭。
DMD基因定位于Xp21.2,长约2 300kb,包含70多个外显子,编码1条相对分子质量为400 000的多肽链,称为dystrophin。Dystrophin主要分布于骨骼肌和心肌细胞中,对维持肌细胞膜结构的完整性起着非常重要的作用。DMD的发生多为缺失突变,缺失主要发生于DMD基因的5′端或中央区域,导致dystrophin无法合成。
BMD症状较DMD轻,患者可活过生育期,从而将致病基因传给子代。BMD和DMD属于同一种基因的同一类型的突变,但因其缺失的范围比较小,肌细胞内尚能合成一定量的dystrophin。
四、受体蛋白病
受体是指位于细胞膜、细胞质或细胞核内的一类具有特殊功能的蛋白质,由于这类蛋白质的遗传性缺陷导致的疾病称为受体病(receptor disease)。20世纪70年代,Goldstein和Brown曾对家族性高胆固醇血症(familiar hypercholesterolemia)患者细胞膜上低密度脂蛋白(low density lipoprotein,LDL)受体做了深入的研究。
家族性高胆固醇血症为遗传性高脂蛋白血症中的一个类型,遗传性高脂蛋白血症患者血浆中的胆固醇和三酰甘油(甘油三酯)增高,从而导致冠心病、心肌梗死等心血管疾病。家族性高胆固醇血症是由于细胞膜上的LDL受体缺陷而致病。在正常情况下,LDL与细胞膜上的LDL受体结合,通过内吞作用进入细胞,被溶酶体吞噬,为溶酶体酸性水解酶水解,释放出游离胆固醇。游离胆固醇在细胞内可激活脂酰辅酶A,将游离胆固醇脂化;游离胆固醇同时可抑制细胞内的β-羟基-β-甲基戊二酰辅酶A还原酶,从而减少细胞内胆固醇的合成。该病患者由于LDL受体缺陷,致使血浆中的LDL不能进入细胞,并使细胞内胆固醇的反馈抑制解除,使细胞内胆固醇合成增加并进入血浆,加重血浆中胆固醇的堆积(图5-8)。
该病为常染色体显性遗传,LDL受体基因定位于19p13.1-p13.2。LDL受体基因突变包括碱基替换、插入、缺失等,其中以碱基缺失较多见。
该病患者在青年期即患冠心病,出现心绞痛、心肌梗死等症状,并可能因此猝死。同时患者可因胆固醇堆积而出现黄瘤,较早出现角膜弓(俗称老人环)。该病患者多为杂合子,患者LDL受体为正常人的40%,血浆总胆固醇为7.8~10.3mmol/L(300~400mg/dl)。如患者为纯合子,其LDL受体只有正常人的10%,血浆总胆固醇为5.5~31.0μmol/L(600~1 200mg/dl),患者在儿童期即可出现症状。
五、膜转运蛋白病
由于膜转运蛋白的遗传缺陷导致的疾病称为膜转运蛋白病,如胱氨酸尿症、囊性纤维样变及先天性葡萄糖、半乳糖吸收不良症等。
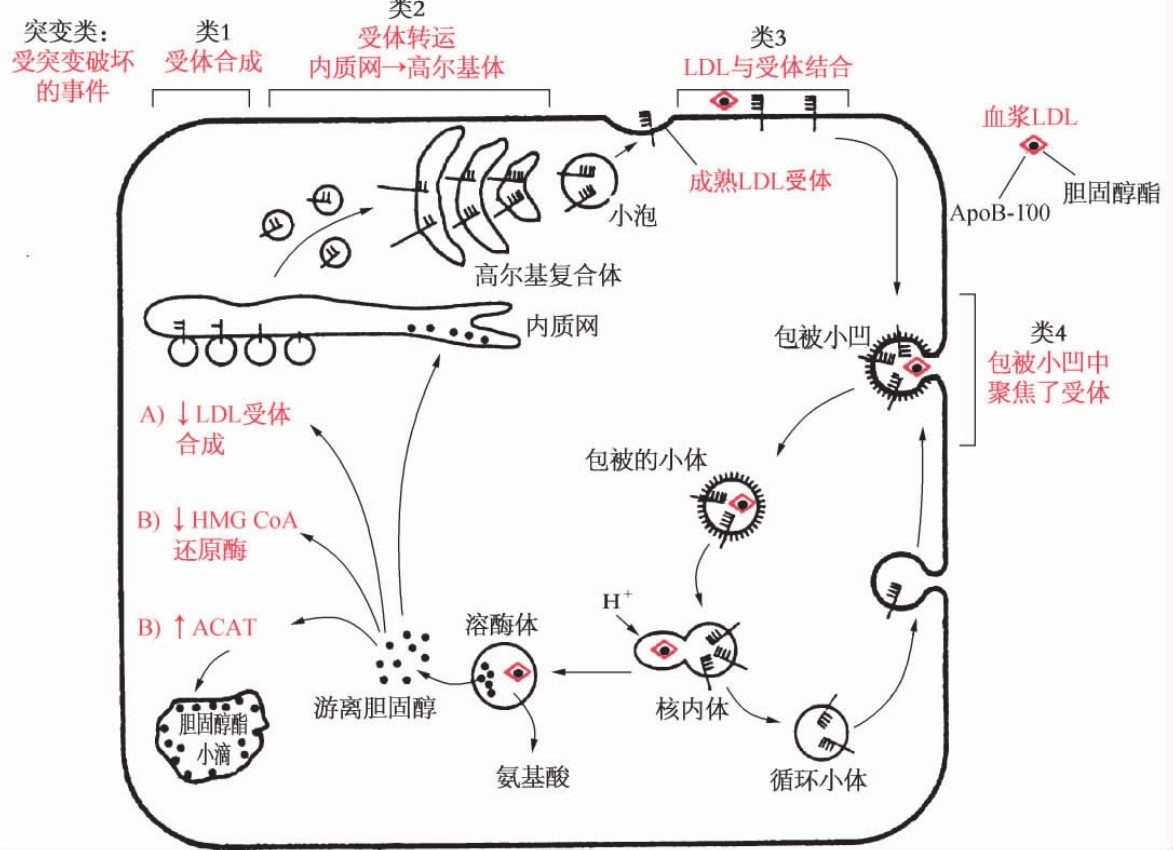
图5-8 LDL受体的细胞生物学功能
(一)胱氨酸尿症
胱氨酸尿症(cystinuria)患者的肾小管及小肠黏膜上皮细胞的膜转运蛋白缺陷,使肾小管对胱氨酸、赖氨酸、精氨酸和鸟氨酸的重吸收障碍。患者血浆中这4种氨基酸的含量偏低,而尿液中的含量增高,导致尿路结石发生,引起尿路感染和绞痛等症状。
该病可分为3个亚型,Ⅰ型为常染色体隐性遗传,患者对4种氨基酸均不能吸收;Ⅱ型和Ⅲ型均为常染色体不完全隐性遗传,Ⅲ型的症状较轻。
(二)先天性葡萄糖、半乳糖吸收不良症
先天性葡萄糖、半乳糖吸收不良症(congenital glucose-galactose malabsorption)为常染色体隐性遗传病。患者小肠上皮细胞转运葡萄糖、半乳糖的膜载体蛋白异常,致使葡萄糖和半乳糖吸收障碍,肠道内渗透压改变而使肠液增加,出现水样腹泻,腹泻的发生和程度与糖的进食时间及量有关,进食24小时后即可出现腹泻。婴儿喂食含葡萄糖和半乳糖的食物后随着腹泻加重继而出现脱水、营养不良等症状,但该病随着年龄增加,对葡萄糖和半乳糖的耐受性也会增加。









