-
1.1内容提要
-
1.2序
-
1.3前 言
-
1.4上 篇
-
1.4.1第1章 膝关节应用解剖
-
1.4.1.1第一节 膝部表面解剖
-
1.4.1.1.1一、膝前面表面解剖
-
1.4.1.1.2二、膝后面表面解剖
-
1.4.1.2第二节 构成膝关节的骨骼
-
1.4.1.2.1一、股骨下端
-
1.4.1.2.2二、胫骨上端
-
1.4.1.2.3三、髌 骨
-
1.4.1.3第三节 维持膝关节稳定的组织
-
1.4.1.3.1一、韧 带
-
1.4.1.3.2二、关节囊
-
1.4.1.3.3三、半月板
-
1.4.1.3.4四、肌肉及肌腱
-
1.4.1.4第四节 膝关节的润滑及散热组织
-
1.4.1.4.1一、滑 膜
-
1.4.1.4.2二、滑膜囊
-
1.4.1.4.3三、滑膜皱襞
-
1.4.1.4.4四、髌下脂肪垫
-
1.4.1.5第五节 膝部的神经支配
-
1.4.1.5.1一、膝部皮神经的来源与分布
-
1.4.1.5.2二、膝关节支神经的来源与分布
-
1.4.1.6第六节 膝关节的运动力学
-
1.4.1.6.1一、股胫关节的运动
-
1.4.1.6.2二、髌股关节的运动
-
1.4.1.6.3三、作用于膝关节的力
-
1.4.1.6.4四、下肢的力线
-
1.4.2第2章 膝关节骨关节炎的病因病理
-
1.4.2.1第一节 膝关节骨关节炎的流行病学
-
1.4.2.1.1一、发病率与流行情况
-
1.4.2.1.2二、发病的危险因素
-
1.4.2.2第二节 膝关节骨关节炎的病理
-
1.4.2.2.1一、关节软骨变化
-
1.4.2.2.2二、软骨下骨质改变
-
1.4.2.2.3三、滑膜病变
-
1.4.2.2.4四、肌肉的改变
-
1.4.2.2.5五、细胞因子在骨关节炎发病中的作用
-
1.4.2.2.6六、骨关节炎膝痛的发生机制
-
1.4.2.2.7七、膝关节骨关节炎患者的运动功能障碍及其相关因素
-
1.4.2.2.8八、骨关节炎患者膝关节本体感觉的改变
-
1.4.2.3第三节 膝关节骨关节炎中医病证理论
-
1.4.2.3.1一、膝关节骨关节炎的中医病名探讨
-
1.4.2.3.2二、膝关节骨关节炎的中医病因病机
-
1.4.2.3.3三、膝关节骨关节炎的中医基本病理环节
-
1.4.2.3.4四、筋骨萎痹是膝关节骨关节炎最终的病理改变
-
1.4.3第3章 膝关节骨关节炎的临床表现和检查
-
1.4.3.1第一节 病史询问
-
1.4.3.1.1一、发病情况
-
1.4.3.1.2二、临床表现
-
1.4.3.1.3三、既往治疗史
-
1.4.3.1.4四、既往疾病史
-
1.4.3.1.5五、过敏史
-
1.4.3.2第二节 症状与体征
-
1.4.3.2.1一、常见症状
-
1.4.3.2.2二、心理障碍
-
1.4.3.2.3三、临床体征
-
1.4.3.3第三节 体格检查方法
-
1.4.3.3.1一、膝部外观检查
-
1.4.3.3.2二、特殊体格检查方法
-
1.4.3.3.3三、膝关节本体感觉的测定
-
1.4.3.4第四节 实验室检查
-
1.4.3.4.1一、血液检查
-
1.4.3.4.2二、滑液检查
-
1.4.3.4.3三、生物标记物检查
-
1.4.3.5第五节 影像学检查
-
1.4.3.5.1一、X线平片
-
1.4.3.5.2二、X线断层扫描
-
1.4.3.5.3三、磁共振成像检查
-
1.4.3.5.4四、超声检查
-
1.4.3.5.5五、关节镜检查
-
1.4.4第4章 膝关节骨关节炎的诊断与鉴别诊断
-
1.4.4.1第一节 诊断标准与诊断思维
-
1.4.4.1.1一、诊断标准
-
1.4.4.1.2二、诊断思维
-
1.4.4.2第二节 鉴别诊断
-
1.4.4.2.1一、痛风性关节炎
-
1.4.4.2.2二、焦磷酸钙沉积病
-
1.4.4.2.3三、色素绒毛结节性滑膜炎
-
1.4.4.2.4四、强直性脊柱炎
-
1.4.4.2.5五、髌骨软化症
-
1.4.4.2.6六、滑膜皱襞综合征
-
1.4.4.2.7七、脂肪垫炎
-
1.4.5第5章 膝关节骨关节炎中医证候诊断
-
1.4.5.1第一节“证”有关概念
-
1.4.5.1.1一、病、证、证素、证名的概念
-
1.4.5.1.2二、辨证的概念及其原理
-
1.4.5.2第二节 膝关节骨关节炎辨证诊断方法
-
1.4.5.2.1一、临床资料的采集
-
1.4.5.2.2二、辨证思维过程
-
1.4.5.3第三节 膝关节骨关节炎的基本证型
-
1.4.5.3.1一、文献资料回顾小结
-
1.4.5.3.2二、膝关节骨关节炎的基本证型
-
1.4.5.4第四节 膝关节骨关节炎中医证候相关性分析
-
1.4.5.4.1一、中医证候分型与X线影像的关系
-
1.4.5.4.2二、中医证型与炎症介质的相关性
-
1.4.5.4.3三、中医证型与滑液中蛋白多糖和透明质酸含量的相关性
-
1.4.5.4.4四、中医证型与MRI影像的相关性
-
1.4.5.4.5五、中医辨证分型与膝关节镜下病理改变对比性研究
-
1.4.5.4.6六、不同中医证型患者血清中标志蛋白探讨
-
1.4.6第6章 膝关节骨关节炎的病情评估
-
1.4.6.1第一节 膝部疼痛的评估
-
1.4.6.1.1一、视觉模拟评分
-
1.4.6.1.2二、数字评价量表
-
1.4.6.1.3三、语言描述量表
-
1.4.6.1.4四、面部疼痛表情量表
-
1.4.6.1.5五、疼痛问卷表
-
1.4.6.2第二节 肌力的测量
-
1.4.6.3第三节 X线影像的分级诊断
-
1.4.6.3.1一、Kellgren和Lawrence的放射学诊断分级标准
-
1.4.6.3.2二、Appel放射学诊断分级标准
-
1.4.6.3.3三、Altman放射学诊断分级标准
-
1.4.6.3.4四、Holden放射学诊断分级标准
-
1.4.6.3.5五、腰野富久放射学诊断分级标准
-
1.4.6.4第四节 膝关节骨关节炎病情评分系统
-
1.4.6.4.1一、Lequesne膝关节骨关节炎严重程度指数
-
1.4.6.4.2二、改良的日本骨科协会膝关节评分法
-
1.4.6.4.3三、Lysholm膝关节评分标准
-
1.4.6.4.4四、美国膝关节学会评分标准
-
1.4.6.4.5五、辛辛那提膝关节评分系统
-
1.4.6.4.6六、Irrgang膝关节日常活动能力评价系统
-
1.4.6.4.7七、WOMAC骨关节炎指数
-
1.4.6.5第五节 生存质量评价
-
1.5下 篇
-
1.5.1第7章 中西医结合诊疗膝关节骨关节炎的思路与方法
-
1.5.1.1第一节 中西医结合诊疗膝关节骨关节炎的切入点
-
1.5.1.1.1一、诊断方面的切入点
-
1.5.1.1.2二、治疗方面的切入点
-
1.5.1.2第二节 中西医结合治疗膝关节骨关节炎的原则
-
1.5.1.2.1一、防治并重
-
1.5.1.2.2二、筋骨同治
-
1.5.1.2.3三、动静相宜
-
1.5.1.2.4四、内外兼治
-
1.5.1.2.5五、医患合作
-
1.5.1.3第三节 膝关节骨关节炎中西医结合治疗的论治途径
-
1.5.1.3.1一、从脏腑论治
-
1.5.1.3.2二、从气血论治
-
1.5.1.3.3三、从邪浊论治
-
1.5.1.3.4四、从筋骨论治
-
1.5.1.4第四节 中西医结合治疗膝关节骨关节炎的误区
-
1.5.2第8章 膝关节骨关节炎的非药物治疗
-
1.5.2.1第一节 健康教育
-
1.5.2.1.1一、健康教育的方式
-
1.5.2.1.2二、健康教育的内容
-
1.5.2.2第二节 社会支持
-
1.5.2.2.1一、社会支持的概念
-
1.5.2.2.2二、膝关节骨关节炎的社会支持
-
1.5.2.3第三节 保护性支具
-
1.5.2.3.1一、手 杖
-
1.5.2.3.2二、护 膝
-
1.5.2.3.3三、步行器
-
1.5.2.3.4四、矫形支具或矫形鞋
-
1.5.2.4第四节 控制体重
-
1.5.2.4.1一、体质指数与体重超重
-
1.5.2.4.2二、控制体重的措施
-
1.5.2.5第五节 物理疗法
-
1.5.2.5.1一、热疗的分类
-
1.5.2.5.2二、常用的热疗方法
-
1.5.2.6第六节 膝关节本体感觉康复重建
-
1.5.2.6.1一、健康教育
-
1.5.2.6.2二、关节护具的使用
-
1.5.2.6.3三、肌力训练
-
1.5.2.6.4四、本体感觉训练
-
1.5.2.6.5五、其他训练方法
-
1.5.3第9章 膝关节骨关节炎的药物治疗
-
1.5.3.1第一节 症状改善药物
-
1.5.3.1.1一、单纯性镇痛药
-
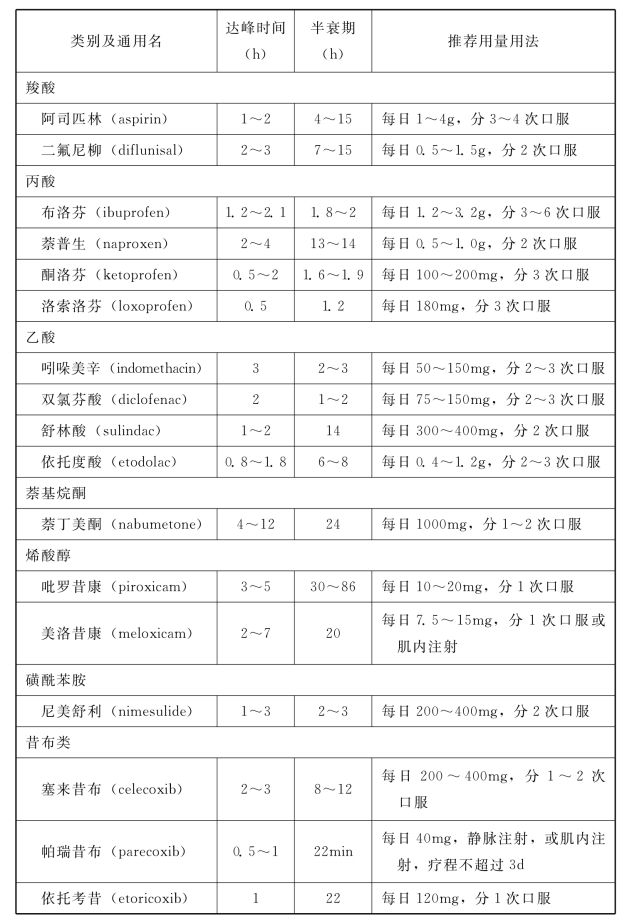
1.5.3.1.2二、非甾体消炎药
-
1.5.3.1.3三、糖皮质激素
-
1.5.3.2第二节 改善病情的药物
-
1.5.3.2.1一、氨基葡萄糖
-
1.5.3.2.2二、双醋瑞因
-
1.5.3.2.3三、硫酸软骨素
-
1.5.3.2.4四、四环素类抗生素
-
1.5.3.2.5五、植物药及其提取物
-
1.5.3.2.6六、基因疗法
-
1.5.3.2.7七、骨代谢改善药物
-
1.5.4第10章 膝关节骨关节炎的中药治疗
-
1.5.4.1第一节 中药治疗的处方用药方式
-
1.5.4.1.1一、方证相对,辨证用药
-
1.5.4.1.2二、辨病分期,序贯用药
-
1.5.4.1.3三、专病专方,随证加减
-
1.5.4.2第二节 中药治疗的常用治法
-
1.5.4.2.1一、内治用药的治法
-
1.5.4.2.2二、外治用药的治法
-
1.5.4.3第三节 常用类别中药的配伍方法
-
1.5.4.3.1一、祛风湿药的配伍
-
1.5.4.3.2二、活血化瘀药的配伍
-
1.5.4.3.3三、补虚药的配伍
-
1.5.4.4第四节 中药治疗常用给药途径和方法
-
1.5.4.4.1一、中药治疗的给药途径
-
1.5.4.4.2二、中药治疗的应用形式
-
1.5.5第11章 膝关节骨关节炎的常用中药与方剂
-
1.5.5.1第一节 治疗骨关节炎常用的中药
-
1.5.5.1.1一、文献资料回顾总结
-
1.5.5.1.2二、治疗膝关节骨关节炎的常用中药
-
1.5.5.2第二节 治疗骨关节炎常用的药对(组)
-
1.5.5.2.1一、药对的组成原则
-
1.5.5.2.2二、治疗骨关节炎常用的药对(组)
-
1.5.5.3第三节 治疗骨关节炎古今名方介绍
-
1.5.5.3.1一、内服方剂
-
1.5.5.3.2二、外用方剂
-
1.5.6第12章 膝关节骨关节炎的注射疗法
-
1.5.6.1第一节 膝关节腔内注射疗法
-
1.5.6.1.1一、关节腔穿刺注射技术
-
1.5.6.1.2二、糖皮质激素关节腔内注射
-
1.5.6.1.3三、透明质酸钠的关节内注射
-
1.5.6.2第二节 膝关节腔外注射疗法
-
1.5.6.2.1一、局部封闭注射
-
1.5.6.2.2二、穴位注射
-
1.5.7第13章 膝关节骨关节炎的针灸疗法
-
1.5.7.1第一节 毫针疗法
-
1.5.7.1.1一、穴位的选择
-
1.5.7.1.2二、常用腧穴的定位及其应用解剖
-
1.5.7.1.3三、针刺方法
-
1.5.7.1.4四、针刺的注意事项
-
1.5.7.2第二节 灸疗法
-
1.5.7.2.1一、艾炷灸
-
1.5.7.2.2二、艾条灸
-
1.5.7.2.3三、灸疗的注意事项
-
1.5.7.3第三节 腹针疗法
-
1.5.7.3.1一、穴位的选取
-
1.5.7.3.2二、腹针刺法
-
1.5.7.3.3三、腹针疗法的治疗效果
-
1.5.7.4第四节 穴位埋线疗法
-
1.5.7.4.1一、穴位的选择
-
1.5.7.4.2二、治疗器具
-
1.5.7.4.3三、埋线方法
-
1.5.7.4.4四、埋线疗法的注意事项
-
1.5.7.5第五节 穴位贴敷疗法
-
1.5.7.5.1一、药物的选择
-
1.5.7.5.2二、穴位的选择
-
1.5.7.5.3三、贴敷方法
-
1.5.7.5.4四、穴位贴敷的注意事项
-
1.5.7.6第六节 刺络疗法
-
1.5.7.6.1一、针具的选择
-
1.5.7.6.2二、刺络部位
-
1.5.7.6.3三、刺络方法
-
1.5.7.6.4四、刺络疗法的注意事项
-
1.5.7.7第七节 针刀疗法
-
1.5.7.7.1一、针刀治疗膝关节骨关节炎可能的作用机制
-
1.5.7.7.2二、针刀治疗方法
-
1.5.7.7.3三、针刀疗法的注意事项
-
1.5.8第14章 膝关节骨关节炎的推拿疗法
-
1.5.8.1第一节 推拿的基本手法
-
1.5.8.1.1一、按 法
-
1.5.8.1.2二、摩 法
-
1.5.8.1.3三、推 法
-
1.5.8.1.4四、拿 法
-
1.5.8.1.5五、<img title="pagenumber_ebook=279,pagenumber_book...
-
1.5.8.1.6六、揉 法
-
1.5.8.1.7七、捋 法
-
1.5.8.1.8八、搓 法
-
1.5.8.1.9九、点穴法
-
1.5.8.1.10十、击打法
-
1.5.8.1.11十一、扳 法
-
1.5.8.1.12十二、抖 法
-
1.5.8.1.13十三、伸屈法
-
1.5.8.1.14十四、旋转法
-
1.5.8.2第二节 膝关节骨关节炎常用的推拿手法
-
1.5.8.2.1一、肌筋放松手法
-
1.5.8.2.2二、解痛手法
-
1.5.8.2.3三、解除膝关节交锁手法
-
1.5.8.2.4四、关节被动运动手法
-
1.5.8.3第三节 关节松动技术
-
1.5.8.3.1一、关节松动技术的基本概念
-
1.5.8.3.2二、膝关节骨关节炎的松动技术
-
1.5.9第15章 膝关节骨关节炎的运动疗法
-
1.5.9.1第一节 肌力训练
-
1.5.9.1.1一、肌力训练的分类
-
1.5.9.1.2二、肌肉训练方法
-
1.5.9.1.3三、肌力训练的注意事项
-
1.5.9.2第二节 关节活动范围训练
-
1.5.9.2.1一、关节活动范围减小的原因
-
1.5.9.2.2二、增加活动范围训练方法
-
1.5.9.3第三节 有氧运动
-
1.5.9.3.1一、有氧运动的特点
-
1.5.9.3.2二、有氧运动的作用
-
1.5.9.3.3三、有氧运动的处方原则
-
1.5.9.3.4四、膝关节骨关节炎常用的有氧运动
-
1.5.10第16章 名医名家经验选萃
-
1.5.10.1第一节 古代医家医论
-
1.5.10.1.1一、与膝关节骨关节炎相近似的中医病名
-
1.5.10.1.2二、膝关节骨关节炎类似病的病因病机
-
1.5.10.1.3三、膝关节骨关节炎类似病的治则
-
1.5.10.1.4四、膝关节骨关节炎类似病的治法
-
1.5.10.2第二节 现代医家经验
-
1.5.10.2.1一、用药经验
-
1.5.10.2.2二、手法经验
-
1.5.10.2.3三、针灸经验
-
1.5.10.3第三节 其他民族医学疗法
-
1.5.10.3.1一、膝关节骨关节炎的维吾尔医诊疗
-
1.5.10.3.2二、骨关节炎的傣医外治疗法
-
1.5.10.3.3三、膝关节骨关节炎的苗医药诊疗
-
1.5.11参考文献
1
中西医结合治疗膝关节骨关节炎