10.2 风险评估
风险评估的过程可以分为4个明显不同的阶段:危害识别、危害描述、暴露评估和风险描述。危害识别采用的是定性方法,其余三步可以采用定性方法,但最好采用定量方法。相对于微生物危害而言,这一方法更适用于化学危害,这主要由于微生物是活体,处于不断动态条件下,进入食品链后受到诸多因素的影响,微生物病原菌可以繁殖,也可以死亡,其生物学相互作用很复杂,对微生物危害来说,这一方法仍停留在概念应用阶段,有待进一步发展,而化学危害进入食品链后发生变化较微生物变化较小。因此,本节主要阐述化学物质风险评估理论。
10.2.1 危害识别
危害识别又称危害确定或危害鉴定,是对可能在食品或食品系列中存在的,能够对健康产生副作用的生物、化学和物理的致病因子进行鉴定。危害识别的目的在于确定人体摄入污染物的潜在不良效应,对这种不良效应进行分类和分级。对于化学因素(包括食品添加剂、农药和兽药残留、有机污染物和天然毒素),可采取流行病学研究、动物试验、体外试验、结构-活性关系等方式,也可采用“证据力”方法采用已证实的科学结论来获取危害程度的依据。一般对于该步骤而言,很多比较成熟的结论可以直接参考或进行相互借鉴。
(1)流行病研究 流行病学研究如果能够从临床和流行病学研究上获得数据,在危害识别和其他步骤中也应当充分利用。但对于大多数化学物质来说,临床和流行病学资料难以得到。如果流行病学研究数据能够获得阳性结果,则需要将其应用到风险评估中。在设计流行病学研究时,或分析具有阳性结果的流行病学资料时,应当充分考虑个体易感性,包括遗传易感性、与年龄和性别相关的易感性以及营养状况与经济状况等。同时,风险评估的流行病学研究必须采用公认的标准程序进行。此外,由于大部分流行病学研究的统计学效率不足以发现低水平暴露的效应,阴性结果在危险性评估中难以得到肯定答案。即使流行病学资料的价值最大,风险管理决策也不可过分依赖流行病学研究。
(2)动物试验 动物试验用于风险评估的绝大多数毒理学数据来自动物试验,这就要求这些试验必须遵循标准化试验程序。国际经济合作与发展组织(OECD)和美国环境保护局(EPA)曾经制定了化学品的危险性评价程序,我国也以国家标准形式制定了《食品安全性毒理学评价程序和方法》。无论采用什么程序,所有试验均应按良好实验室规范(CLP)和标准化的质量保证/质量控制方案实施。
长期动物试验数据至关重要,主要针对的毒理学效应终点包括致癌性、生殖/发育毒性、神经毒性、免疫毒性等。短期毒理学试验资料也是有用的,如急性毒性的分级是以LD50数值的大小为依据的。这些动物毒理学试验的设计可以找出观察到有害作用的最低剂量(LOAEL)、未观察到有害作用剂量(NOAEL)。在试验中选择较高剂量可以尽可能减少假阴性的产生。动物试验还可以提供作用机制、染毒剂量、剂量-效应关系以及毒物代谢动力学和毒效学等研究资料,确定化学物对人健康可能引起的潜在不良效应。而作用机制的资料可以用体外试验补充,如遗传毒性试验,增加对毒作用机制和毒物代谢动力学和毒效学的了解。
(3)体外试验 体外试验相对于体内试验,体外试验可作为作用机制的补充资料,例如遗传毒性试验。这些试验必须遵循良好实验室规范(CLP)或其他广泛接受的程序。但是,体外试验的数据不能作为预测对人体危害的唯一资料来源。体内和体外试验的结果可以促进对作用机制和药物代谢动力学/药效学的认识,但在许多情况下无取得这些资料,因而风险评估进程不应因等待作用机制和药物代谢动力学或药效学资料而延误。给药量和药物作用计量的资料有助于评价作用机制和药物代谢动力学数据,评估时尚需考虑化学物特性(给予剂量)和代谢物毒性(作用剂量)。
(4)结构-活性关系 结构-活性关系对于识别人类健康危害的加权分析有用。在对一类化学物进行评价时,此类化学物的一种或多种物质有足够的毒理学资料,可采用毒物浓度的方法并通过对该类化学物中的一种物质的认识来推导该类化学物中另外物质对人类摄入后的健康危害,如DDT有机氯农药。一般化学物结构-活性关系是一个定量关系,即定量结构-活性关系,主要反映其化学结构与其对生态或生物体效应的因果关系和量变规律。化学物质包括其物理化学特性(如溶解性、熔点、沸点等)、立体化学特性(如原子质量、电子密度等)、量子化学特性(如分子容积、表面积等)。其危害性与其中的物理化学特性具有非常大的相关性,尤其是水溶性,根据—COOH、—CO、—OH、—NH2、—CN化学键,其毒性有增加的趋势。结构-活性关系对于暴露评估过程中了解化学物与度量终点之间关系效应非常重要。
10.2.2 危害描述
危害描述又称危害特征描述,是指定量、定性地评价由危害产生的对健康副作用的性质。对于化学性致病因子要进行剂量-反应评估,对于生物或物理因子在可以获得资料的情况下也应进行剂量-反应评估。危害描述重点在于这些不良反应的定量表述,核心是剂量-反应关系的评估,其主要内容是描述不良影响的严重性和持久性,在危害描述过程中,一定要明确被感染的主体,并尽可能测定感染的结果。危害描述一般包括不良影响的剂量-反应评估、易感人群的鉴定及其与普通人群的比较、分析不良影响的作用模式或机制的特性,以及不同物种间的推断,即由高到低的剂量-反应外推等4个步骤,具体采用以下5种方法进行危害描述。
(1)剂量-反应关系的外推 剂量一般取决于化学物质摄入量(即浓度、进食量与接触时间的乘积),效应是指最敏感和关键的不良健康状况的变化。所谓剂量-反应关系的评估就是确定化学物的摄入量与不良健康效应的强度与频率,包括剂量-效应关系和剂量-反应关系。剂量-效应关系是指不同剂量的外源性化学物与其在个体或群体中所表现的量效应大小的关系;剂量-反应关系则指不同剂量的外源性化学物与其在群体中所引起的质效应发生率之间的关系。为了与人体摄入量水平相比较,需要把动物试验数据外推到比动物试验低得多的剂量,也就是在所研究的剂量-反应关系的评估曲线之外。但这种外推过程在质和量上皆存在不确定性。危害的性质也许会随剂量的改变而改变或完全消失。如果动物与人体的反应在本质上不一致,则所选的剂量-反应模型可能有误。即使在同一个剂量,人与动物在毒物代谢动力学上也可能存在不同;如果剂量不同,代谢方式存在不同的可能性更大,如高剂量化学物会使其正常解毒(代谢)途径饱和,而在低剂量时不会产生毒害作用。因此,在将高剂量的不良效应外推到低剂量时,这些与剂量有关的变化所造成的潜在影响就成为毒理学家关注的焦点。
(2)剂量的度量 动物与人体的毒理学剂量是否相同是另一个有争议的问题。一般使用每千克体重的毫克数作为种属间的度量。近年来,美国提出度量单位每千克体重的毫克数应该乘以3/4的系数。检测人体和动物靶器官中的组织浓度和消除速率可以取得理想的度量系数(如在二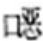 英中就考虑体脂含量和消除速率),血中化学物的水平也接近这种理想方法。在无法获得充分证据时,常规使用种属间的通用系数可以作为主要依据。
英中就考虑体脂含量和消除速率),血中化学物的水平也接近这种理想方法。在无法获得充分证据时,常规使用种属间的通用系数可以作为主要依据。
(3)遗传毒性与非遗传毒性致癌物 毒理学家对化学物的不良健康效应存在阈值的认识比较一致,但遗传毒性致癌物例外。由少数几个分子甚至一个分子的突变就有可能诱发人体或动物的癌症,根据这一致癌理论,致癌物就没有安全剂量。
近年来,对待不同种类的致癌物已有所区别,并确定了一类非遗传毒性致癌物,即本身不诱发突变、但可作用于其他致癌物或某些物理化学因素启动的细胞致癌中的后期过程。相反,大部分致癌物通过诱发体细胞基因突变而活化致癌基因和(或)灭活抑癌基因,因此可以将遗传毒性致癌物定义为能直接或间接地引起靶细胞遗传改变的化学物。遗传毒性致癌物的主要作用靶点是遗传物质,而非遗传毒性致癌物作用于非遗传位点,主要是促进靶细胞增殖和(或)持续性的靶点功能亢进或衰竭。毒理学家和遗传学家已建立了一套致突变试验,这是采用体内和体外试验(如Ames试验)相结合的一组试验。尽管每一方法本身都存在局限性,但在区分致癌物属于遗传毒性与非遗传毒性上还是有用的。
许多国家的食品安全管理机构认定遗传毒性与非遗传毒性致癌物存在不同,即某些非遗传毒性致癌物存在剂量阈值,而遗传毒性致癌物不存在剂量阈值。由于目前对致癌机制的认识不足,致突变性试验筛选致癌物的方法尚不能应用于所有致癌物。原则上,非遗传毒性致癌物可以按阈值方法进行管理,如可观察的无作用剂量水平——安全系数法。在证明某一种物质属于非遗传毒性致癌物之外,往往需要提供致癌机制的科学资料。
(4)阈值法 由动物毒理学试验获得的LOAEL或NOAEL值除以合适的安全系数就得到安全阈值水平,即每日允许摄入量(acceptahle daily intake,ADI)。ADI值提供的信息是:如果按其ADI值或低于ADI的量摄入某一种化学物,则对健康没有明显的风险。这是由于假定该化学物对人体与试验动物的有害作用存在着合理的阈剂量值。但试验动物与人体存在种属差别,其敏感性和遗传特性也存在差异,并且膳食习惯也不同,鉴于此,安全系数可以克服此类不确定性,弥补人群中的个体差异。通常对动物长期毒性试验资料的安全系数为100。当然,理论上存在某些个体的敏感性程度超出安全系数的范围。因此,当一个化学物的科学数据有限时,原则上采用更大的安全系数,如200倍。此外,有些国家的卫生机构按效应的强度和可逆性来调整ADI。即使如此,采用安全系数并不能够保证每个个体的绝对安全。因此,对于特殊人群如儿童、老人,可以在考虑他们摄入水平的基础上,采用一个特殊的转换系数进行保护。
(5)非阈值法 对于遗传毒性致癌物,一般不采用NOAEL乘以安全系数的方法来制定允许摄入量,因为即使在最低剂量仍然存在致癌危险性,即一次受到致癌物的攻击造成遗传物质的突变就有可能致癌。致癌物零阈值的概念在现实管理中是难以实行的,而可接受风险的概念成为人们的共识。在遗传毒性致癌物的管理上存在2种办法:①禁止生产和使用某些化学物(如二溴乙烷农药、致癌性的食品添加剂等);②对化学物制定一种极低且可以忽略不计、对健康影响甚微或社会可以接受的风险水平,这一办法的实施就要求对致癌物进行定量风险评估。评估用的数据仍然来自高剂量动物试验,而高剂量时的剂量-反应关系可能与低剂量时剂量-反应关系完全不同。以数学模型对可接受风险的剂量水平进行推导,曾提出多种拟合度较高的外推模型。目前有6种常用的模型,其中最常用的线性多阶段模型,但对许多化学致癌物外推到人可能摄入的低剂量时的反应仍不是最适合的。目前的模型大多数是以统计学为基础,而不是以生物学为基础进行评估。也就是说,目前的模型仅利用试验性肿瘤的发生率与剂量,几乎没有其他生物学资料。没有一个模型能利用试验验证,也没有对高剂量的毒性、细胞增殖与促癌或DNA修复等作用进行修正。由此可以认为当前在实践中使用的线性模型是对危险性的保守性估计,用线性模型做出的风险特征描述一般以“合理的上限”或“最坏估计量”等字眼表述。许多管理机构已经认识到它们无法预测人群的接近真正的风险。非线性模型可以部分克服线性模型所固有的保守性,采用它的先决条件就是制定可接受的风险水平。选择可接受的危险性水平取决于每个国家危险性管理者的决策,美国FDA和EPA选用百万分之一(10-6)作为界限,这代表了科学界和管理者的共识。
10.2.3 暴露评估
暴露评估又称摄入量评估,是指定量、定性地评价由食品以及其他相关方式对生物的、化学的和物理的致病因子的可能摄入量。暴露评估主要根据膳食调查和各种食品中化学物质暴露水平调查的数据进行的。通过计算,可以得到人体对于该种化学物质的暴露量。人体与化学物的接触,显然发生于外部环境和机体的交换界面(如皮肤、肺和胃肠道)。暴露评估就是对人体对化学物接触进行定性和定量评估,包括暴露的强度、频率和时间,暴露途径(如经皮、经口和呼吸道),化学物摄入(intake)和摄取(uptake)速率,跨过界面的量和吸收剂量(内剂量),也就是测定某一化学物进入机体的途径、范围和速率,来估计人群与环境(水、土、气和食品)暴露化学物的浓度和剂量。
(1)摄入量的评估 对于食品添加剂、农药和兽药残留以及污染物的膳食摄入量的估计,需要有相应的食物消费量与这些食物中要评估的化学物浓度资料。食品添加剂、农药和兽药残留的膳食摄入量可根据规定的使用范围和使用量来估计。最简单的情况是,食品中某一添加剂含量保持恒定,原则上以最高使用量计算摄入量。但在许多情况下,食品中的量在食用前就发生了变化,如食品添加剂(如亚硝酸盐、抗坏血酸等)在食品储存过程中可能发生降解或与食品发生反应,农药残留在农产品原料加工过程中会降解或富积,食品中的兽药残留则受到动物体内代谢动力学、器官分布和停药期的影响。因此,食品中的实际水平可能远远低于最大允许使用量或残留量。因仅有部分农作物或家畜家禽使用农药和兽药,食品中有时甚至可以不含农药或兽药残留。食品添加剂的含量可以从制造商那里获得,而包括农药和兽药残留在内的食品污染物的摄入量则要通过敏感和可靠的分析方法对代表性食品进行分析获得。一般来说,膳食摄入量评估有3种方法:总膳食研究、单个食品的选择性研究和双膳食研究。总膳食研究将某一国家或地区的食物进行聚类,按当地菜谱进行烹调成为能够直接入口的样品,通过化学分析获得整个人群的膳食摄入量。单个食品的选择性研究,是针对某些特殊污染物在典型(或称为代表性)地区选择指示性食品(如猪肾中的镉、玉米和花生中的黄曲霉毒素等)进行研究。双膳食研究则对个体污染物摄入量的变异研究更加有效。WHO自1975年以来开展了全球环境监测系统/食品规划部分(GEMS/Food),制定了膳食中化学污染物和农药摄入量的研究准则。中国预防医学科学院营养与食品卫生研究所作为WHO食品污染物监测合作中心(中国),一直承担着GEMS/Food在中国的监测任务,进行中国总膳食研究和污染物监测,开展我国食品污染物国家卫生标准的制订工作。
根据测定的食品中化学物含量进行摄入量评估时,必须有可靠的食物消费量资料。评估化学物的摄入量时,不仅要求我国居民食物消费的平均数,而且应该有不同人群的食物消费资料,特别是敏感人群的资料。如在铅的评估中,婴幼儿十分重要,1992年的中国总膳食研究就包括了婴儿和2~8岁的食物消费量数据,并采用这些数据进行食品样品的制备与分析。我国目前膳食摄入量的数据主要来自膳食调查,但在制定国际性食品安全风险评估办法时应该注意膳食摄入量资料的可比性,特别是世界上不同主食消费情况。GEMS/Food已经建立了5个地区性(亚洲、非洲、东地中海、欧洲和拉美)的和全球性的膳食数据库,这是依据联合国粮食和农业组织(FAO)食物平衡表数据制定的。
膳食中食品添加剂、农药和兽药的摄入量必须低于相应的ADI值。通常实际摄入量远远低于ADI数值。因为对污染物确定ADI值存在困难,常采用暂定允许摄入量的办法。污染物的膳食摄入量偶然会比暂定允许摄入量高,如我国的总膳食研究表明,2~8岁儿童膳食铅的摄入量超过了铅的暂定允许摄入量的18%,这说明我国膳食铅已经可能对健康引起损害。
(2)暴露的生物标志物/内剂量和生物有效剂量的评估 可以采用生物监测来评估机体中化学物的内暴露量,这包括以下几点:①生物组织或体液(血液、尿液、呼出气、头发、脂肪组织等)中化学物及其代谢物的浓度,②人体由于暴露化学物导致的生物效应(如烷基化血红蛋白、酶诱导的改变等),③结合于靶分子中化学物及其代谢产物的量。生物标志物(biomarker)不仅整合了所有来源的环境暴露的信息,也反映了诸多因素(包括环境特征、生理处置的遗传学差别、年龄、性别、种族和/或生活方式等)。对于许多的环境污染物,在暴露和生物效应之间的生物学过程尚不清楚,生物标志物可以提供线索。因此,生物标志物就成为生物监测的关键,而在暴露水平和生物标志物之间建立包括毒物代谢动力学在内的相关性有利于生物标志物的选择。通过改进生物学标志物的灵敏度、特异性和对低剂量暴露的早期有害效应的可预测性,来保护易感人群。在过去十几年中,已经发展的生物标志物主要用来检测损伤DNA各种化学物和致癌物的暴露,包括体液中母体化合物及其代谢产物或DNA/蛋白质(如白蛋白和血花蛋白)加合物的接触指标,并发展了生物学效应标志物,如暴露个体的细胞遗传学改变。已建立生物标志物的有烟草和涉及膳食方面化学物如黄曲霉毒素、亚硝胺、多环芳烃、芳香胺和杂环胺等。在食品污染物的生物监测中,除了上面这些以DNA加合物为主要生物标志物外,还有一些采用了机体负荷水平,如有机氯农药六六六和滴滴涕、多氯联苯和二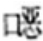 英等环境持久性污染物可以采用体脂中含量来评估。而有机磷农药等可以采用血液胆碱酯酶活性作为接触/效应性生物学标志物。镉可以损害肾小球的通透性和肾小管的重吸收而出现小分子蛋白尿,此也可以作为生物学标志物。
英等环境持久性污染物可以采用体脂中含量来评估。而有机磷农药等可以采用血液胆碱酯酶活性作为接触/效应性生物学标志物。镉可以损害肾小球的通透性和肾小管的重吸收而出现小分子蛋白尿,此也可以作为生物学标志物。
10.2.4 风险描述
风险描述是指在危害确定、危害特征描述和暴露评估的基础上,对给定人群中已知或潜在的副作用产生的可能性和副作用的严重性,作出定量或定性估价的过程,包括伴随的不确定性的描述。风险描述的结果是对人体摄入某化学物对健康产生不良效应的可能性进行估计,它是危害鉴定、危害描述和摄入量评估的综合结果。某一化学物如果存在阈值,则对人群风险可以采用摄入量与ADI相比较的百分数作为风险描述,如果所评价的化学物质的摄入量较ADI小,则对人的健康危害的可能性甚小,甚至为零。如1992年中国总膳食研究评估,我国膳食总的来说是安全的,但2~8岁儿童铅的摄入量超过暂定允许摄入量的18%,表明我国儿童已经处于铅污染的危害中,同时从大样本的儿童调查也发现血铅超过100μg/L的儿童在城市已经占40%,这也表明铅对我国儿童健康的潜在危害已经是不容忽视的问题。如果所评价的化学物没有阈值,对人群的风险是摄入量与危害强度的综合结果。
食品添加剂以及农药和兽药残留采用固定的风险水平是比较切合实际的,因为假如估计的风险超过了规定的可接受水平,就可以禁止这些化学物的使用。在描述危险性特征时,必须认识到在风险评估过程中每一步所涉及的不确定性。危险性特征描述中的不确定性反映了在前面三个阶段评估中的不确定性。将动物试验的结果外推到人时存在不确定性,例如喂养BHA的大鼠发生前胃肿瘤和阿斯巴甜引发小鼠神经毒性效应的结果可能不适用于人;而人体对化学物的某些高度易感性反应在动物中可能并不出现,如人对味精(谷氨酸钠)的不适反应。在实际工作中应该进行额外的人体试验研究以降低不确定性。
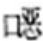 英中就考虑体脂含量和消除速率),血中化学物的水平也接近这种理想方法。在无法获得充分证据时,常规使用种属间的通用系数可以作为主要依据。
英中就考虑体脂含量和消除速率),血中化学物的水平也接近这种理想方法。在无法获得充分证据时,常规使用种属间的通用系数可以作为主要依据。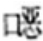 英等环境持久性污染物可以采用体脂中含量来评估。而有机磷农药等可以采用血液胆碱酯酶活性作为接触/效应性生物学标志物。镉可以损害肾小球的通透性和肾小管的重吸收而出现小分子蛋白尿,此也可以作为生物学标志物。
英等环境持久性污染物可以采用体脂中含量来评估。而有机磷农药等可以采用血液胆碱酯酶活性作为接触/效应性生物学标志物。镉可以损害肾小球的通透性和肾小管的重吸收而出现小分子蛋白尿,此也可以作为生物学标志物。