正常时,凝血系统一旦被激活,抗凝和纤溶系统也被相继激活,这样既可以有效止血,又可防止凝血的扩大化,保证血液的正常流动。
因此,当机体抗凝或纤溶系统功能异常时,可发生凝血与抗凝血平衡紊乱,产生出血或血栓形成倾向。
一、抗凝系统功能异常
抗凝系统功能异常,在临床上多表现为血栓形成倾向。
1. 抗凝血酶Ⅲ减少或缺乏
抗凝血酶Ⅲ(AT- Ⅲ)主要由肝脏和血管内皮细胞产生,可使FⅦa、FⅨa、FⅩa、FⅪa等灭活,其单独灭活速度慢,与肝素或血管内皮细胞上表达的硫酸乙酰肝素结合后,灭活速度增加约1000倍。
AT-Ⅲ 数量不足和(或)功能异常可影响抗凝作用导致血栓形成倾向。
(1)遗传性缺乏
AT-Ⅲ基因变异可导致AT-Ⅲ缺乏,引起反复性、家族性深部静脉血栓症。
(2)获得性缺乏
1)AT-Ⅲ 合成减少:
肠道消化吸收蛋白质功能障碍时,因底物不足使其合成减少;
肝功能严重障碍也可导致AT- Ⅲ合成减少。
此外,口服避孕药时,雌激素等成分可使AT- Ⅲ减少,因而也易导致静脉血栓形成。
2)AT-Ⅲ 丢失或消耗增多:
肾病综合征患者可从肾脏丢失大量AT- Ⅲ;
大面积烧伤患者,AT- Ⅲ可随血浆丢失;
DIC时也有AT- Ⅲ消耗增多。
2. 蛋白C和蛋白S缺乏
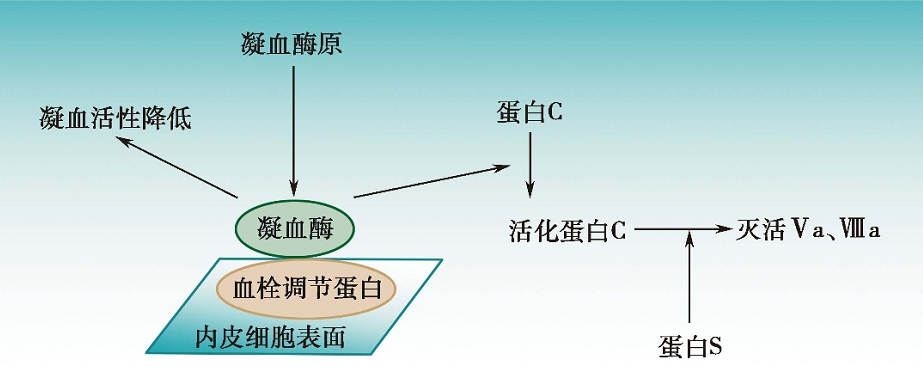
蛋白C(PC)在肝脏合成,以酶原形式存在于血液中,凝血酶可将之活化为激活的蛋白C(APC)。
APC可水解FⅤa、FⅧa,使其灭活,阻碍了由FⅧa和FⅨa组成的FⅩ激活物的形成,另一方面也阻碍
了由FⅤa和FⅩa组成的凝血酶原激活物的形成。
此外,APC还可限制FⅩa与血小板结合,灭活纤溶酶原激活物抑制物,并促进纤溶酶原激活物的释放。
蛋白S(PS)作为APC的辅因子,可促进APC清除凝血酶原激活物中的FⅩa。
血栓调节蛋白(thrombomodulin,TM)是内皮细胞膜上的凝血酶受体之一,与凝血酶结合后降低其凝血活性,却显著增强了凝血酶激活蛋白C的作用。因此,血栓调节蛋白是使凝血酶由促凝转向抗凝的重要的血管内凝血抑制因子。
(1)遗传性缺乏或异常和APC抵抗
1)遗传性蛋白C、蛋白S缺乏或异常:包括数量缺乏和结构异常,临床上多发生深部静脉血栓症或血栓形成倾向。
2)APC抵抗:正常情况下,在血浆中加入APC,活化部分凝血活酶时间(APTT)延长。但一部分静脉血栓症患者的血浆标本,若想获得同样的APTT延长时间,必须加人更多的APC,称为APC抵抗。
产生APC抵抗的主要原因有蛋白S缺乏、抗蛋白C抗体和抗磷脂抗体的产生以及FV或FVⅢ基因突变等。
(2)获得性缺乏
维生素K缺乏或应用维生素K拮抗剂、严重肝病、肝硬化等可使其合成障碍,引起蛋白C、蛋白S缺乏。
二、纤溶系统功能异常
1. 纤溶系统的激活与抑制
纤溶系统主要包括纤溶酶原激活物( plasminogen activator,PA) 、纤溶酶原、纤溶酶、纤溶抑制物等成分。其主要功能是使纤维蛋白凝块溶解,保证血流畅通,另外,也参与组织的修复和血管的再生等。
纤溶酶原主要在肝脏、骨髓、嗜酸性粒细胞和肾脏合成,可被纤溶酶原激活物水解为纤溶酶。
纤溶酶可使纤维蛋白(原)降解为纤维蛋白(原)降解产物,还能水解凝血酶、FⅤ、FⅧ、FⅫ等,参与抗凝
作用。
纤溶抑制物主要有:纤溶酶原激活物抑制物-1 ( PAI-1)、补体C1抑制物、α2-抗纤溶酶、α2-巨球蛋白和凝血酶激活的纤溶抑制物( TAFI)等。
2. 纤溶功能亢进引起的出血倾向
(1)遗传性纤溶功能亢进
目前已发现先天性α2-抗纤溶酶缺乏症和PAI-1缺乏症可引起出血倾向。
(2)获得性纤溶功能亢进
可见于 下列几种情况:
①富含纤溶酶原激活物的器官,如子宫、卵巢、前列腺、心、肺、脑等脏器大手术或严重损伤时,可释放大量纤溶酶原激活物,引起纤溶亢进;
②某些恶性肿瘤(如白血病等)也可释放大量组织型纤溶酶原激活物人血,引起纤溶亢进;
③肝脏功能严重障碍,如:肝硬化、肝癌、肝叶切除等,可因PAI-1合成减少或组织型纤溶酶原激活物灭活减少引起纤溶亢进;
④DIC时可产生继发性纤溶亢进(见DIC);
⑤溶栓疗法时,溶栓药物等可引起纤溶亢进,甚至引起出血。
3. 纤溶功能降低与血栓形成倾向
(1)遗传性纤溶功能降低
1)PAI-1基因多态性
2)先天性纤溶酶原异常症
(2)获得性纤溶功能降低
临床上常见于血栓前状态,动静脉血栓形成、高脂血症、缺血性脑卒中及口服避孕药等。
与血栓形成相关的先天性异常如下:



