水中细菌总数及大肠菌群的测定
【实验目的】
(1)学习水中细菌总数和大肠菌群数量测定的方法-多管发酵法。
(2)了解大肠菌群指数在饮用水细菌学检查中的重要性。
(3)学习快速纸片法测定水中细菌总数和大肠菌群数。
【实验原理】为检验饮用水是否达到卫生标准,需要进行水中的细菌数量及大肠菌群数的测定。细菌总数可以说明水质被污染的程度,一般来说,细菌数量越多,污染的程度越高。大肠菌群是大量出现在粪便中的非致病菌,从其数量的多少可判断水源被人畜排泄物污染的程度,所以大肠杆菌可作为粪便污染的指示菌。国家饮用水标准规定,饮用水中大肠菌群数不超过3CFU/L,细菌总数不超过100CFU/mL。2005年6月开始,城市供水卫生标准有所提高,自来水中细菌菌落数不得超过80CFU/mL,任意取100mL水样不得检出大肠杆菌。因此,对水中的细菌数量及大肠菌群数的检验是保证饮用水安全和控制传染病的有效手段,同时也是评价水质状况的重要指标。
本实验采用平板菌落计数法测定水中细菌总数。其方法是将待测样品经适当稀释,涂布在平板上,经培养后在平板上形成肉眼可见的菌落。统计菌落数,根据稀释倍数和取样量计算出样品中的细菌数量。平板菌落计数法由于计算的是平板上形成的菌落数,故其反映的是样品中活菌的数量,又称活菌计数法。另外,由于样品往往不易完全分散成单个细胞,平板上形成的每个菌落不一定是单个细胞生长繁殖而成,有的可能来自两个或多个细胞,故平板菌落计数法使用菌落形成单位(colony-forming unit, CFU),而非绝对细菌数量。水中大肠菌群数量的测定可采用多管发酵法或滤膜法。其中,多管发酵法是最通用的方法。其原理是,利用大肠菌群发酵乳糖产酸、产气的生理特点,将水样根据含菌量做适当稀释后,接种到乳糖蛋白胨发酵液中,经37℃培养24h后,如果试管中发酵液由紫色变为黄色,且小管内有气体产生,说明产酸、产气,判为阳性;若24h后尚未产气,可能由于菌量少,可继续培养到48h,判定结果为可疑;若既不产酸,也不产气,判为阴性。此法适用于各种水样的检测,但操作繁琐,需要时间长。相比较而言,滤膜法操作简便、快速。该法是采用一种孔径约0.45μm的多孔硝化纤维膜或乙酸纤维膜滤膜过滤器过滤水样,使其中的细菌截留在滤膜上,然后将滤膜放在适当的培养基上进行培养,大肠菌群可直接在膜上生长,从而可直接计数。此法仅适用于水质较好、体积较大的水体,如大城市的水厂常采用此法,但不适用于杂质较多、易于阻塞滤孔的水样。
【实验器材】
1.实验材料自来水、池水、河水或湖水。2.乳糖蛋白胨水培养基(内含倒置杜氏小管)、三倍浓缩乳糖蛋白胨水培养基(内含倒置杜氏小管)、伊红美蓝培养基(EMB培养基)。
2.试剂无菌水等。
3.器皿内装9mL无菌水的试管、内装50mL无菌水的三角烧瓶、无菌带玻璃塞瓶、无菌培养皿、无菌吸管、微孔滤膜(孔径0.45μm)、过滤器(容量500mL)、抽气设备、镊子、移液管、接种环、酒精灯等。
【实验步骤】
1.水样的采取
(1)自来水先将自来水龙头用火焰灼烧3min灭菌,再开放水龙头使水流5min,以无菌三角烧瓶接取水样,以待分析。
(2)池水、河水或湖水取距水面10~375px水层的水样。先将无菌的玻璃瓶瓶口向下浸入水中,然后翻转过来,除去玻璃塞,水即流入瓶中,盛满后,将瓶塞盖好,再从水中取出。注意:采来的水样最好立即用于检测,否则需放入4℃冰箱中暂时保存。
2.细菌总数测定
(1)自来水
1)加样:用无菌吸管吸取1mL水样,注入无菌培养皿中。每个水样重复三皿。2)制平板:分别倾注约15mL已溶化并冷却到45℃左右的牛肉膏蛋白胨琼脂培养基,盖上皿盖,立即轻轻旋转摇动,使水样与培养基充分混匀,平放待凝。另取一空的无菌培养皿,倾注牛肉膏蛋白胨琼脂培养基15mL,作空白对照。3)培养:平板凝固后,倒置于37℃培养箱中,培养24h。
(2)池水、河水或湖水
1)稀释水样:取3支装有9mL无菌水的试管,加入1mL水样,依次稀释到10-3。注意:稀释倍数视水样污浊程度而定,以培养后平板的菌落数在30~300个之间的稀释度最为合适。若一般中等污秽水样,可取10-1、10-2、10-3稀释度;污秽严重的水样,取10-2、10-3、10-4甚至更高的稀释度。2)加样:取适当稀释度水样1mL加入空的无菌培养皿中,每一稀释度做2个重复。3)以下步骤与“自来水”的方法相同。
(3)菌落计数
1)首先选择平均菌落数在30~300个之间的,当只有一个稀释度的平均菌落数符合此范围时,则该平均菌落数乘以稀释倍数即为该水样的细菌总数(附表2中例1)。
2)若有两个稀释度的平均菌落数均在30~300个之间,则按两者菌落总数之比值来决定。若其比值小于2,应取两者的平均数;若大于2,则取其中较小的菌落总数(附表2中例2及例3)。
3)若所有稀释度的平均菌落数均大于300,则应按稀释度最高的平均菌落数乘以稀释倍数计算(附表2中例4)。
4)若所有稀释度的平均菌落数均小于30,则应按稀释度最低的平均菌落数乘以稀释倍数计算(附表2中例5)。
5)若所有稀释度的平均菌落数均不在30~300个之间,则以最接近300或30的平均菌落数乘以稀释倍数计算(附表2中例6)。
注意:同一稀释度的两个平板,若其中一个平板有较大片状菌苔生长,则不应采用,而以无片状菌苔生长的平板作为该稀释度的平均菌落数;若片状菌苔的大小不到平板的一半,而其余的一半菌落分布又很均匀时,则可将此一半的菌落数乘2以代表整个平板的菌落数。以上平板菌落计数的方法如图11-1所示。
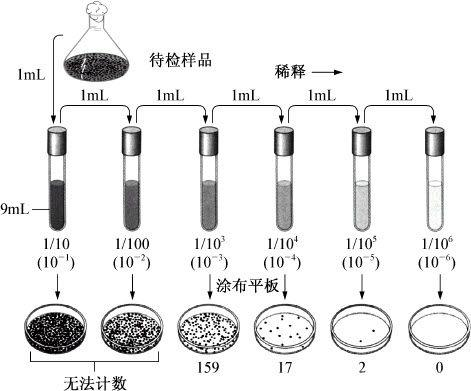
图11-1 平板菌落计数法
3.大肠菌群指数测定
(1)多管发酵法(图11-2)
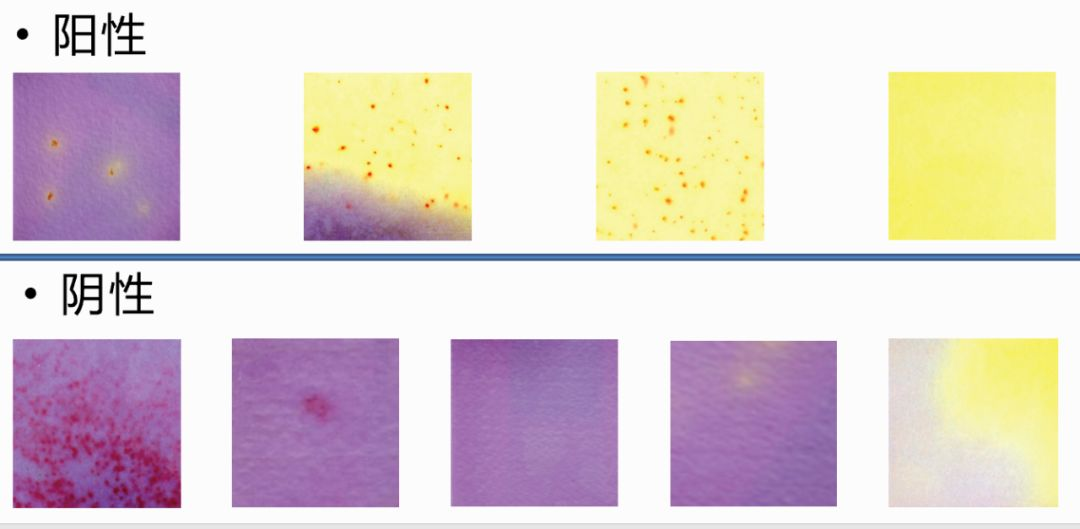
1)自来水①初发酵:取10mL水样接种到10mL双料乳糖蛋白胨培养液中,取1mL水样接种到10mL单料乳糖蛋白胨培养液中,另取1mL水样注入到9mL灭菌生理盐水中,混匀后吸取1mL(即0.1mL水样)注入到10mL单料乳糖蛋白胨培养液中,每一稀释度接种5管。混匀后,于36℃培养24h(24h未产气的继续培养至48h)。
②平板分离:将24h培养后产酸、产气及48h培养后产酸、产气的发酵管(瓶)中的菌液,分别划线接种于伊红美蓝琼脂平板上,于37℃培养18~24h,将符合下列特征的菌落进行涂片、革兰氏染色和镜检:(a)深紫黑色、有金属光泽;(b)紫黑色、不带或略带金属光泽;(c)淡紫红色、中心颜色较深。
③复发酵:经涂片、染色和镜检后,如为革兰氏阴性无芽孢杆菌,则挑取该菌落,重新接种于普通浓度的乳糖蛋白胨水培养基试管中,每管可接种同类型菌落1~3个,于37℃培养24h,若结果是产酸又产气,即证实有大肠菌群存在。根据初发酵试验的阳性管(瓶)数查附表4,即得大肠菌群数。
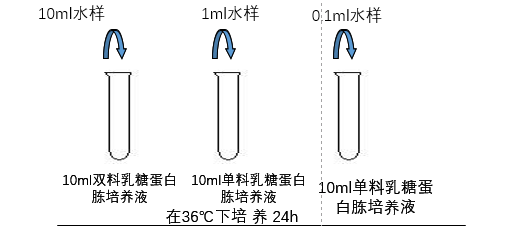
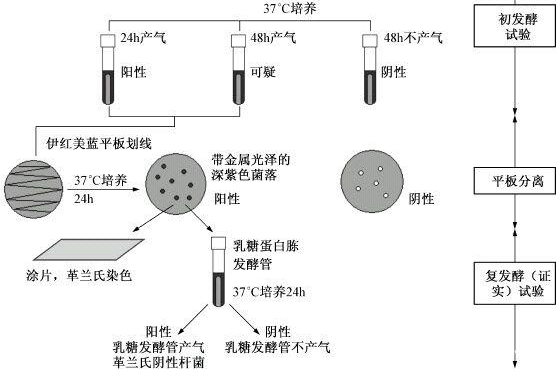
图11-2 多管发酵法测定水中大肠菌群的操作方法
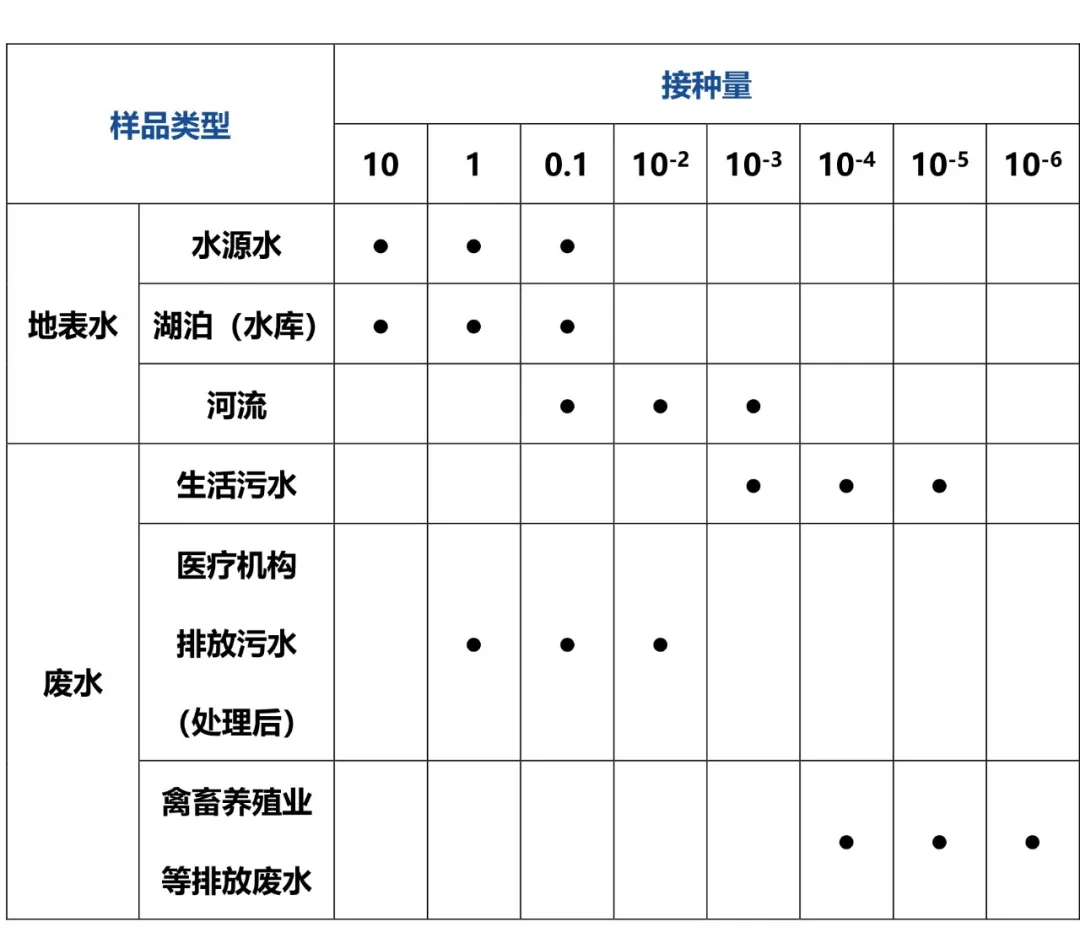
2)池水、河水或湖水①稀释水样:将水样稀释成10-1与10-2。②初发酵:分别吸取1mL10-2、10-1的稀释水样和1mL原水样,注入装有10mL普通浓度乳糖蛋白胨试管中。另取10mL和100mL原水样,分别注入装有5mL和50mL三倍浓缩乳糖蛋白胨水培养基的试管和三角烧瓶中。③以下步骤同上述“自来水”的平板分离和复发酵试验。所加水样体积为100、10、1、0.1mL的发酵管结果查附表11-3;水样体积为10、1、0.1、0.01mL的发酵管结果查附表11-4(15管法,最大可能数表),即得每升水样中的大肠菌群数。
附录1:
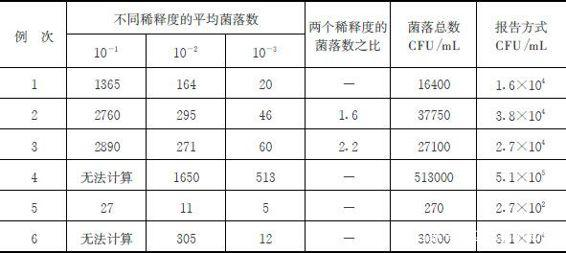
附表2 计算菌落总数方法
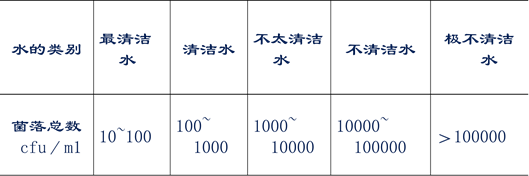
附表3 一般水源水中菌落总数与水清洁程度的关系