一、主要的免疫细胞
(一)淋巴细胞
根据其发生来源、形态特点和免疫功能等方面的不同,淋巴细胞可分为T细胞、B细胞和NK细胞三类。
1. T细胞 来源于骨髓,在胸腺发育成熟并转移到外周淋巴器官或淋巴组织。在没有接触特异性抗原分子前,保持相对静息状态,称初始T细胞。一旦接触了抗原呈递细 胞呈递的与其抗原受体相匹配的抗原肽,它们便转化为代谢活跃、直径为15 ~20nm的大淋巴细胞,并增殖分化。成熟的T细胞体积较小,大部分分化为效应T细胞,小部分形成记忆性T细胞。效应T细胞有显著MHC限制性,只在近距离起作用,能迅速清除抗原,其寿命仅1周左右;而记忆性T细胞寿命可长达数年,甚至终身,当它们再次遇到相同抗原时,能迅速转化增殖,形成大量效应T细胞,启动更大强度的免疫应答,并使机体较长期保持对该抗原的免疫力。
T细胞分为三个亚群:
(1)辅助性T细胞:简称Th细胞,表达CD4膜分子。能分泌多种细胞因子,以辅助其他淋巴细胞发挥免疫活性。Th细胞有Thl、Th2、Thl7、Th9、Th22和Tfh等亚型,Thl细胞参与细胞免疫及迟发型超敏性炎症反应;Th2可辅助B细胞分化为浆细胞,参与体液免疫应答;Thl7与机体自身免疫病的发生和急性炎症的调节密切相关。
(2)细胞毒性T细胞:简称Tc细胞,表达CD8膜分子,具有直接、连续、特异性 免疫杀伤效应的功能。它们能直接攻击外来的异体细胞、体内的肿瘤细胞和病毒感染细胞等。当它们与靶细胞接触后,能释放穿孔素,嵌入靶细胞膜内形成多聚体穿膜管状结构,细胞外液便可通过此管状结构进入靶细胞,导致细胞溶解死亡。Tc细胞还分泌颗粒酶,从小孔进入靶细胞,诱发靶细胞凋亡。
(3)调节性T细胞:简称Tr细胞,数量较少,表达CD4、CD25膜分子和核转录因子Foxp3,具有对机体免疫应答的负调节功能。Tr细胞通过接触方式,或通过分泌抑制性细胞因子如IL-10、TGF-B等,直接或间接抑制T细胞的增殖、分化及其活性。Tr细胞的免疫学特点是诱导免疫无能和免疫抑制,进而通过下调机体的免疫应答,维持对抗原的免疫耐受,其数量和功能异常往往导致自身免疫性疾病。
由于效应T细胞可直接杀灭靶细胞,故T细胞参与的免疫称细胞免疫。
2. B细胞
在骨髓成熟的初始B细胞迁移到外周淋巴器官和淋巴组织的初级淋巴小结,在相应抗原刺激下,呈递转化为大淋巴细胞并增殖分化,其大部分子细胞成为效应B细胞,即浆细胞,分泌抗体。抗体与相应抗原结合后,发挥中和毒素、中和病毒、阻止病原体黏附细胞的作用, 加速了巨噬细胞对抗原的吞噬和清除。小部分子细胞成为记忆性B细胞,其作用和记忆性T细胞相同。
B细胞分为两个亚群:
(1) B-1细胞:在人和小鼠仅占B细胞总数的5%〜10%,来源于胚胎肝造血干细胞,高表达CD5 分子,主要分泌IgM,其活化不需要T细胞参与,主要对最常见微生物的碳水化合物抗原作出反应,在 机体抗感染时发挥作用。它们构成了黏膜B细胞的50%,但不形成记忆B细胞。
(2) B-2细胞:即绝大多数B细胞,表达CD40分子,主要分泌IgG,其活化需要T细胞参与,主要 对蛋白质抗原作出反应,能与Th2细胞结合并释放细胞因子,从而抑制Thl细胞的细胞周期,促进记 忆B细胞和浆细胞形成,是体液免疫的主要执行者。
由于B细胞以分泌抗体这一可溶性蛋白分子进入体液而执行免疫功能,故B细胞介导的免疫称 体液免疫。
3. NK细胞 来源于骨髓,约占血液淋巴细胞的15%,为大颗粒淋巴细胞,直径约15um,表达 CD16和CD56,不表达T细胞和B细胞的膜受体,无需抗原呈递细胞的中介即可活化,属于固有免疫 细胞,其杀伤靶细胞没有MHC限制性,是机体抗肿瘤和抗感染免疫的第一道天然防线。
淋巴细胞再循环:外周淋巴器官和淋巴组织内的淋巴细胞可经淋巴管进入血流,循环于全身,它们又可通过弥散淋巴组织内的高内皮微静脉(见后述),再返回淋巴器官或淋巴组织,如此周而复始,使淋巴细胞从一个淋巴器官或一处淋巴组织进入另一个淋巴器官或另一处淋巴组织,这种现象称淋巴细胞再循环。淋巴细胞再循环使得体内淋巴细胞的区域分布更趋合理,局部的淋巴细胞能得到不断补充,使分散于全身的免疫细胞成为一个相互关联的统一体,也增加了其与 抗原接触和活化的机会,有利于识别抗原,产生更有效的免疫应答。
(二)巨噬细胞及单核吞噬细胞系统
巨噬细胞由血液单核细胞穿出血管进入结缔组织后分化形成,广泛分布于机体,为终末细 胞,一般不再返回血液。与单核细胞相比,巨噬细胞无论形态还是功能均发生显著变化,体积增 加5-10倍,细胞器尤其溶酶体大量增加,功能更为复杂,吞噬能力增强,能分泌大量的可溶性 因子。单核吞噬细胞系统包括单核细胞和由其分化而来的具有吞噬功能的细胞,包括结缔组织和淋巴组织的巨噬细胞、骨组织的破骨细胞、神经组织的小胶质 细胞、肝巨噬细胞(库普弗细胞)和肺巨噬细胞(尘细胞)等,它们均具有强大的吞噬能力,也是主要的抗原呈递细胞。
(三)抗原呈递细胞
抗原呈递细胞是指能捕获和处理抗原,形成抗原肽/MHC分子复合 物,并将抗原呈递给T细胞,激发后者活化、增殖的一类免疫细胞。专司抗原呈递功能的专职性APC 主要有树突状细胞、单核/巨噬细胞和B淋巴细胞。
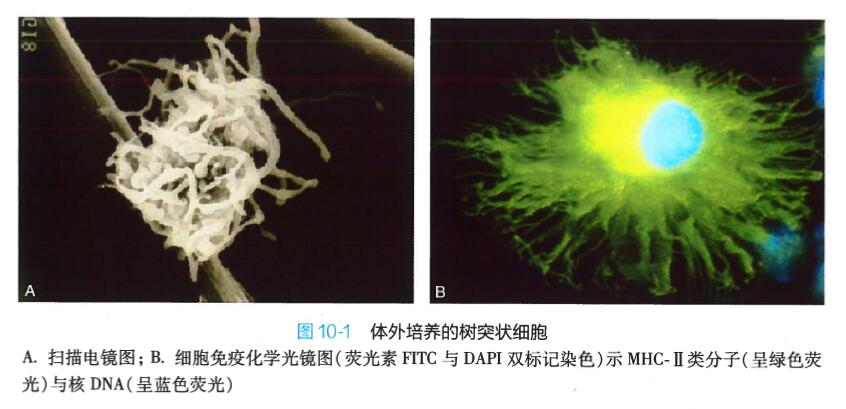
树突状细胞:是目前发现的抗原呈递功能最强的APC,因其胞体具有很多树枝状的突起而得名(图10-1 )。 DC来源于骨髓造血干细胞,数量很少,但分布很广,不同部位名称不同,包括表皮的朗格汉斯细胞,心、肝、肺、肾、消化管的间质DC,胸腺DC,淋巴内的面纱细胞,外周淋巴组织中的交错突细胞及血液DC等,它们分别处于不同的发育成熟时期,隶属不同亚型。DC在迁移过程中摄取抗原能力逐渐下降,而抗原呈递功能不断增强。
二、淋巴组织
淋巴组织以网状组织为支架,网孔内充满大量淋巴细胞及其他免疫细胞,是免疫应答的场所。淋巴组织分为弥散淋巴组织和淋巴小结两种。
1.弥散淋巴组织无明确的界限,组织中除有一般的毛细血管和毛细淋巴管外,还常见直径约30-50um的高内皮微静脉(HEV),即毛细血管后微静脉,其内皮细胞为杆状,能分泌黏附分子以利于淋巴细胞穿越,是淋巴细胞从血液进入淋巴组 织的重要通道(见图10-8)。抗原刺激可使弥散淋巴组织扩大,并出现淋巴小结。
2.淋巴小结又称淋巴滤泡,为直径1-2mm的球形小体,界限较明确。淋巴小结受抗原刺激后增大,并产生生发中心。无生发中心的淋巴小结较小,称初级淋巴小结,有生发中心的称次级淋巴小结。
生发中心可分为深部的暗区和浅部的明区。暗区较小,主要由B细胞和Th细胞组成,由于细胞较大,嗜碱性较强,故暗区着色深;明区较大,除B细胞和Th细胞外,还多见滤泡树突状细胞和巨噬细胞。生发中心的周边有一层密集的小淋巴细胞,着色较深、形似新月,尤以顶部最厚,称小结帽(图10-2,图10-3)。
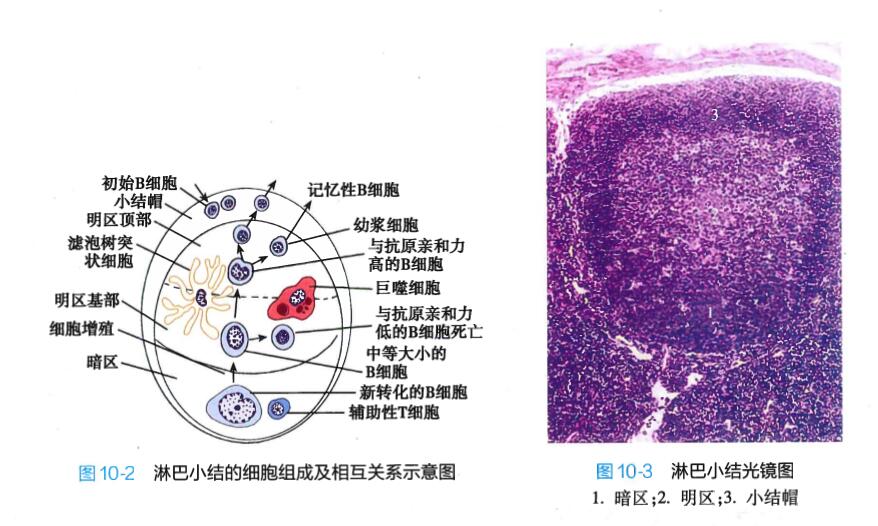
生发中心的形成过程如下:初始B细胞或记忆性B细胞识别抗原并与Th细胞相互作用后, 迁移到初级淋巴小结并分裂增殖,成为大而幼稚的生发中心母细胞,它们紧密聚集,构成暗区。这些细胞继续增殖分化,生成体积较小的生发中心细胞,后者排列不甚紧密,其间夹杂较多的滤泡树突状细胞,构成明区。部分B细胞经过不断分化发育,形成体积 较小的幼浆细胞及记忆性B细胞。幼浆细胞将迁移至附近的弥散淋巴组织,或进入稣巴后迁移至机体其他部位的淋巴组织或结缔组织,转化为浆细胞,分泌抗体。不发生分裂增殖的B细胞被推向外侧,形成小结帽。
次级淋巴小结的发育一般在接触抗原后2周达高峰。淋巴小结增大增多是体液免疫应答的重要 标志,抗原被清除后淋巴小结又渐消失。
滤泡树突状细胞(FDC)与一般的树突状细胞在来源和功能上有很大差别。 FDC虽然也有很多树枝状突起,但它们并非源于骨髓细胞,也不表达MHC-H类分子,其细胞表面有丰富的抗体受体,可与抗原结合成抗原-抗体复合物。
三、胸腺
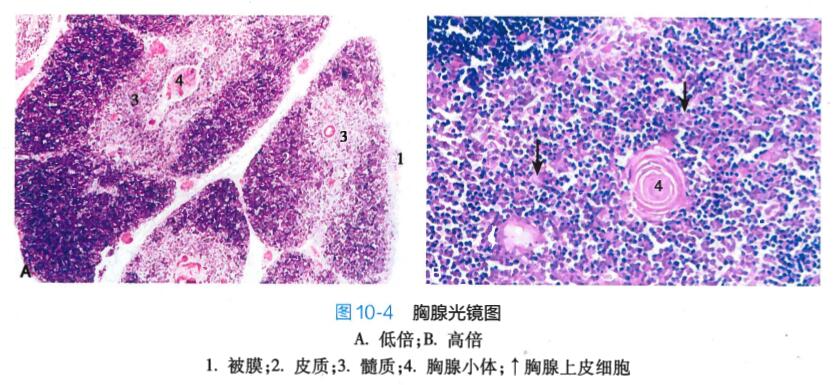
1. 胸腺的结构 胸腺分左右两叶,表面有薄层结缔组织被膜。被膜结缔组织成片状伸入胸腺内部形成小叶间隔,将实质分隔成许多不完全分离的胸腺小叶,每个小叶都有皮质和髓质两部分,相邻小叶间的髓质相互连续。皮质内胸腺细胞密集,故着色较深;髓质含较多上皮细胞,故着色较浅(图10-4)。胸腺为T细胞发育提供了独特的微环境,构成这一微环境的细胞统称胸腺基质细胞,主要包括胸腺上皮细胞、胸腺树突状细胞、巨噬细胞、嗜酸性粒细胞、肥大细胞、成纤维细胞等。胸腺于幼儿期较大,进入青春期后逐渐退化缩小,到老年时期胸腺实质大部被脂肪组织代替,皮 质可完全消失,但髓质则终生存留。
(1)皮质(cortex):以胸腺上皮细胞为支架,间隙内含有大量胸腺细胞和少量基质细胞(图10-5) 。
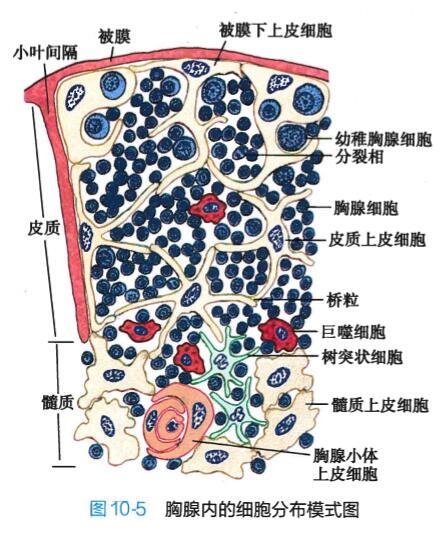
胸腺上皮细胞(thymic epithelial cell):又称 上皮性网状细胞。皮质的上皮细胞分布于被膜 下和胸腺细胞之间,多呈星形,有突起,相邻上 皮细胞的突起间以桥粒连接成网。某些被膜下 上皮细胞胞质丰富,包绕胸腺细胞,称哺育细胞 (nurse cell) o胸腺上皮细胞表面表达大量的 MHC分子,能分泌胸腺素(thymosin)、胸腺肽 (thymulin )和胸腺生成素(thymopoietin ),为胸腺 细胞发育所必需。
胸腺细胞(thymocyte):即胸腺内处于不同 分化发育阶段的T细胞,它们密集于皮质内,占 皮质细胞总数的85%〜90%。
由骨髓来的淋巴性造血干细胞进入胸腺, 在由皮质到髓质的迁移发育过程中,在周围胸 腺基质细胞参与下,经受了两次选择,即阳性选 择和阴性选择。阳性选择发生在皮质外层,赋 予T细胞具有MHC分子限制性识别能力;而阴 性选择则发生在皮质深层和髓质,淘汰了能与机体自身抗原发生反应的T细胞。最终只有不足5% 左右的胸腺细胞发育成熟,成为初始T细胞,具有正常的免疫应答潜能。而绝大部分胸腺细胞发生凋 亡,被巨噬细胞吞噬清除。
(2)髓质(medulla):内含较多胸腺上皮细胞、少量初始T细胞和巨噬细胞等。髓质上皮细胞呈 多边形,胞体较大,细胞间以桥粒相连,也能分泌胸腺素,部分胸腺上皮细胞构成胸腺小体。
胸腺小体(thymic corpuscle)是胸腺髓质的特征性结构,随年龄增长而增加,直径30〜150呻,散 在分布,由胸腺上皮细胞呈同心圆状排列而成。小体外周的上皮细胞,其核明显,细胞可分裂;近小体 中心的上皮细胞,核渐退化,胞质中含有较多角蛋白;小体中心的上皮细胞则已完全角质化,呈强嗜酸 性染色,有的已破碎,呈均质透明状。小体中还常见巨噬细胞、嗜酸性粒细胞和淋巴细胞。
胸腺小体的作用仍未完全阐明。人类胸腺小体分泌胸腺基质淋巴细胞生成素(thymic stromal lymphopoietin,TSLP),能刺激胸腺树突状细胞的成熟,后者能够诱导胸腺内调节性T细胞的增殖和 分化。
(3)胸腺的血液供应及血■胸腺屏障:小动脉穿越胸腺被膜,沿小叶间隔至皮质与髓质交界处形 成微动脉,然后发出分支进入皮质和髓质。皮质毛细血管在皮髓质交界处汇合为高内皮微静脉,成熟的初始T细胞在此穿过高内皮进入血流。髓质毛细血管常为有孔型,汇入微静脉后经小叶间隔及被膜出胸腺。
血-胸腺屏1^(blood-thymus barrier):实验证明,血液内的大分子物质如抗体、细胞色素C、铁蛋白、 辣根过氧化物酶等均不能进入胸腺皮质,使胸腺内T细胞分化发育成熟过程基本不受外界抗原影响, 说明皮质的毛细血管及其周围结构具有屏障作用,称血-胸腺屏障。血-胸腺屏障由下列结构组成: ①连续毛细血管,其内皮细胞间有完整的紧密连接;②内皮周围连续的基膜;③血管周隙,内含巨噬细 胞;④上皮基膜;⑤一层连续的胸腺上皮细胞(突起)(图10-6)。血-胸腺屏障在维持胸腺内环境的稳 定,保证胸腺细胞的正常发育中起着极其重要的作用。
2. 胸腺的功能 胸腺是形成初始T细胞的场所,从皮质到髓质,T细胞逐渐成熟。实验证明,若切除新生小鼠的胸腺,该动物即缺乏T细胞,不能排斥异体移植物,周围淋巴器官及淋巴组织中无次 级淋巴小结出现,机体产生抗体的能力也明显下降。若在动物出生后数周再切除胸腺,此时因已有大 量初始T细胞迁移至周围淋巴器官和淋巴组织内,已能行使一定的免疫功能,故短期内看不出影响, 但机体的免疫力仍会逐渐下降。若给切除胸腺的新生动物移植胸腺,则能明显改善该动物的免疫缺 陷状态。研究表明,人类终生保留产生T细胞的能力。
四、 淋巴结
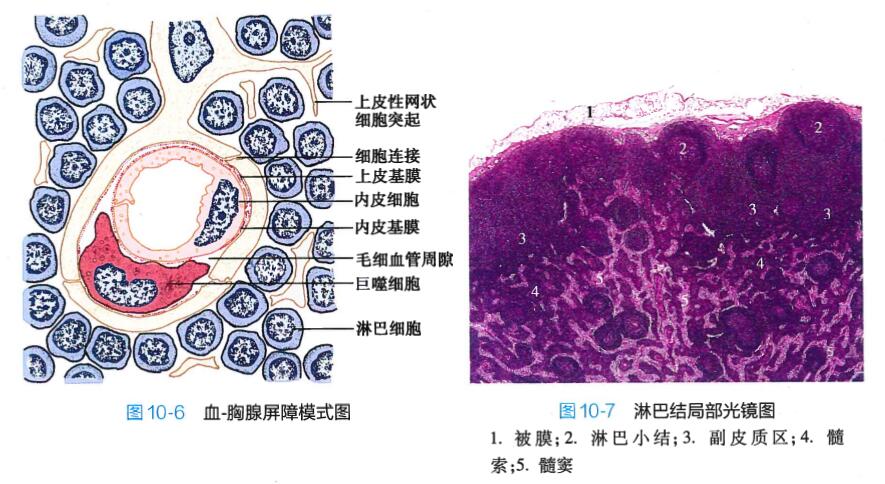
1. 淋巴结的结构 人有500 ~ 600个淋巴结,其大小和结构与机体的免疫功能状态密切相关。 淋巴结表面有薄层致密结缔组织构成的被膜,数条输入淋巴管(afferent lymphatic vessel)穿越被膜,与 被膜下淋巴窦相通连。淋巴结的一侧凹陷,为门部,有血管和输出淋巴管(efferent lymphatic vessel)。 被膜和门部的结缔组织伸入淋巴结实质,形成相互连接的小梁(trabecula),构成淋巴结的粗支架,血 管走行于其内。小梁之间为淋巴组织和淋巴窦。淋巴结实质分为皮质和髓质两部分,二者无截然界限(图 10-7 )。
(1)皮质:位于被膜下方,由浅层皮质、副皮质区及皮质淋巴窦构成。
浅层皮质(superfacial cortex):含淋巴小结及小结之间的弥散淋巴组织,为B细胞区。
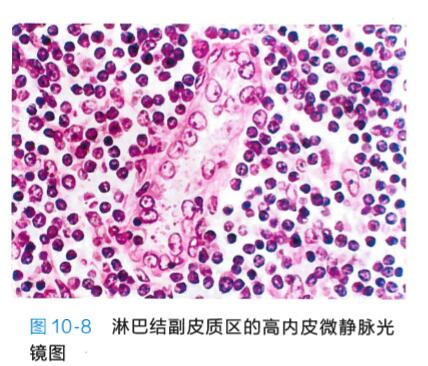
副皮质区(paracortex zone):位于皮质深层,为 较大片的弥散淋巴组织,其淋巴细胞主要为Th细 胞;给新生动物切除胸腺后,此区即不发育,故又称 胸腺依赖区(thymus dependent area ) o该区还有较 多的交错突细胞、巨噬细胞和少量B细胞等。副皮 质区有许多高内皮微静脉,其内皮细胞胞质丰富 (图10-8),核较大,异染色质少,染色浅,核仁明显。 血液流经此段时,约10%的淋巴细胞穿越内皮进入副皮质区,其中B细胞再迁移到淋巴小结,因而高 内皮微静脉是淋巴结内淋巴细胞再循环的重要部 位。在细胞免疫应答时,副皮质区的细胞分裂相增 多,区域范围迅速扩大。
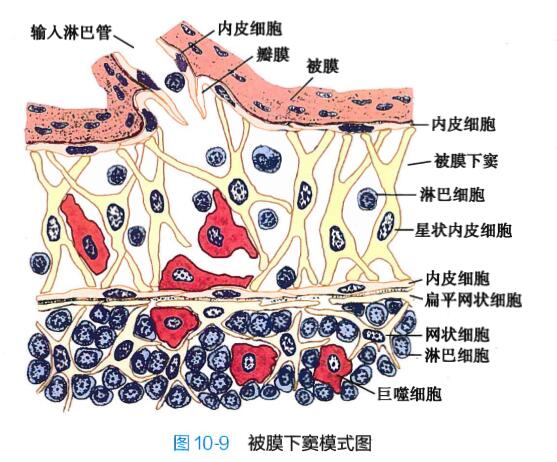
皮质淋巴窦(cortical sinus):包括被膜下方和小梁周围的淋巴窦,分别称被膜下窦和小梁周窦,二 者相互通连。被膜下窦为一宽敞的扁囊,包绕整个淋巴结实质,其被膜侧有数条输入淋巴管通入(图 10-9)。小梁周窦末端常为盲端,仅部分与髓质淋巴窦直接相通。淋巴窦壁由扁平的内皮细胞衬里, 内皮外有薄层基质、少量网状纤维及一层扁平的网状细胞。淋巴窦内有呈星状的内皮细胞支撑窦腔, 有巨噬细胞附着于内皮细胞。淋巴在窦内缓慢流动,有利于巨噬细胞清除抗原。淋巴内的各种细胞 (如面纱细胞)和淋巴液不断穿过或渗过内皮,进入皮质淋巴组织;而淋巴组织中的细胞、抗体等成分 也不断进入淋巴,这样淋巴组织便成为一种动态的结构,有利于免疫应答。
(2)髓质:由髓索和其间的髓窦组成。髓索( medullary cord)是相互连接的索条状淋巴组织,也可见高内皮微静脉。主要含T细胞、B细胞、巨噬细胞和大量浆细胞。髓窦(medullary sinus)与皮质淋 巴窦的结构相同,但较宽大,腔内的巨噬细胞较多,故有较强的滤过功能(图10-10,图10-11)。
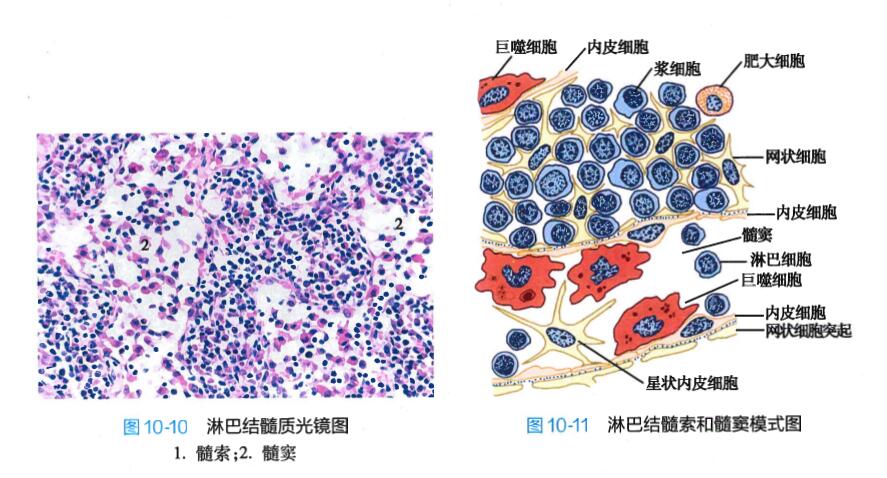
2. 淋巴结内的淋巴通路 淋巴从输入淋巴管进入被膜下窦和小梁周窦,部分渗入皮质淋巴组 织,然后渗入髓窦;部分经小梁周窦直接流入髓窦,继而汇入输出淋巴管。淋巴流经一个淋巴结需数 小时,含抗原越多则流速越慢。淋巴经滤过后,其中的细菌等抗原绝大部分被清除。淋巴组织中的细 胞和产生的抗体等也不断进入淋巴,因此,输出的淋巴常较输入的淋巴含较多的淋巴细胞和抗体。
3. 淋巴结的功能
(1) 滤过淋巴:进入淋巴结的淋巴常带有细菌、病毒、毒素等抗原物质,在缓慢地流经淋巴结时, 它们可被巨噬细胞清除。正常淋巴结对细菌的清除率可达99.5%。
(2) 免疫应答:抗原进入淋巴结后,巨噬细胞和交错突细胞可捕获和处理抗原,并呈递给具有相 应抗原受体的初始T细胞或记忆性T细胞,引起T细胞增殖,副皮质区明显扩大,效应T细胞输出增 多,引发细胞免疫。B细胞在接触抗原后,在Th细胞的辅助下于浅层皮质增殖分化,淋巴小结增多增 大,髓索中浆细胞增多,输出淋巴管内的抗体含量明显上升。淋巴结内细胞免疫应答和体液免疫应答 常同时发生。
五、脾
脾是胚胎时期的造血器官,自骨髓开始造血后,脾演变成人体最大的淋巴器官。
1. 脾的结构 在新鲜的脾切面,可见大部分组织为深红色,称红髓;其间有散在分布的灰白色点 状区域,称白髓,二者构成了脾的实质。脾富含血管,脾内淋巴组织形成的各种微细结构沿血管有规 律地分布(图10-12, 10-13) 。
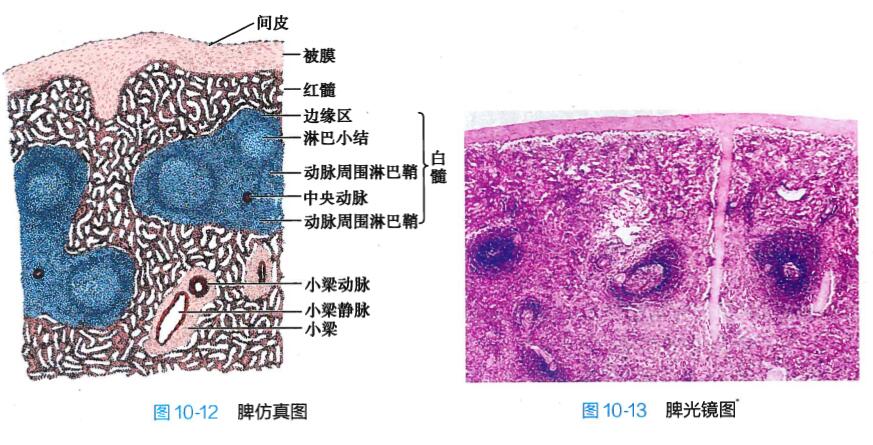
(1) 被膜与小梁:脾的被膜较厚,由富含弹 性纤维、IK型胶原纤维及平滑肌纤维的不规则 致密结缔组织构成,表面覆有间皮。被膜和脾 门的结缔组织伸入脾内形成小梁,构成脾的粗 支架。结缔组织内的平滑肌纤维收缩可调节脾 的含血量。脾动脉从脾门进入后,分支随小梁 走行,称小梁动脉(图10-14) 。
(2) 白髓(white pulp):由动脉周围淋巴鞘、 淋巴小结和边缘区构成湘当于淋巴结的皮质。
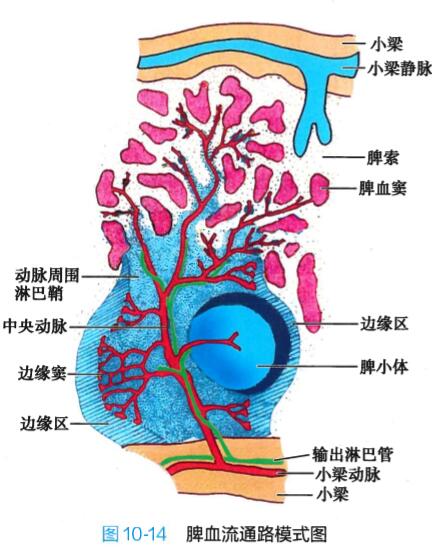
白髓内的主要小动脉称中央动脉(central arteriole)(图10-14)。中央动脉周围有厚层弥散 淋巴组织,由大量T细胞、少量巨噬细胞与交错 突细胞等构成,称动脉周围淋巴鞘(periarterial lymphatic sheath),相当于淋巴结的副皮质区,但 无高内皮微静脉。当发生细胞免疫应答时,动脉 周围淋巴鞘内的T细胞分裂增殖,鞘增厚。中央 动脉旁有一条伴行的小淋巴管,它是鞘内T细胞 经淋巴迁出脾的重要通道。
在动脉周围淋巴鞘的一侧,可见淋巴小结,主要由大量B细胞构成。初级淋巴小结受抗原刺激后 形成生发中心,含较多的滤泡树突状细胞和巨噬细胞,可见明区与暗区,小结帽朝向红髓,在此产生的幼浆细胞多进入红髓的脾索。健康人脾内淋巴小结较少,当抗原侵入时,淋巴小结数量剧增。
在白髓与红髓交界的狭窄区域,称边缘E(marginal zone),宽约100nm。边缘区含有较多巨噬细 胞和一些B细胞。中央动脉的侧支末端在此区膨大,形成小血窦,称边缘窦(marginal sinusoid),是血 液内抗原及淋巴细胞进入白髓的通道。白髓内的淋巴细胞也可进入边缘窦,参与再循环。
(3) 红髓(red pulp):分布于被膜下、小梁周围及白髓边缘区外侧的广大区域,约占脾实质的 80% ,由脾索和脾血窦组成(图10-14,图10-15) 。
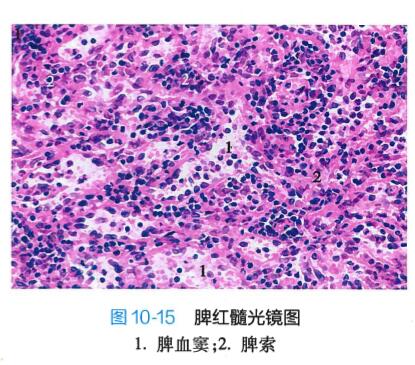
脾索(splenic cord)由富含血细胞的淋巴组织构成,呈不规则索条状,互连成网,网孔即为脾血窦。 脾索含较多网状细胞、淋巴细胞、浆细胞、红细胞、巨噬细胞和树突状细胞。
脾血窦(splenic sinus)宽约20〜50jxm,形态不 规则,互连成网。纵切面上,血窦壁如同多孔隙的 栅栏,由一层纵向平行排列的长杆状内皮细胞围 成,内皮外有不完整的基膜及环行网状纤维;横切 面上,可见内皮细胞沿血窦壁排列,核突入管腔,细 胞间有0.2~0.5nm宽的间隙(图10-16,图10-17)。 脾索内的血细胞可变形,穿越内皮细胞间隙进入血窦。血窦外侧有较多巨噬细胞,其突起可通过内皮间隙伸向窦腔。
2. 脾的血液供应脾的血液供应与其功能密 切相关。脾动脉从脾门进入后分几支进入小梁,称 为小梁动脉,而后离开小梁进入白髓称中央动脉,
中央动脉主干穿出白髓进入脾索后,分支成形似笔毛的笔毛微动脉(peniciRar arteriole),后者除少数直接注入脾血窦外,多数末端扩大成喇叭状,开口于脾索,因而大量血液直接进入脾索(图10-16) 。脾血窦汇入小梁静脉,再于脾门汇合为脾静脉出脾。
3. 脾的功能
(1) 滤血:脾脏是清除衰老红细胞和血小板的主要器官。进入脾索的血细胞,大部分可经变形, 穿过血窦内皮细胞间隙,回到血循环。而衰老的红细胞,由于膜骨架蛋白变性,细胞的变形性降低,不能穿过内皮细胞间隙,滞留在脾索中,被巨噬细胞清除。当脾肿大或功能亢进时,红细胞破坏过多,可 引起贫血。脾切除后,血液内的异形衰老红细胞会大量增多。
(2) 免疫应答:脾是对血源性抗原物质产生免疫应答的部位。进入血液的病原体,如细菌、疟原 虫和血吸虫等,可引起脾内发生免疫应答,脾淋巴小结增多增大,脾索内浆细胞增多;动脉周围淋巴鞘 显著增厚,脾脏的体积增大。细胞放射标记实验显示,每天通过脾血流进行再循环的淋巴细胞数远超 过通过全身淋巴结的细胞总量。
(3) 造血:胚胎早期的脾有造血功能,成年后,脾内仍有少量造血干细胞,当机体严重缺血或某些 病理状态下,脾可以恢复造血功能。