7-6 配位化合物的空间构型(配位化合物的空间构型与杂化轨道类型的对应关系详见于书本表7-1)
形如MLn型的配合物中,M为中心离子(原子),L为配体,按照价键理论,其空间构型取决于中心离子的杂化类型。
以配位数4为例,中心原子进行dsp2杂化,为平面正方形结构;sp3杂化,为四面体构型。配位数6时,中心原子进行sp3d2杂化或d2sp3杂化均为八面体结构。
7-7 配位化合物的磁矩
中心离子的电子(一般看d轨道电子)若全部成对,自旋磁场强度为零。化合物中有未成对电子,自旋磁场强度>0。物质的磁性大小以磁矩μ表示。磁矩μ与未成对电子数n之间的近似关系是

7-8 内轨型和外轨型
配合物的中心体大多数为过渡金属,它们轨道的杂化除有s、p轨道参与外,常有d轨道参与。d轨道参与杂化形成配合物时有两种情况分别是外轨型配合物和内轨型配合物。
比如在配位数为6 的情况中,外层d轨道参与杂化的是sp3d2杂化,形成了外轨型配合物;内层d轨道参与杂化则是d2sp3杂化,形成了内轨型配合物。
相比与外轨型配合物,内轨型配合物的d轨道电子往往经历了重排,使得未成对电子数减少,配合物磁矩下降甚至消失。
dsp2内轨型配合物
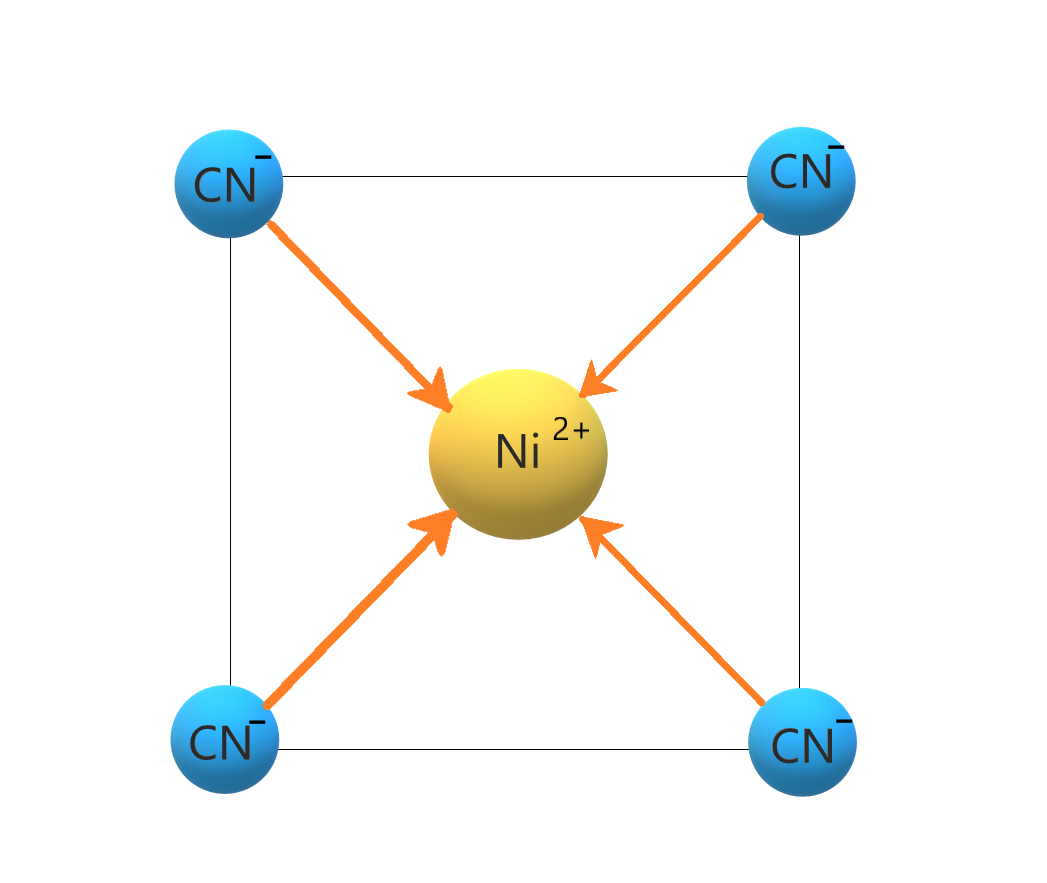
sp3外轨型配合物

7-9 d轨道能级分裂
根据配合物的晶体场理论,中心离子的d轨道在配体的静电场作用下会发生能级分裂。不同的配位数分裂情况不同,配位数为6的配体在八面体场静电场作用下,中心离子的d轨道分裂为两组,它们之间的能量差称为八面体场分裂能Do。
7-10 低自旋和高自旋
过渡金属中心离子有5个简并的d轨道,在八面体场(配位数为6的配合物)中分裂为两组,即三个低能级的t2g轨道和两个高能级的eg轨道。当1个轨道中已有1个电子时,安排第2个电子时需要克服排斥作用才能与之偶合成对,这个能量称为电子成对能Ep。
八面体场中对于d4-d7构型的离子,d电子可以有两种排布方式。Δo>Ep时,第4个以后的d电子优先进入t2g轨道形成低自旋配合物、Δo<Ep时,第4个以后的d电子优先进入eg轨道形成高自旋配合物。
晶体场理论中高自旋相当于价键理论中的外轨型,其磁矩相对较大;低自旋相当于价键理论中的内轨型,磁矩相对较小。
7-11 晶体场稳定化能
在晶体场的作用下,中心离子的d轨道发生分裂后,d电子发生了重排,进入分裂后各轨道上的d电子总能量通常比未分裂前的d电子总能量降低,这部分降低的能量称为晶体场稳定化能(CFSE) 。CFSE的数值越负,代表配合物越稳定。
d轨道在八面体场(配位数6)中的受力情况







