-
1 内容
-
2 测验4.2
一、教学目标
1.了解蛋白质对生物体的重要意义;
2.蛋白质的分类,掌握蛋白质元素组成的特点;
3.掌握氨基酸的结构特点及理化性质;
4.蛋白质一、二、三、四级结构的概念及稳定因素;
5.理解蛋白质结构与功能的关系;
6.掌握蛋白质的理化性质以及这些性质的生理意义及实践意义;
7.了解蛋白质分离提纯常用方法及基本原理。
二、教学重点
1.氨基酸的结构特点及理化性质
2.蛋白质一级结构的概念
3.蛋白质二级结构的概念
4.掌握蛋白质的理化性质以及这些性质的生理意义及实践意义
三、教学难点
1.氨基酸的结构和理化性质
2.蛋白质的结构和功能的关系
蛋白质的分子组成
一、氨基酸
(二)氨基酸的理化性质
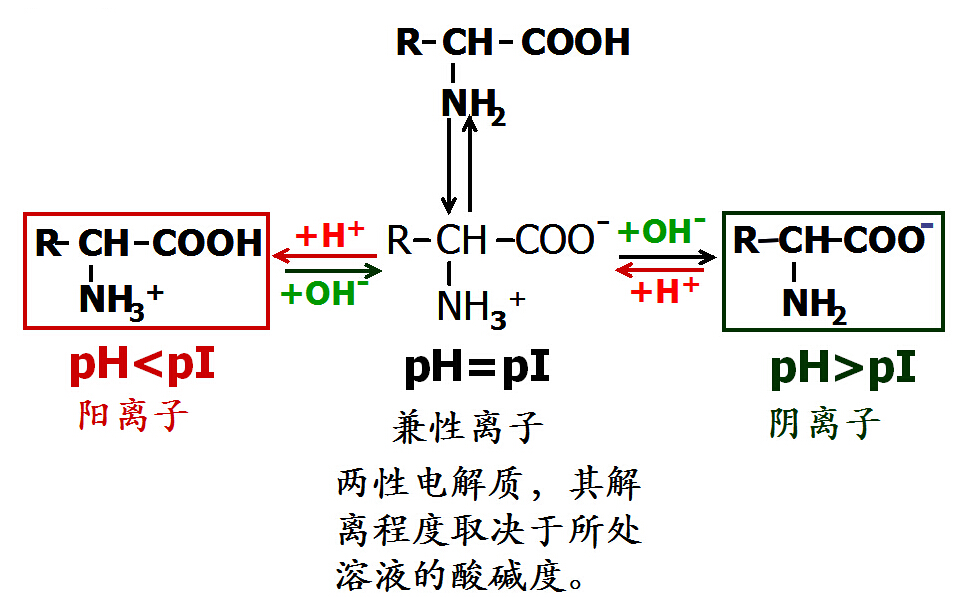
1. 两性解离、等电点
2. 芳香族氨基酸紫外吸收

3.由α-氨基参加的反应
(1) 与亚硝酸反应;
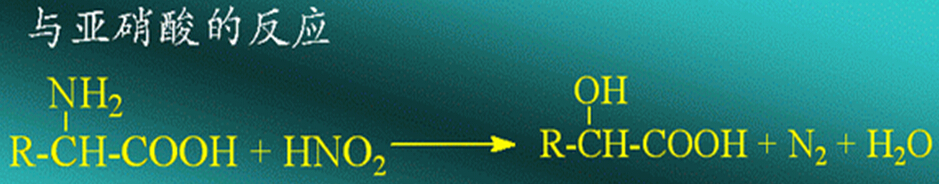
(2) 与甲醛的反应;
(3) 与2,4-二硝基氟苯(2,4-DNFB)的反应(Sanger反应);生成黄色的二硝基苯-氨基酸衍生物。
(4) 与苯异硫氰酸酯(PITC)反应(Edman反应): 生成苯乙内酰硫脲-氨基酸。
(5) 与丹磺酰氯(DNS-Cl)的反应:生成荧光物质DNS-氨基酸。
(3)、(4)、(5)反应用于蛋白质的N-末端的测定。
4. α-羧基参加的反应:
(1)与碱反应成盐
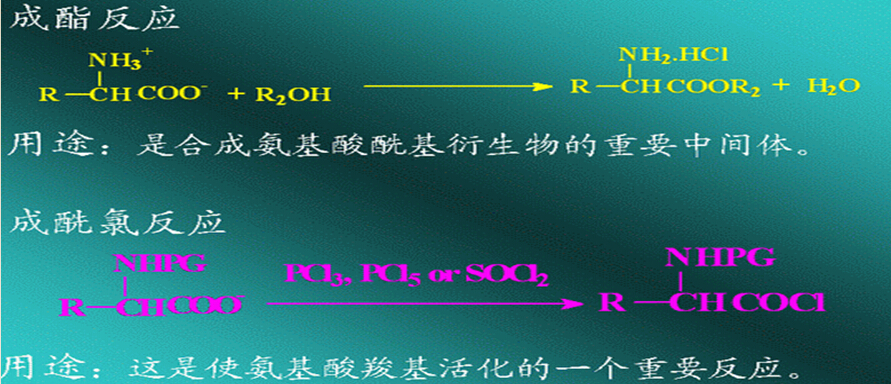
(2)与醇反应成酯
(3)与酰化试剂反应成酰氯
5. α-氨基与α-羧基共同参加的反应:茚三酮反应(ninhydrin reaction)
原理:氨基酸与茚三酮水合物共热,可生成蓝紫色化合物,其最大吸收峰在570nm处。
应用:此法可以对氨基酸进行定量分析(吸收峰值与氨基酸的含量存在正比关系)。
6.侧链反应(颜色反应):
(1) Millon反应:检测Tyr或含Tyr的蛋白质的反应。
Millon试剂:汞的硝酸盐与亚硝酸盐溶液。
产物:红色的化合物。
(2) Folin反应:检测Tyr或含Tyr的蛋白质的反应。
Folin试剂:磷钼酸、磷钨酸混合溶液。
产物:蓝色的钼蓝、钨蓝。
(3) 坂口反应:检测Arg或含Arg的蛋白质的反应。
坂口试剂:α—萘酚的碱性次溴酸钠溶液。
产物:砖红色的沉淀。
(4) Pauly反应:检测His、Tyr及含His、Tyr蛋白质的反应。
试剂:对氨基苯磺酸盐酸溶液、亚硝酸钠、碳酸钠混合溶液。产物:橘红色的化合物。
(5) 乙醛酸的反应:检测Trp或含Trp蛋白质的反应。
当Trp与乙醛酸和浓硫酸在试管中叠加时,产生分层现象,界面出现紫色环。
(6) Cys的反应:Cys或含Cys蛋白质与亚硝基亚铁氰酸钠在稀氨的溶液中,产生一种红色的化合物。


