一、免疫球蛋白的概念
1.免疫球蛋白的发现(Figure)
抗毒素 → 抗体 → 球蛋白 → 免疫球蛋白
1890 → → → 1938 → 1968、1972
2.免疫球蛋白的概念
具有抗体活性或化学性质与抗体相似的球蛋白,Immunoglobulin,Ig.
分泌型:存在于血清和组织液中
膜型:B细胞表面抗原受体
3.抗体与免疫球蛋白的关系
抗体是生物学功能方面概念,免疫球蛋白是化学和结构方面概念;
所有抗体都是免疫球蛋白,免疫球蛋白不一定都是抗体。
二、免疫球蛋白的结构
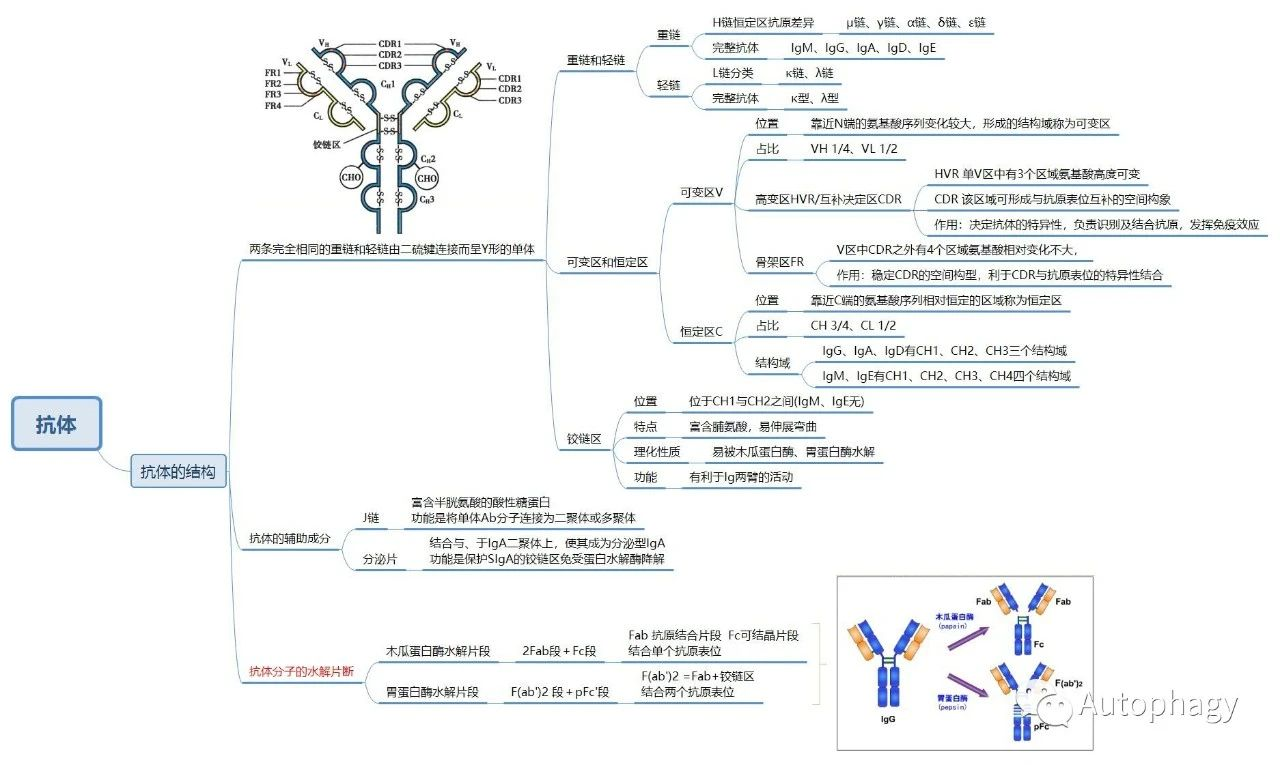
1.基本结构及分类(Figure)
Ig分子单体由4条肽链构成对称的“Y”形结构;
4条肽链:轻链(L链):2条,214个aa残基,分子量为25kD
重链(H链):2条,450-550个aa残基,分子量为50-75kD
重链与轻链通过链间二硫键相连;
★轻链:根据化学结构和抗原性差异,分为两型:κ及λ;
同一Ig分子中,轻链是同型的;同一个体的Ig分子,轻链可以是不同型的;正常人血清中,
κ:λ约为2:1。
★重链:根据aa排列顺序、空间结构、抗原性差异,分为5种:
μ、γ、δ、α、ε;由这五种重链构成的Ig分子分别为:IgM、IgG、IgD、IgA、IgE;
◆ 可变区:N端,L链(VL)约1/2,重链(VH)约1/4(或1/5),该区域aa种类及排列顺序变化较
大;
高变区:HVR1、2、3,又称“互补决定区”,CDR1、2、3;
骨架区:可变区中除高变区以外的区域
◆ 恒定区:C端,L链(CL)约1/2,重链(CH)约3/4(或4/5),该区域aa种类及排列顺序相对稳
定;
◎J链:是酸性含糖肽链,由浆细胞合成,124个aa残基,分子量为15kD,通过二硫键结合在Ig分子H链上,连接Ig分子单体形成多聚体。
◎分泌片:分子量为75kD,以非共价形式与IgA二聚体结合,使IgA分泌至黏膜表面,同时保护IgA免受蛋白酶水解。
2.免疫球蛋白功能区
构成Ig分子的肽链可通过链内二硫键形成球形的环状结构,称为肽环,或功能区(domain),每个功能区约由110个aa残基构成。
L链:2个功能区(VL、CL)
H链:IgM、IgE有5个功能区(VH、CH1、CH2、CH3、CH4);
IgG、IgA、IgD有4个功能区(VH、CH1、CH2、CH3)
Ig功能区的功能:
√ VL、VH:抗原结合部位
√ CL、CH:有部分同种异型的遗传标记
√ IgG CH2:具有补体C1q分子的结合位点;与通过胎盘有关
√ IgG CH3:具有结合FcR功能
√ IgM CH3:具有补体结合位点
√ IgE CH2、CH3:结合FcεR功能
铰链区:①位于CH1、CH2之间,富含脯aa残基和二硫键,易发生伸展及一定程度的转动;
② VL、VH与抗原结合时,该区发生转动,使抗原结合位点更好地与抗原决定簇结合;
③该区转动可致CH1、CH2构型变化,暴露补体结合位点;
④该区对多种蛋白酶敏感,易被水解。
3. 免疫球蛋白水解片段(Figure)
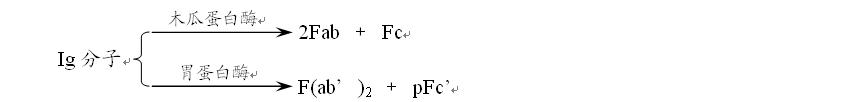
生物学意义:一个Fab片段为单价,可与抗原结合但不能形成凝聚反应或沉淀反应,称为抗原结合片段;Fc片段在低温条件下可析出,称为可结晶片段,可与多种效应分子或免疫细胞相互作用;
F(ab’)2片段为双价,可与抗原结合且能形成凝聚反应或沉淀反应,而且,由于F(ab’)2片段保留了结合抗原的生物性活性,又避免了Fc片段免疫原性可能引起的副作用,因而被广泛的应用于制备生物制品。如白喉抗毒素、破伤风抗毒素经胃蛋白酶消化后精致提纯的制品。
4.免疫球蛋白的血清型(Figure)
①同种型:同一种属内所有个体Ig分子所共有的抗原特异性。
②同种异型:同一种属内不同个体的Ig分子所具有的抗原特异性。
③独特型:同一个体内不同Ig分子的可变区所具有的抗原特异性。