-
1 讲稿
-
2 课件与视频
-
3 知识点扩展
-
4 作业
-
5 参考资料

药品质量标准分析方法的验证
《中国药典》从2000年版起收载了“药品质量标准分析方法验证指导原则”。指导原则指出,药品质量标准分析方法验证的目的是证明采用的方法适合于检验的要求。在建立药品质量标准时,分析方法需经验证;在药品生产工艺变更,制剂的组分变更,或对原分析方法进行修订时,也需要对质量标准的分析方法进行验证。
验证的分析项目有:鉴别试验、杂质检查、原料或制剂中有效成分的含量测定、制剂中其他成分(如防腐剂等)的测定以及药物溶出度、释放度检查中其溶出量的测定方法等。
验证的内容有:准确度、精密度、专属性、检测限、定量限、线性、范围和耐用性等。
一、准确度
准确度是指用该方法的测定结果与真实值或参考值接近的程度。准确度一般用回收率(%)来表示。
验证原料药的含量测定方法时,可用已知纯度的对照品或供试品进行测定,将测定结果与已知的参考值进行比较,也可用本法测得的结果与已知准确度的另一个方法的测定结果进行比较,看是否一致。
制剂的含量测定方法一般用回收试验来考察。将已知量的测定组分加入到处方比例的附加剂中,用验证的方法进行测定,根据测定结果计算回收率。

如不能得到制剂的全部组分,也可将已知量的测定组分加入一定量已知含量的样品中,照验证方法测定,根据测定结果按下式计算回收率:

二、精密度
精密度是指在规定的测试条件下,同一个均匀样品,经多次取样测定所得结果之间的接近程度。精密度一般用偏差、标准偏差(SD)或相对标准偏差(RSD)来表示。若对同一样品重复测定了n次,第i次的测定结果为xi,测定结果的平均值为![]() ,则标准偏差的计算公式为:
,则标准偏差的计算公式为:
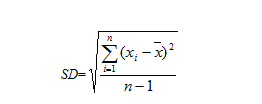
由于SD的大小与所使用的单位以及测定结果数值的大小有关,所以常常使用相对标准偏差来表示精密度。相对标准偏差的计算公式为:
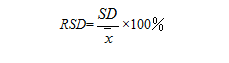
偏差、标准偏差(SD)或相对标准偏差(RSD)越小,说明测定结果越集中,精密度越好。方法的精密度好是准确度高的前提,但方法的精密度好,准确度不一定高,只有在消除了系统误差的前提下,精密度好,准确度也才高。
含量测定和杂质的定量测定应考察方法的精密度。
1.重复性 在相同条件下,由同一个分析人员测定所得结果的精密度称为重复性。考察重复性时,可在规定范围内设计3个不同浓度,每个浓度分别制备3份供试品溶液,进行测定;或制备相当于100%浓度水平的供试品溶液6份,用至少测定6次的结果进行评价。
2.中间精密度 在同一个实验室,不同时间由不同分析人员用不同设备测定结果之间的精密度称为中间精密度。中间精密度用于考察随机变动因素对精密度的影响。
3.重现性 在不同实验室由不同分析人员测定结果之间的精密度称为重现性。法定标准采用的方法应进行重现性试验。如建立药典分析方法时,应通过协同检验得出重现性的结果。
三、专属性
专属性是指在其他组分(如杂质、降解产物、辅料等)可能存在的情况下,分析方法能准确地测出被测组分的特性。原料药物中常含有杂质,如合成的原料、中间体、副产物以及降解产物等,制剂中则含有辅料,分析方法的专属性高,就可以排除这些干扰组分的影响,准确地测定被测组分。
四、检测限
检测限是指分析方法在规定的实验条件下所能检出被测组分的最低浓度或最低量。当被测组分的量高于检测限时,即可被检出,但不一定能准确测定。
1.目视法 非仪器分析的方法采用目视法确定检测限。即用已知浓度的被测物,试验出可能被检出的最低浓度或最低量。如薄层色谱法,可在薄层板上点加不同浓度的供试品溶液,展开后,检视,以可观察的最低浓度作为检测限。
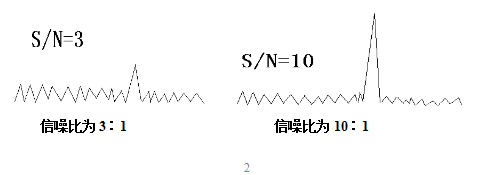
2.信噪比法 对能显示基线噪音的仪器分析方法,可将已知低浓度的被测组分溶液与空白样品的测定结果进行比较,按信(号)噪(音)比确定可被检出的最低浓度。一般以信噪比为3∶1或2∶1时相应的浓度或注入仪器的量确定检测限。
五、定量限
定量限是指样品中被测组分能被定量测定的最低浓度或最低量,其测定结果应具有一定的准确度和精密度。杂质和降解产物用定量方法测定时,应确定方法的定量限。常用信噪比确定定量限,一般以信噪比为10∶1时相应的浓度或注入仪器的量来确定定量限。
六、线性
线性是指在设计范围内,测试结果和样品中被测组分的浓度(或量)直接成正比关系的程度。
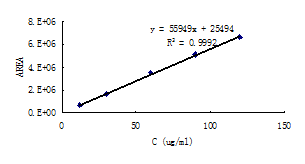
在药物分析中,不少检测结果在理论上和测定组分的浓度(或量)有线性关系,如分光光度法中的吸光度(A)和浓度(C)满足线性方程A=a+bC。理论上有线性关系的两个量,由于受实验条件以及其他因素的影响,是否有线性关系以及线性方程中的两个参数a和b还需要通过实验来确定。考察的方法是配制一系列不同浓度的测定组分溶液(至少5份),分别测定其响应值,用最小二乘法以响应值对浓度进行线性回归,即可计算出相关系数r和a、b的值。相关系数r接近于1,说明线性关系好。
七、范围
范围是指在达到一定的精密度、准确度和线性的前提下,分析方法适用的高低限浓度或量的区间。
范围应根据分析方法应用的具体情况以及线性、准确度和精密度试验的结果来确定。如原料药和制剂的含量测定,范围应为测试浓度的80%~120%;制剂含量均匀度的检查,范围应为测试浓度的70%~130%;溶出度或释放度中溶出量的测定,范围应为限度的±20%。如果含量测定和杂质检查同时进行,用百分归一化法计算,则线性范围应为杂质规定限度的-20%至含量限度的+20%。
八、耐用性
耐用性是指在测定条件有小的变动时,测定结果不受其影响的承受程度。方法的耐用性好,意味着该方法对测定条件的要求不苛刻,一定条件的变化,对测定结果的影响不大。
典型的变动因素有样品溶液的稳定性,样品提取的次数和时间;液相色谱流动相中溶剂的比例和pH值,不同厂牌、不同批号同类型的色谱柱,柱温,流速等;气相色谱的变动因素有:不同厂牌、不同批号的色谱柱、固定相,不同类型的担体,色谱柱、检测器和进样器的温度等。在建立分析方法时,应对以上条件进行试验,以考察方法的耐用性。
不同的检验项目对方法验证指标的要求有所不同,不同检验项目对验证指标的要求见下表:
不同检验项目对效能指标的要求
效 能 指 标 | 鉴 别 | 杂 质 检 查 | 含 量 测 定 | |
定量测定 | 限量检查 | |||
准确度 | - | + | - | + |
精密度 | - | + | - | + |
专属性 | + | + | + | + |
检测限 | - | - | + | - |
定量限 | - | + | - | - |
线性 | - | + | - | + |
范围 | - | + | - | + |
耐用性 | + | + | + | + |