-
1 讲稿
-
2 课件与视频
-
3 知识点拓展图
-
4 作业

(一)原理
吸收系数系指,在给定波长,溶剂和温度等条件下,吸光物质在单位浓度,单位液层厚度时的吸光度。吸收系数是与该物质共轭结构特征相关的物理常数,可用于定性和定量分析。
分子对特定波长光的吸收程度除了与分子的结构有关外,还与被测物质溶液的浓度有关。根据比尔定律,测定药物的吸收系数时,取供试液,测定吸光度值,按下列公式计算吸收系数:
![]()
如果已知药物的吸收系数,可将测得的吸光度代入下式,计算药物的浓度和含量:
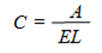
式中,A为吸光度,E为吸收系数,C为被测物质溶液的浓度,L为液层厚度。
随浓度C单位的不同,吸收系数E有不同的意义和表示方法。当C以“mol/L”为单位时,E称为摩尔吸收系数,用表示;当C用“g/100ml”为单位时,E称为百分吸收系数,用
表示。在药品检验中使用百分吸收系数(
![]() ),简称吸收系数,其物理意义是当吸光物质溶液浓度为1% (1g/100ml),液层厚度为1cm时,在一定条件(波长、溶剂、温度)下的吸光度。作为物理常数,不仅可用于考察该原料药的质量,也可作为制剂的溶出度和含量测定中选用值的依据。
),简称吸收系数,其物理意义是当吸光物质溶液浓度为1% (1g/100ml),液层厚度为1cm时,在一定条件(波长、溶剂、温度)下的吸光度。作为物理常数,不仅可用于考察该原料药的质量,也可作为制剂的溶出度和含量测定中选用值的依据。
(二)测定方法
1.仪器
紫外-可见分光光度计,基本结构如图1所示。
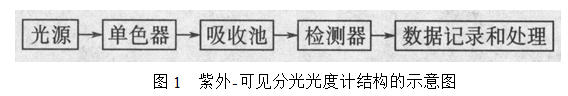
紫外-可见分光光度计的校正和检定:
(1)波长 为保证测定结果的准确性,《中国药典》规定,除定期对仪器进行全面校正和检定外,还应于测定前对波长进行校正。常以汞灯中的几根较强的谱线或用仪器中氘灯的特定谱线为参照进行校正。
(2)吸光度的准确度 取在120℃干燥至恒重的基准重铬酸钾约60mg,精密称定,用0.005mol/L的硫酸溶液溶解并稀释至1000ml,在规定的波长处测定吸光度,计算吸收系数,与规定的数值相比,应符合规定。
(3)杂散光的检查 配制一定浓度的碘化钠和亚硝酸钠溶液,在杂散光影响比较显著的波长处测定透光率,不得大于规定值。
2.测定方法
![]() 值应取精制品采用数台紫外-可见分光光度计测定,并统计处理确定。测定要求如下:
值应取精制品采用数台紫外-可见分光光度计测定,并统计处理确定。测定要求如下:
(1)仪器:选用5台不同的紫外-可见分光光度计。
(2)溶剂:溶剂对供试品应化学惰性;溶剂在选用的波长附近应符合透光限度要求,不得有干扰吸收峰;避免使用低沸点、易挥发的溶剂;水为常用溶剂,当溶液的pH不恒定,并影响到药品的紫外吸收光谱特征时,可采用适宜的缓冲溶液、稀酸或稀碱溶液作为溶剂。
(3)最大吸收波长:以配制供试品溶液的同批溶剂为空白,在规定的吸收峰波长±2nm范围扫描或测试吸光度,以核对供试品的吸收峰波长位置是否正确。并以吸光度最大的波长作为测定波长。
(4)吸收池:吸收池应配对使用,并扣除溶剂空白,或由仪器自动扣除空白。
(5)供试品溶液:直接采用精制供试品进行精密定量试验,再按其干燥品或无水物计算。先定量配制高浓度的供试品溶液,再用同批溶剂定量稀释一倍制成低浓度的供试品溶液,并以同批溶剂为空白分别进行吸光度的精密测定。低高浓度供试品溶液的吸光度应分别在0.3~0.4和0.6~0.8之间。
(6)结果与分析:各供试品溶液应同时精密配制3份,并控制测定环境的温度(25℃±2℃)。同一台仪器测得的![]() 相对偏差应不超过1.0%,所有仪器偏差应不超过1.5%,以平均值定为供试品的
相对偏差应不超过1.0%,所有仪器偏差应不超过1.5%,以平均值定为供试品的![]() 。用于定量测定的
。用于定量测定的![]() 通常应大于100。在同一台仪器上,对多批供试品进行
通常应大于100。在同一台仪器上,对多批供试品进行![]() 值测定,统计分析确定
值测定,统计分析确定![]() 值的合理限度范围,一般在平均值的±5%范围以内。
值的合理限度范围,一般在平均值的±5%范围以内。
(三)应用
1.药物鉴别 测定![]() 可用来鉴别药物或判断药物的纯杂程度。
可用来鉴别药物或判断药物的纯杂程度。
例如,贝诺酯的鉴别则要求供试品的无水乙醇溶液在240nm波长处有最大吸收,且![]() 为730~760(按干燥品计)。头孢克洛的吸收系数测定方法是:取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含20μg的溶液,照紫外-可见分光光度法,在264nm的波长处测定吸光度,吸收系数(
为730~760(按干燥品计)。头孢克洛的吸收系数测定方法是:取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含20μg的溶液,照紫外-可见分光光度法,在264nm的波长处测定吸光度,吸收系数(![]() )为230~255。
)为230~255。
2.杂质检查
若药物与杂质的吸收光谱有明显差别,可以利用本法对杂质进行检查。
例如,地蒽酚中二羟基蒽醌的检查。二羟基蒽醌为地蒽酚的制备原料及氧化分解产物,该杂质的氯仿溶液在432nm波长处有最大吸收(![]() 为495),而地蒽酚在该波长处几乎无吸收(
为495),而地蒽酚在该波长处几乎无吸收(![]() 为2.2)。《中国药典》规定,0.01%的地蒽酚氯仿溶液在432nm波长处的吸光度不得过0.12,即可控制杂质二羟基蒽醌的含量不大于2.0%。
为2.2)。《中国药典》规定,0.01%的地蒽酚氯仿溶液在432nm波长处的吸光度不得过0.12,即可控制杂质二羟基蒽醌的含量不大于2.0%。
又如,肾上腺素在生产中由其酮体经氢化还原制得。若氢化不完全,则易引入酮体杂质。《中国药典》规定,需对酮体进行限量检查。检查原理是利用酮体在310nm波长有最大吸收,而肾上腺素主成分在此波长几乎无吸收,因此通过限制在310nm波长处的吸光度值,即可达到限制相应酮体含量的目的。方法是:取供试品,加盐酸溶液(9→2000)制成每1ml中含2.0mg的溶液,在310nm波长处测定,吸光度不得大于0.05。酮体(![]() 为435)的限量为0.06%。
为435)的限量为0.06%。
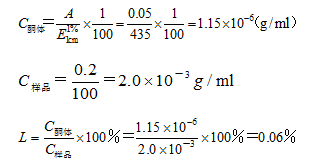
肾上腺素
头孢噻酚钠吸光度的检查。《中国药典》规定,头孢噻吩钠水溶液(20μg/ml)在237nm波长处的吸光度应为0.65~0.72。由于在237nm处的吸收系噻吩乙酰基产生,若产品在精制过程中未有效地除去噻吩乙酸,则在237nm处的吸光度将增大;而当部分产品降解时,吸光度将减少。因此规定供试品溶液吸光度的上下限,可在一定程度上控制杂质的量。
3.含量测定
按各品种项下方法,配制供试品溶液,在规定波长处测定其吸光度,再根据![]() 按下式计算供试品溶液的浓度。
按下式计算供试品溶液的浓度。
例如,对乙酰氨基酚结构中有苯环,在碱性溶液中,在257nm波长处有最大吸收。《中国药典》采用紫外-可见分光光度法测定含量。测定方法为:取本品约40mg,精密称定,置250ml量瓶中,加0.4%氢氧化钠溶液50ml溶解后,加水至刻度,摇匀,精密量取5ml,置100ml量瓶中,加0.4%氢氧化钠溶液10ml,加水至刻度,在257nm的波长处测定吸光度,按对乙酰氨基酚(C8H9NO2)的吸收系数(![]() )为715计算,即得。
)为715计算,即得。
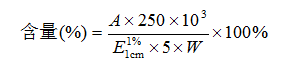
式中,A为测得的吸光度,W为称样量(mg)。