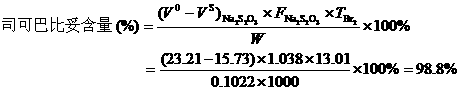-
1 讲稿
-
2 课件与视频
-
3 知识点扩展
-
4 作业
-
5 参考书
一、药物的含量测定方法
含量测定是指用规定的方法测定药物中有效成分的含量。常用的含量测定方法有化学分析法、仪器分析法、生物学方法和酶化学方法等。化学分析法属经典的分析方法,具有精密度高、准确性好的特点。用于含量测定的仪器分析法主要有紫外-可见分光光度法、原子吸收分光光度法、荧光分析法、高效液相色谱法和气相色谱法等。仪器分析方法具有灵敏度高、专属性强的特点。生物学方法包括生物检定法和微生物检定法,是根据药物对生物(如鼠、兔、犬等实验动物)或微生物(如细菌)作用的强度来测定含量的方法。生物学方法的测定结果与药物作用的强度有很好的相关性。使用化学分析法和仪器分析法测定药物的含量,在药品质量标准中称为“含量测定”,测定结果用含量百分率(%)来表示。用生物学方法或酶化学方法测定药物的含量,称为“效价测定”,测定结果一般用效价单位来表示。
化学分析法中最常用容量分析法,操作简便、结果准确、方法耐用性高,但方法缺乏专属性,主要适用于对结果准确度与精密度要求较高的样品测定;光谱分析法简便、快速,灵敏度高、并具有一定的准确度,但方法专属性稍差,主要适用于对灵敏度要求较高、样本量较大的分析项目;色谱分析法则具有高灵敏度与高专属性、并具有一定的准确度,但其结果计算需要对照品,本法主要适用于对方法的专属性与灵敏度要求较高的复杂样品的含量测定。
1.容量分析法
也称滴定法,是将已知浓度的滴定液(标准物质溶液)由滴定管滴加到被测药物的溶液中,直至滴定液与被测药物反应完全(通过适当方法指示),然后根据滴定液的浓度和被消耗的体积,按化学计量关系计算出被测药物的含量。最常用的方法是借助指示剂的颜色或电子设备的电流或电压变化来判断化学计量点。
化学原料药的含量测定,因为纯度较高、所含杂质较少,故强调测定结果的准确和重现,通常要求方法具有更高的准确度和精密度,首选容量分析法;对于药物制剂的含量测定,则因为制剂组分复杂、干扰物质多,且含量限度一般较宽,故更加强调方法的灵敏度和专属性或选择性,多采用具有分离能力的色谱分析法,在辅料不干扰测定时也可选用光谱分析法;而对于药物制剂的定量检查,如溶出度、含量均匀度检查中药物的溶出量或含量的测定,因为分析样本量较大、且限度亦较宽,在辅料不干扰测定时宜选用光谱分析法。
2.滴定度
指每1 ml规定浓度的滴定液所相当的被测药物的质量。在容量分析中,被测药物分子(A)与滴定剂(滴定液中的反应物质单元,B)之间按一定的摩尔(mol)比进行反应,反应可表示为:
![]()
单位体积(VB=1ml)的滴定液相当于被测药物的量![]() 被称为“滴定度”,以T表示,量纲为mg/ml。T是滴定液浓度的一种特殊表示形式。使用T可使滴定结果的计算简化,
被称为“滴定度”,以T表示,量纲为mg/ml。T是滴定液浓度的一种特殊表示形式。使用T可使滴定结果的计算简化,![]() 。
。
因为不同被测药物的摩尔质量以及与滴定剂反应的摩尔比不同,同一滴定液对不同被测药物的滴定度是不同的,计算通式如下:
![]()
式中,m为滴定液的摩尔浓度(mol/L);a为被测药物的摩尔数;b为滴定剂的摩尔数;M为被测药物的毫摩尔质量(分子量,以mg表示)。
例如,用溴酸钾法测定异烟肼[M(C6H7N3O)=137.14]的含量时,溴酸钾滴定液的摩尔浓度为0.01667 mol/L(以KBrO3为单元),化学反应式如下:
![]()
滴定度:![]()
3.含量结果计算
1)直接滴定法:本法是用滴定液直接滴定被测药物,则被测药物的百分含量计算式为:
![]()
在《中国药典》收载的容量分析法中,均给出了滴定度值。根据供试品的称取量(W)、滴定液的消耗体积(V)和滴定度(T),即可计算出被测药物的百分含量。
如配制的滴定液的摩尔浓度与《中国药典》中标准的摩尔浓度不完全一致,应将滴定度(T)乘以滴定液的浓度校正因数(F),换算成实际的滴定度(T′= T×F),或将滴定体积(V)校正为规定浓度时应消耗的体积(V′ = V×F)。其中,
![]()
![]()
2)间接滴定法:间接滴定法包括生成物滴定法和剩余量滴定法。
生成物滴定法系指被测药物与化合物A作用,定量生成化合物B,再用滴定液滴定化合物B。该法的百分含量计算方法与直接滴定法相同,只是在计算滴定度时需考虑被测药物与化合物B以及化合物B与滴定剂三者之间的化学计量关系(摩尔比)。
例如,葡萄糖酸锑钠的含量测定:取本品约0.3g,精密称定,置具塞锥形瓶中,加水100ml、盐酸15ml与碘化钾试液10ml,密塞,振摇后在暗处放置10分钟,用硫代硫酸钠滴定液(0.1mol/L)滴定,至近终点时,加淀粉指示液,继续滴定至蓝色消失,并将滴定的结果用空白试验校正。每1ml硫代硫酸钠滴定液(0.1mol/L)相当于6.088 mg的锑(Sb)。反应式如下:
![]()
![]()
可见,1mol锑(葡萄糖酸锑钠)与碘化钾作用生成1mol碘(I2),而1mol碘(I2)消耗2mol硫代硫酸钠。所以,硫代硫酸钠滴定液(0.1mol/L)对葡萄糖酸锑钠(以Sb=121.76计算)的滴定度
![]()
剩余量滴定法亦称回滴定法,本法是先加入定量过量的滴定液A,使其与被测药物定量反应,待反应完全后,再用另一滴定液B回滴定反应后剩余的滴定液A。在计算百分含量时,需考虑滴定过程中是否进行空白试验校正。当不进行空白试验校正时,含量计算公式如下:
![]()
式中,VA为定量加入的滴定液A的体积(ml),VB为滴定液B在回滴定中被消耗的体积(ml),FA为滴定液A的浓度校正因数,FB为滴定液B的浓度校正因数,TA为滴定液A的滴定度(mg/ml),W为供试品的称取量(mg,量纲与滴定度的一致)。
剩余量滴定法大多进行空白试验校正,其含量计算式如下:
![]()
式中,![]() 为空白试验时消耗滴定液B的体积(ml),
为空白试验时消耗滴定液B的体积(ml),![]() 为样品测定时消耗滴定液B的体积(ml),FB为滴定液B的浓度校正因数(mg/ml),TA为滴定液A的滴定度,W为供试品的称取量。
为样品测定时消耗滴定液B的体积(ml),FB为滴定液B的浓度校正因数(mg/ml),TA为滴定液A的滴定度,W为供试品的称取量。
例如,司可巴比妥钠的含量测定:取本品约0.1g,精密称定,置250ml碘瓶中,加水10ml,振摇使溶解,精密加溴滴定液(0.05mol/L)25ml,再加盐酸5ml,立即密塞并振摇1分钟,在暗处放置15分钟后,注意微开瓶塞,加碘化钾试液10ml,立即密塞,摇匀后,用硫代硫酸钠滴定液(0.1mol/L)滴定,至近终点时,加淀粉指示液,继续滴定至蓝色消失,并将滴定的结果用空白试验校正。
已知:司可巴比妥钠的摩尔质量M=260.27;司可巴比妥钠与溴反应的摩尔比为1∶1;供试品的称取量W=0.1022g;硫代硫酸钠滴定液(0.1mol/L)浓度校正因数F=1.038;供试品滴定消耗硫代硫酸钠滴定液15.73ml;空白试验消耗硫代硫酸钠滴定液23.21ml。
溴滴定液(0.05mol/L)的滴定度 ![]()