第四节 血型与输血
一、血型
(一)ABO血型系统
1.分型依据
ABO血型系统的抗原又叫凝集原。根据红细胞膜上A抗原与B抗原的有无和种类而将血液分为四种ABO血型:红细胞膜上只含有A抗原者为A型;只含B抗原者为B型;含有A、B两种抗原者为AB型;A、B两种抗原均无者为O型。
ABO血型系统的血浆中含有两种天然抗体又叫凝集素,分别是抗A抗体和抗B抗体。在A型血的血清中,只含有抗B抗体;B 型血的血清中只含有抗A抗体;AB型血的
血清中无抗体;O型血的血清中含有抗A和抗B两种抗体。在同一个体中,相对抗的抗原和抗体不会同时存在,即其血清中绝不会含有对抗自身红细胞抗原的抗体。
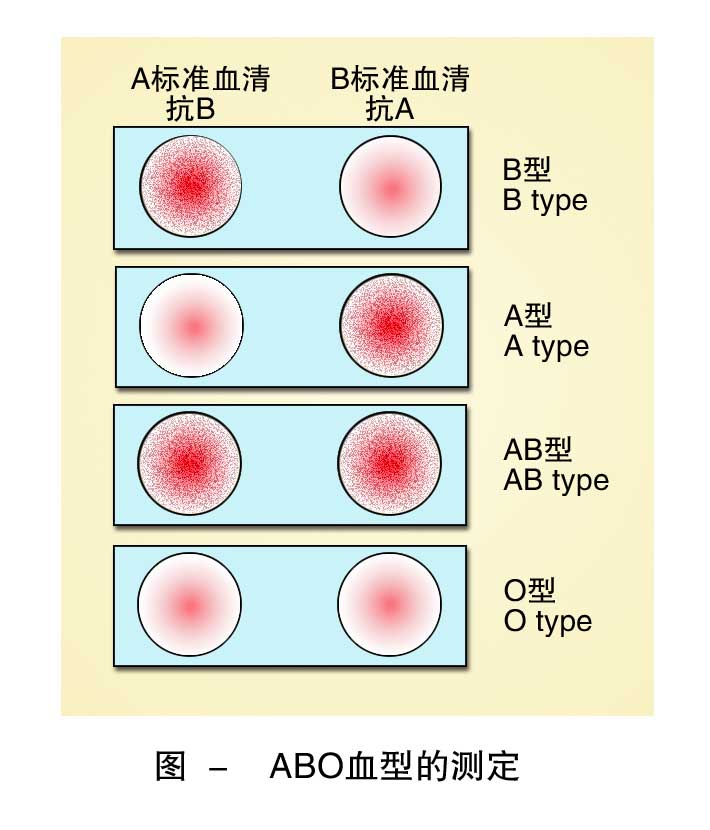
2.凝集反应
红细胞膜上的抗原与血浆中对应的抗体相遇时,红细胞凝集成一簇簇不规则细胞团的现象称为凝集反应(红细胞凝集)。凝集反应的本质是抗原一抗体免疫反应。凝集的红细胞破裂,血红蛋白逸出称为溶血,此即为血型不合时发生的输血反应。
(二)Rh 血型系统
1.Rh血型的分型与特点
人类红细胞膜上还有另一类与ABO血型系统同时存在的Rh 血型系统,因最早发现于恒河猴的红细胞而得名。迄今已发现40多种Rh抗原(也称Rh因子),与临床关系密切的是C、c、D、E、e 五种抗原,其中以D抗原的抗原性最强,故将红细胞上含有D抗原者称为Rh阳性,红细胞上缺乏D抗原者称为Rh阴性。在我国汉族人群中Rh阳性者占99%,Rh阴性者只占1%左右。有些少数民族,Rh阴性者比例较大,如苗族为12.3%,塔塔尔族为15.8%等。Rh血型系统的显著特点是血清中不存在抗Rh抗原的天然抗体。但Rh阴性者在接受Rh抗原刺激后,可以通过体液性免疫产生抗Rh抗体。
2.Rh血型的临床意义
(1)输血反应:Rh阴性者第一次接受Rh阳性血液后,一般不发生输血反应,但却产生了抗Rh抗原的抗体;当再次输入Rh阳性血液后,输入的红细胞将被破坏而发生溶血。
(2)母婴血型不合:Rh血型系统的抗体主要是IgG,分子较小,能透过胎盘。因此,当Rh阴性的母亲孕育Rh阳性的胎儿时,在分娩时Rh阳性胎儿的红细胞或D抗原可进入母体,使母体产生抗D抗体。若再次孕育Rh阳性胎儿,母体内的抗D抗体可进入胎儿体内而引起新生儿溶血,甚至导致胎儿死亡。若在Rh阴性母亲生育第一胎后,及时输注特异性抗D免疫球蛋白,中和进入母体的D抗原,以避免Rh阴性母亲致敏,可预防第二次妊娠时新生儿溶血的发生。
二、输血原则
输血已经成为治疗某些疾病、抢救生命和保证一些手术得以顺利进行的重要手段。但若输血不当或发生差错,就会给病人造成严重损害,甚至引起死亡。为了保证输血的安全和提高输血的效果,必须遵守输血的原则。
(1)血型鉴定:在准备输血时,首先 必须鉴定血型,保证供血者与受血者的 ABO血型相合。对于生育年龄的妇女和 需要反复输血的病人,还必须使供血者 与受血者的Rh血型相合。首先,临床 输血应输同型血。如遇紧急情况必须输 血而又无同型血时,可考虑缓慢、少量 (一般不超过200m1)、严密观察下输入异型血,但异型血相输必须符合供血者的红细胞抗原不被受血者的血清抗体所凝集的原则。
(2)交叉配血试验:即使在血型相同的人之间进行输血,输血前也必须进行交叉配血试验。把供血者红细胞与受血者血清进行混合,称为交叉配血主侧;同时将受血者红细胞与供血者血清进行混合,称为交叉配血次侧。
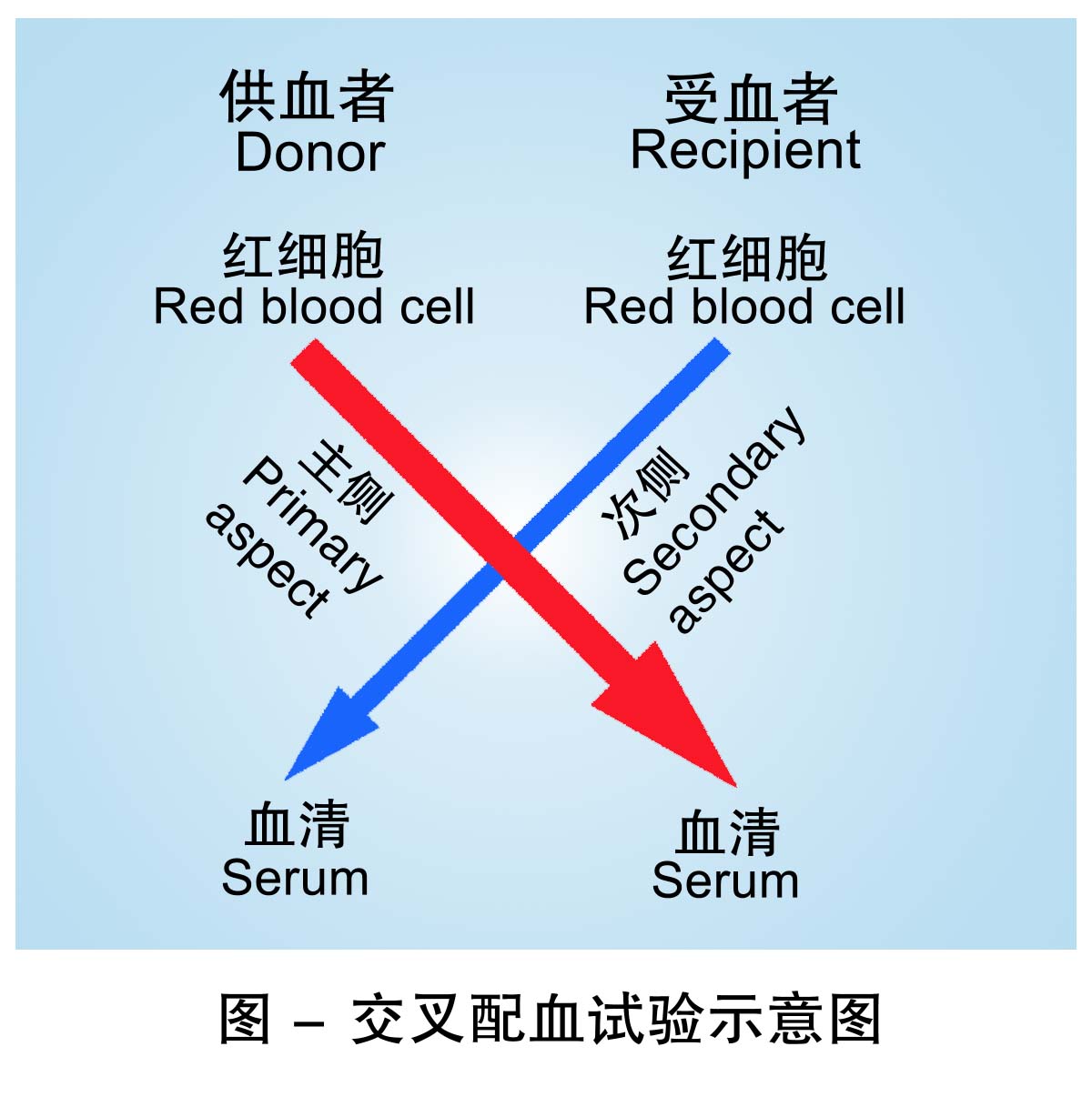
根据交叉配血试验结果判断: 如果两侧 均无凝集反应,即为配血相合,可以进行 输血;如果主侧凝集,为配血不合,禁止 输血;如果主侧不凝集,次侧凝集,称为 配血基本相合,则只能少量、缓慢输血, 并密切观察有无输血反应。
贫血发生的基本机制
贫血(anemia)是指人体外周血红细胞容量减少,低于正常范围下限的一种常见的临床 症状。由于红细胞容量测定较复杂,临床上常以血红蛋白(Hb)浓度和(或)红细胞计数 来代替。WHO 规定,作为正常值观察的人群应该排除营养缺乏患者,排除的方法可以采用 在该人群中预先补充一段时间的营养素(如铁和叶酸等)后再测定血红蛋白浓度和红细胞计 数,或者应用实验室方法排除营养素缺乏者。1972 年 WHO 制订的贫血诊断标准为:在海 平面地区 6 个月到<6 岁的儿童 Hb<110g/L,6~14 岁儿童 Hb<120g/L,成年男性 Hb< 130g/L,成年女性 Hb<120g/L,孕妇 Hb<110g/L,海拔每升高 1000 米,血红蛋白上升 4%。 在我国由于缺乏规范的健康正常者血液参数值的普查资料,无法按照 WHO 的标准方法获得 血红蛋白浓度和红细胞计数的正常值,通常认为海平面地区,成年男性 Hb<120g/L,成年 女性(非妊娠)Hb<110g/L,孕妇 Hb<100g/L就可诊断为贫血。红细胞生成减少、红细胞 破坏过多或失血过多均可引起贫血。 值得指出的是,由于某种原因导致血浆容量增加时,此时即使红细胞容量是正常的,但 因血液被稀释,血红蛋白浓度和红细胞计数降低,容易被误诊为贫血;而在脱水或失血等循 环血容量减少时,由于血液浓缩,即使红细胞容量偏低,但因血红蛋白浓度增高,贫血容易 被漏诊。
一、红细胞生成减少性贫血 造血细胞、骨髓造血微环境、造血原料或造血调控的异常均可影响红细胞生成,导致红 细胞生成减少。
(一)造血干祖细胞异常所致贫血——再生障碍性贫血 再生障碍性贫血(简称再障,aplastic anemia)是骨髓造血功能衰竭综合征,其病因不 明,主要表现为骨髓造血功能低下,全血细胞减少和贫血、出血、感染等症。再障发生机制 尚未完全阐明,可能与下列因素有关。 1.造血干祖细胞数量减少和缺陷 许多研究显示,再障患者骨髓造血干祖细胞(CD34+ 细胞)数量明显减少(可能仅为正常人的 1%),减少程度与病情相关。再障患者的造血干 祖细胞集落形成能力显著降低,体外对造血生长因子(HGFs)的反应差,DNA修复能力降 低。这些结果表明造血干祖细胞不仅数量减少,也存在内在缺陷。 2.造血微环境异常 再障患者骨髓活检除发现造血细胞减少外,部分患者还有骨髓“脂 肪化”、静脉窦壁水肿、出血、毛细血管坏死,以及骨髓基质细胞体外培养生长情况差,分 泌的各类造血调控因子明显不同于正常人。若骨髓基质细胞受损的再障患者在接受造血干细 胞移植时不易成功。 3.异常免疫反应损伤造血干细胞 多数患者采用免疫抑制治疗后其自身造血功能可能 得到改善,而异体骨髓移植治疗重型再障前需要免疫抑制及预处理,这表明免疫异常参与再 障的发生。研究显示,再障患者外周血及骨髓淋巴细胞比例增高,T细胞亚群失衡,T辅助 细胞I型(Th1)、 CD8+T抑制细胞、CD25+T细胞和γδTCR+T细胞比例增高。T细胞分泌的造 血负调控因子(IFN-γ、TNF)明显增多,髓系细胞凋亡亢进。细胞毒性T细胞分泌穿孔素直接杀伤造血干细胞而使髓系造血功能衰竭。 过去认为,在一定遗传背景下,再障可能通过三种机制发病:原发、继发性造血干祖细 胞(种子)缺陷、造血微环境(土壤)及免疫(虫子)异常。近年来认为再障发病的主要机 制是免疫异常。T 细胞功能异常亢进,细胞毒性 T 细胞直接杀伤和淋巴因子介导的造血干细 胞过度凋亡引起的骨髓衰竭是再障的主要发病机制。造血微环境与造血干祖细胞量的改变是 异常免疫损伤的结果。
(二)造血微环境异常所致贫血 造血微环境包括骨髓基质,基质细胞和细胞因子。 1.骨髓基质和基质细胞受损所致贫血 骨髓坏死、骨髓纤维化、骨髓硬化症、各种髓 外肿瘤性疾病的骨髓转移以及各种感染或非感染性骨髓炎,均可因损伤骨髓基质和基质细 胞,造血微环境发生异常而影响血细胞生成。 2.造血调节因子水平异常所致贫血 干细胞因子(stem cell factor, SCF)、白细胞介素 (IL)、粒 -单系集落刺激因子(GM-CSF)、粒系集落刺激因子(G-CSF)、红细胞生成素 (EPO)、血小板生成素(TPO)等具有促进造血的作用,而肿瘤坏死因子(TNF)和干扰 素(IFN)等对造血具有负调控作用。EPO 是促进红细胞生成最重要的因子。肾脏是 EPO 生成的最主要部位,肾脏病变时可因 EPO 生成不足而引起肾性贫血。肿瘤性疾病或某些病 毒感染会诱导机体产生较多的造血负调控因子如 TNF、IFN 等炎症因子等,均可导致慢性病 性贫血(anemia of chronic disease, ACD),也称炎症性贫血(anemia of inflammation, AI)。此 外,慢性病性贫血患者对 EPO 刺激的敏感性降低。
(三)造血原料不足所致贫血 造血原料是指造血细胞增殖、分化、代谢所必需的物质,如蛋白质、脂类、维生素(叶 酸、维生素B12等)、微量元素(铁、铜、锌等)等。任一种造血原料不足都可能导致红细胞 生成减少。其中缺铁和叶酸、维生素B12缺乏是常见的造血原料不足所致贫血的类型。 1.缺铁性贫血 缺铁性贫血(iron deficiency anemia)是临床上最常见的贫血。缺铁或 铁的利用障碍可影响血红素的合成,导致血红蛋白的合成减少,属于血红素合成异常性贫血。 由于缺铁对细胞的分裂、增殖影响较小,故红细胞数量减少程度不如血红蛋白减少明显,从 而形成小细胞低色素性贫血,红细胞形态变小,中央淡染区扩大。 此外,由于多种酶含铁(如细胞色素 C、单胺氧化酶、核糖核苷酸还原酶、琥珀酸脱氢 酶等),缺铁时这些含铁酶的活性减低。由于这些含铁酶与生物氧化、组织呼吸、神经递质 分解与合成有关,故铁缺乏时造成细胞功能紊乱,甚至造成重要的神经介质如 5-羟色胺、 去甲肾上腺素、肾上腺素及多巴胺发生明显变化,产生一系列非造血系统的表现,如体力减 弱、易疲劳、表情淡漠、注意力难于集中、注意力减退和智力减低等。 2.巨幼细胞性贫血 由于各种生理或病理因素导致机体叶酸或维生素B12绝对或相对缺 乏或利用障碍可引起的巨幼细胞贫血(megaloblastic anemia)。叶酸在维生素B12的作用下经 叶酸还原酶的催化变成活性形式N5, N10-亚甲FH4,后者是DNA合成过程中必需的辅酶,为 胸苷酸合成酶催化dUMP甲基化形成dTMP提供一碳基团,继而形成dTTP。由于叶酸缺乏, dTTP形成减少,DNA合成障碍,DNA复制延迟。因RNA合成所受影响不大,细胞内RNA/DNA 比值增大,造成细胞体积增大,胞核发育滞后于胞浆,形成巨幼变。骨髓中虽然各阶段的巨 幼红细胞增多,但许多未能发育成熟即遭到破坏。由于红细胞生成速度慢,进入血循环的红细胞寿命缩短(为正常的 1/2~1/3),从而出现贫血。此外,骨髓中除红系外,粒系和巨核 系细胞均可发生巨幼变,分化成熟异常,在骨髓中过早死亡,导致无效造血和全血细胞减少。 因此,无论是叶酸还是维生素B12缺乏均可引起巨幼细胞贫血。 此外,L-甲基丙二酰-CoA变位酶和甲硫氨酸合成酶的催化作用也需要维生素B12的参 与。L-甲基丙二酰-CoA变位酶催化反应障碍导致神经髓鞘合成障碍,而甲硫氨酸合成酶催 化反应障碍引起神经细胞甲基化反应受损。因此,VitB12缺乏还可引起神经系统症状。
二、红细胞破坏过多所致贫血——溶血性贫血 溶血(hemolysis)是红细胞遭到破坏,寿命缩短的过程。由于溶血超过骨髓的代偿能力 引起的贫血即为溶血性贫血(hemolytic anemia,HA)。骨髓具有正常造血 6~8 倍的代偿能 力,溶血发生而骨髓能够代偿时,可无贫血,称为溶血性疾病。
(一)红细胞自身异常导致溶血性贫血 1.遗传性红细胞膜异常——遗传性球形红细胞增多症 遗传性球形红细胞增多症 (hereditary spherocytosis, HS)患者存在遗传性红细胞膜缺陷。由于调控红细胞膜蛋白的基 因突变造成膜骨架蛋白(膜收缩蛋白、锚蛋白)单独或联合缺陷而造成:①红细胞膜双层脂 质不稳定,以出芽形式形成囊状而丢失,使红细胞表面积减少,表面积与体积比值下降,红 细胞变成球形,可塑变形性降低;②红细胞膜对阳离子通透增加,Na+和水进入胞内而K+透 出胞外,为维持红细胞内外Na+平衡,钠泵活动加强,ATP消耗增多,钙泵活动受抑,导致 细胞内Ca2+浓度升高并沉积在红细胞膜上,使膜的柔韧性降低。红细胞通过脾时易被破坏而 溶解,发生血管外溶血。 2.遗传性红细胞酶缺乏——葡萄糖-6-磷酸脱氢酶(G-6-PD)缺乏症 葡萄糖-6-磷酸 脱氢酶(G-6-PD)缺乏症是由于调控 G-6-PD 的基因突变所致。G-6-PD 是磷酸戊糖旁路 中催化 6-磷酸葡萄糖(G-6-P)转变为 6-磷酸葡萄糖酸(G-6-PG)反应所必需的酶。G-6-PD 缺乏时,将使 NADPH 减少,不能细胞内还原型谷胱甘肽(GSH)的生理浓度,从而使红细 胞膜蛋白和酶蛋白中的巯基遭受氧化,破坏了红细胞膜的完整性。NADPH 减少后,使高铁 血红蛋白(MHb)不能转变为氧合血红蛋白,MHb 的增加导致红细胞内还可溶性变性珠蛋 白小体(Heinz body)形成明显增加。Heinz 小体大多分布在红细胞膜上,通过脾脏时被破 坏这些红细胞极易被脾索阻滞而被单核巨噬细胞所吞噬。G-6-PD 缺乏者在服用氧化性药物 (如伯氨喹啉)常诱发溶血。 3.遗传性珠蛋白生成障碍——镰状细胞贫血 血红蛋白是一种由血红素和珠蛋白组成 的结合蛋白。珠蛋白有两种肽链,一种是 α 链,由 141 个氨基酸残基构成;另一种是非 α 链(包括 β、γ 及 δ 链),各有 146 个氨基酸残基,各种肽链有固定的氨基酸排列顺序。每一 条肽链和一个血红素连接,构成一个血红蛋白单体。人类血红蛋白由 2 对(4 条)血红蛋白 单体聚合而成。正常成人血红蛋白主要为血红蛋白 A(HbA)。镰状细胞贫血因 β 珠蛋白链 第 6 位谷氨酸被缬氨酸替代所致,又称血红蛋白 S(HbS)病。由于 HbS 在缺氧情况下分子 间相互作用,成为溶解度很低的螺旋形多聚体,使红细胞扭曲成镰状细胞(镰变)。这类细 胞变形性差,在微循环内易被淤滞而破坏,发生溶血性贫血。
(二)红细胞外部异常导致溶血性贫血 1.免疫性溶血性贫血 如血型不符的输血反应、新生儿溶血病等同种免疫性溶血病。 2.血管性溶血病 如在长途步行过程中由于脚底血管壁受到反复挤压导致红细胞血管内机械破坏增加引起行军性血红蛋白尿。 此外,蛇毒、疟疾、等生物因素也可引起红细胞大量破坏。
三、失血性贫血 当失血速度大于红细胞生成速度时,外周血红细胞数目减少,血红蛋白浓度降低而引起 失血性贫血。根据失血速度分急性和慢性,慢性失血性贫血往往合并缺铁性贫血。可分为出 凝血性疾病(如特发性血小板减少性紫癜、血友病和严重肝病等)所致和非出凝血性疾病(如 外伤、肿瘤、结核、支气管扩张、消化性溃疡、痔和妇科疾病等)所致两类。
自体输血的研究进展与前景
Research Progress and Prospects of Autologous Blood Transfusion
毛小红
摘要:目的 简述自体输血国内外的发展状况。方法 参阅国内外有关自体输血的有关文献, 对自体输血的研究进展与前景进行综述。结果 自体输血已广泛应用于骨科、大血管外科、 心脏外科、神经外科、妇产科等临床领域,并对凝血及免疫功能有一定影响。结论 自体输 血对机体有许多优点,已成为输血工作的发展方向之一。
关键词:自体输血;机体功能;进展
自体输血是指采集受血者自身血液,或回收手术野或创伤区无污染的血液,以满足病人 自身手术或将来应急情况用血需求。它有 3 种形式:贮存式自体输血、稀释式自体输血和回 收式自体输血。1886 年首次出现,到 1921 年成为临床上可接受的输血,随后在临床上应用 越来越广泛,发展到现在,自体输血已经成为输血工作的重要发展方向之一。自体输血在国 外已得到广泛应用,德国临床上的术前存血率已达 89%,澳大利亚择期手术患者约 60%输 的是自体血,美国有的医院输自体血量已占总用血量的 15%左右[1]。在我国自体输血开展 越来越广泛,1978 年上海第二医科大学第三附属医院麻醉科报告了血液稀释式和自体输血 150 例,1979 年天津、上海血液中心先后发表了同类报告,1989 年中国医学科学院阜外医 院输血科报告了心血管外科手术稀释与自体输血 100 例,我国在一些大城市、中心医院已开 展自体输血,取得良好效果。近年来,特别是我国 1998 年 10 月 1 日实施的《中华人民共和 国献血法》第 15 条规定:国家提倡并指导择期手术的患者自身储血、自身输血,自体输血 受到空前重视。本文就自体输血的优点以及对机体凝血功能、免疫功能的影响综述如下。
1.自体输血的优点
相对异体输血而言,自体输血有着不可比拟的优越性,其优点如下:①用血安全,没有 传播艾滋病、疟疾、梅毒、肝病、巨细胞病毒等血液传染性疾病的危险。②可以避免因输入 异体血液可能导致的溶血反应、发热及过敏。还可避免移植物的抗宿主反应,避免受血者因 输入异体血液而导致的免疫功能下降,有文献认为异体输血可引起免疫抑制,使术后感染(尿 路感染、肺炎、菌血症等)发生率升高[2]。③回输的自体血液新鲜,其携氧功能、凝血功 能都大大优于库存异体血。④进行自体输血的患者,由于需反复抽血,可以刺激骨髓造血细 胞活力,使患者术后的造血速度加快,有利于身体康复。⑤可以缓解目前用血紧张的状况, 解决某些稀有血型如Rh阴性血型者供血问题。⑥扩大血源,减少患者经济开支,提供安全 用血。有文献报道的使用自体引流血回输可减少 50%~90%异体血输入[3]。⑦自体血的储 存时间较短,其各项生化指标比较接近机体本身,因此输血后发生代谢性酸中毒、低钙血症、 高钾血症的可能性非常低。
2.自体输血对机体功能的影响 自体血在回收、回输过程中,血液中的血小板于回收的过程中因负压吸引及机械性损伤 而破坏,或降低其生理功能,其他凝血因子如纤维蛋白原因出血及与组织接触而耗损,以及 大量输入回收自体血或血液稀释均可引起凝血因子减少或失活,或抗凝剂用量不当等,理论 上会导致机体凝血功能障碍。但这并不绝对,Laub[4]等采用随机单盲设计的试验方法,发 现回收式自体输血组患者术后 1d血小板数量从术前 267.9 × 109 /L 下降到 160.8 × 109 /L,凝 血酶原时间(Pr)和部分凝血激酶时间均较术前延长,然而临床上没有观察到术后出血增加 的现象。Kalra等[5]报道术中进行自体回输血后,Hb、Hct虽较术前下降但都没有统计学意 义;血小板数量在术后 4h和 24h均明显下降,PT显著延长,PTT变化不明显,血浆纤维蛋白 原(FIB)水平术后 4h显著下降,但 24h后恢复至术前水平,全身循环中的肝素含量极低; 所有患者术后均没有出血并发症;生化检查发现术后 24h胆红素水平升高,但在正常范围内; Ca2+浓度和总蛋白术后 4h和 24h明显下降;尿素、肌酐及肝酶水平变化不明显,说明术后肝 肾功能无异常。尽管如此,Horst等[6]还是认为回输自体血超过 15h时,需仔细监测凝血指 标。
也有认为,当回输自体血超过约 3 000mL时,应认真监测凝血指标,补充血浆,必要时 加输血小板。 自体输血还对手术患者免疫功能存有影响。孙艳红等[7]研究发现异体输血组术后 2d病 人血浆中有免疫增强作用的IL−2 与术前相比明显下降,自体血回输组IL−2 与术前比较稍低 但无统计学差异,同时,异体输血组IL−6 升高没有自体输血组明显,表明自体血回输组对 免疫功能抑制不明显。此外,自体血回输组和不输血组CD3+ T、CD4+ T、CD8+ T、CD4+/CD8+ 比值在术后 2d、术后 7d与术前比较两组间无明显差异,而异体输血组CD3+ T、CD4+ T、 CD8+ T在术后 2d与术前及其他两组比较明显下降,表明自体血液回输对病人的T细胞免疫功 能影响较小。Jacobi等[8]在回收血中检测到高浓度的C3a、TNFα、IL−1β、IL−6、IL−8,但 也有资料用ELISA法测定自体血回输后患者IL−2、IL−6 的变化,结果显示术后 2d IL−2 较术 前稍降低,但无统计学差异,术后 7d有所回升;IL−6 术后 2d较术前显著升高,术后 7d仍有 统计学差异;异体输血组术后 2d IL−2 明显下降,IL−6 升高不如自体输血组显著。正常生理 状态下,IL−2 表现免疫增强作用,IL−6 除有免疫增强和促进造血作用外,还能提高炎症时 机体的非特异免疫功能,说明自体输血对患者的免疫功能影响较小;而TNFα可刺激花生四 烯酸类炎性物质的释放,IL−8 可诱使中性粒细胞脱颗粒,释放过量的溶酶体及其他炎性物质,在增强中性粒细胞杀菌作用的同时也造成机体损害,两者均可诱发多器官功能衰竭。 Goldie等[9]证实,利用IL−1 受体的拮抗剂可拮抗IL−1 的致炎作用,改善患者的预后。Heiss 等[10]研究发现,不输血的手术病人,术后 3d,NK和LAK细胞活性下降,8d下降更明显; 异体输血组NK和LAK细胞活性抑制更重、时间更长,自体输血组在术后 8d,NK细胞活性 显著高于手术前水平,LAK细胞活性较术后 3d明显回升,表明自体输血可调节手术创伤和 麻醉引起的NK细胞和LAK细胞的活性抑制。他们对结肠癌病人输自体血和异体血后体内不 同炎性介质的变化进行了研究,结果表明可溶性TNF受体(免疫抑制指标)只有异体输血组 术后升高而自体输血组未升高。IL−10(细胞免疫抑制指标)在异体输血组和未输血组术后 均立即升高,而自体输血组未升高。上述结果支持自体输血能够调节由手术创伤和麻醉引起 的细胞免疫抑制。 自体回收血中常存在的脂肪滴、纤维蛋白、血小板或细胞、白细胞团等,这些物质易于 形成微小的栓子。当大量输入未经滤过的血液可引起广泛的肺微血管栓塞,引起严重的低氧 血症。自体输血还可能造成肿瘤细胞扩散、高氯性酸中毒等症状。
自体输血已广泛地应用于骨科、大血管外科、心脏外科、神经外科、妇产科等临床领域, 它能有效地防止感染性疾病传播,不仅可以避免异体输血所致的各种输血后合并症的发生, 而且可以节约血源,弥补血源不足,解决某些稀有血型如Rh阴性血型者供血问题,同时, 减少患者医疗经费开支,具有深远的社会意义和经济意义。总之,自体输血有诸多优点,也 有其可能存在的缺点,如Jurkorich[11]提出的自体输血分析、德国学者Rosolakit[12]对自体输 血回收血液的分析,在临床应用上并不能也不可能完全代替异体输血。二者各有优缺点和适 应证,具体应用时应根据实际的临床情况来决定。但是,自体输血已经体现出了它的优越性, 成为今后输血工作的发展方向之一,我们有理由相信自体输血在临床上的应用将越来越广 泛,这一临床治疗研究领域必将结出更丰硕的科学成果。




