-
1
-
2 测验

抗病原微生物药(antimicrobial drugs)是指对病原微生物有抑制或杀灭作用,用于防治病原微生物感染性疾病的药物。包括抗菌药、抗病毒药、抗真菌药、抗结核药等。属于化疗药。
抗病原微生物药与化学治疗学
化学治疗学(chemotherapy, 化疗):病原微生物、寄生虫及癌细胞所致疾病的药物治疗。
化疗药:用于治疗病原微生物、寄生虫及癌细胞所致疾病的药物。包括
化疗药物 :
抗病原微生物药(antimiczobial drug)
抗寄生虫药(antiparasitic drug)
抗癌药(anticancer drug)
生活中多数人理解有差异。经常神神秘秘的说:“XX正在化疗,可能是得了癌症。”其实,不一定。我们患有急性扁桃体炎、肺炎或者胃肠道感染时的药物治疗都是化疗。
病原微生物
(细菌、病毒、放线菌、真菌、立克次体、衣原体、支原体、螺旋体)感染性疾病遍布临床各科,其中细菌性感染最常见,抗菌药也就成为应用最广泛的抗病原微生物药。

抗菌药
指对病原菌有抑制或杀灭作用的药物。包括抗生素、人工合成抗菌药。
抗生素(Antibiotics)
是由细菌、真菌或其他微生物在代谢过程中所产生的具有抗病原体或其他活性的一类物质
应用抗病原微生物药治疗感染性疾病的过程中,应注意机体、病原体、药物三者间的相互关系,病原体的致病性对感染性疾病的发生起着重要作用,但病原体并不能决定疾病发展的全过程,机体的抗病性是战胜病原体,使其不能致病或发病后迅速康复的机体内在因素,抗病原微生物药的应用为机体彻底消灭病原体,促进疾病痊愈提供了有力武器。选择使用时,必须在恢复和提高机体防御功能的前提下,充分利用药物的体内过程发挥药物的治疗作用,同时防止细菌耐药性的产生,并尽量避免和降低药物对机体不良反应的发生。
相关术语
a. 抗菌谱(antibacterial spectrum)
窄谱抗菌药:单一菌种、单一菌属
广谱抗菌药:多数G+、G-菌,衣原体、支原体、立克次体、螺旋体、原虫等
b. 抗菌活性(antibacterial activity)
抑菌药:仅抑制病原菌生长繁殖无杀灭作用
杀菌药:不仅抑制并能杀灭病原菌
用最低抑菌浓度、最低杀菌浓度评价抗菌活性
最低抑菌浓度(MIC):指体外抗菌实验中,抑制供试细菌生长的抗菌药物的最低浓度
最低杀菌浓度(MBC):指体外抗菌实验中,杀灭供试细菌的抗菌药物的最低浓度
c.抗生素后效应(post antibiotic effect,PAE)
是指细菌与抗菌药短暂接触后,当抗菌药的血药浓度降至最低抑菌浓度以下,细菌的生长繁殖仍受到持续抑制的现象。
——评价抗菌药物活性的重要指标
几乎所有抗菌药物都有不同程度的抗生素后效应
d.安全性指标
化疗指数(chemotherapeuticindex, CI)
CI=LD50/ED50

抗菌作用机制
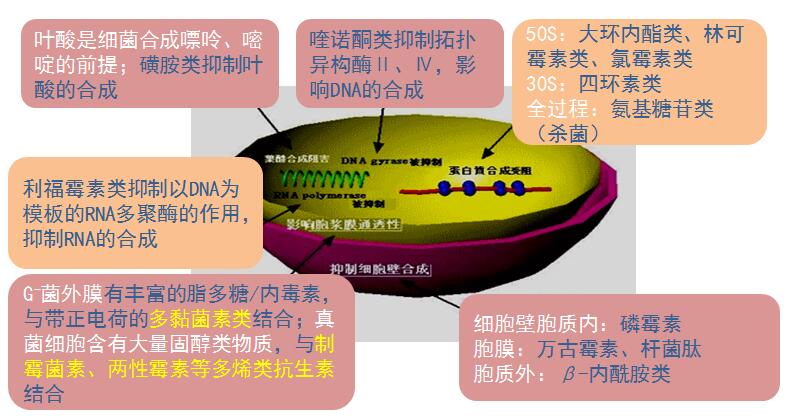
包括:
1. 抑制细胞壁的合成
2. 影响胞浆膜通透性
3.影响胞浆内生命物质的合成:
①抑制蛋白质合成
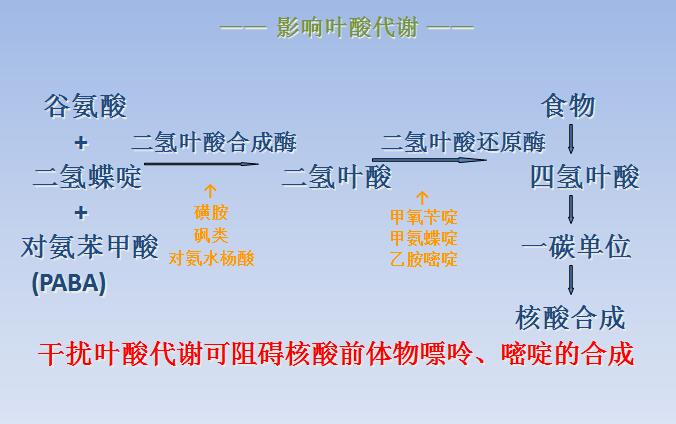
②影响叶酸代谢
③抑制核酸合成
抑制细胞壁合成
细菌最外层是致密而坚韧的细胞壁,不但能保持细菌的外形,还能抵抗菌体内外强大的渗透压,具有保护和维持细菌正常形态的功能。G+细菌细胞壁主要结构成分是黏肽,青霉素类、头孢菌素类、万古霉素等通过影响黏肽合成的不同环节阻碍细菌细胞壁合成,导致新生细菌细胞壁缺损。受菌体内的高渗透压的影响,水分不断渗入,致使细菌膨胀、变形,同时激发自溶酶活性,使细菌破裂溶解而死亡。
增加胞浆膜通透性
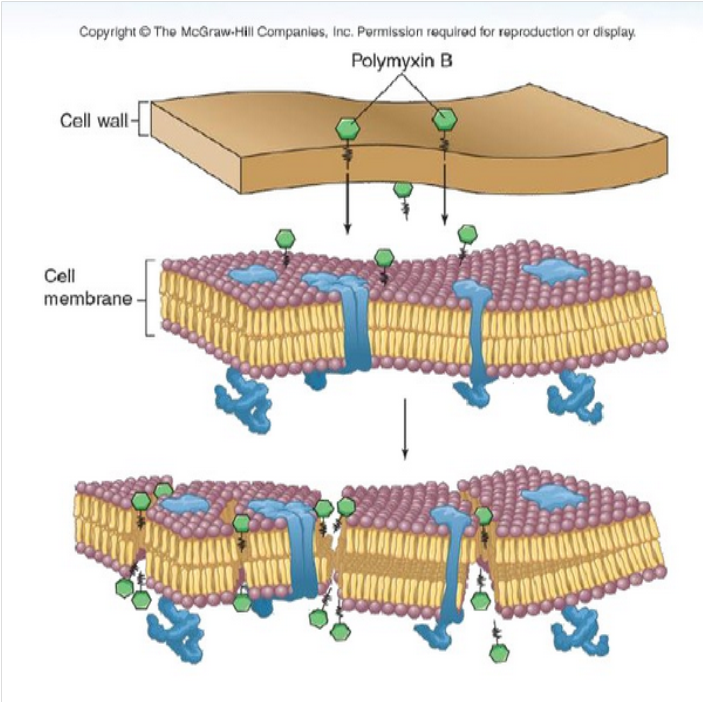
细菌胞浆膜主要是由类脂质和蛋白质分子构成的一种半透膜,具有渗透屏障和运输物质的功能。多粘菌素类抗生素为阳离子型表面活性剂,能选择性地与细菌胞浆膜中的磷酯结合;
而制霉菌素和两性霉素B等能与真菌胞浆膜中固醇类物质结合。它们均能使胞浆膜通透性增加,导致菌体内的蛋白质、核苷酸、氨基酸、糖和盐类等重要物质外漏,从而使细菌死亡。
抑制菌体蛋白质合成
细菌为原核细胞,其核蛋白体为70S,由30S和50S亚基组成,多种抗生素能抑制细菌的蛋白质合成。
①大环内酯类抗生素、氯霉素、林可霉素能与细菌核蛋白体50S亚基结合,使蛋白质合成呈可逆性抑制
②四环素能与核蛋白体30S亚基结合,使肽链的形成与延伸受阻而抑制蛋白质合成。
③氨基甙类抗生素主要作用部位是30S亚基结合,影响蛋白质合成的全过程,因而具有杀菌作用。
哺乳动物是真核细胞,其核蛋白体为80S,由40S与60S亚基构成,因而它们的生理、生化与功能不同,抗菌药物对细菌的核蛋白体有高度的选择性毒性,而不影响哺乳动物的核蛋白体和蛋白质合成。
药物对病原微生物抑制、杀灭的过程中,细菌不可能“坐以待毙”,也会通过各种途径来对药物产生抵抗作用,耐药性就是他们“绝处逢生”的具体表现。
耐药性(resistance)及机制
耐药性(resistance):连续用药后病原体及肿瘤细胞等对化学治疗药物的敏感性降低,需增加剂量才能恢复原效应,称耐药性,又叫抗药性。
区分耐受性
交叉耐药(Cross Resistance):病原体对某种药物耐药后,对于结构相似或作用机理相同的药物也耐药,称之为交叉耐药。根据程度的不同,又有完全交叉耐药和部分交叉耐药之分。
耐药性可分为固有耐药性和获得耐药性
固有耐药
又称天然耐药性,是由细菌染色体基因决定、代代相传,不会改变的,如链球菌对氨基糖苷类抗生素天然耐药;肠道G-杆菌对青霉素天然耐药;铜绿假单胞菌对多数抗生素均不敏感。
获得性耐药性
是由于细菌与抗菌药接触后敏感性降低或消失,多数由质粒介导。如金黄色葡萄球菌产生β-内酰胺酶而耐药。细菌的获得性耐药可因中断与抗菌药接触而消失,也可由质粒将耐药基因转移给染色体而代代相传,成为固有耐药。
曾经抗生素被视为伤员的“续命剂”,如今却成为“超级细菌”的助力器。
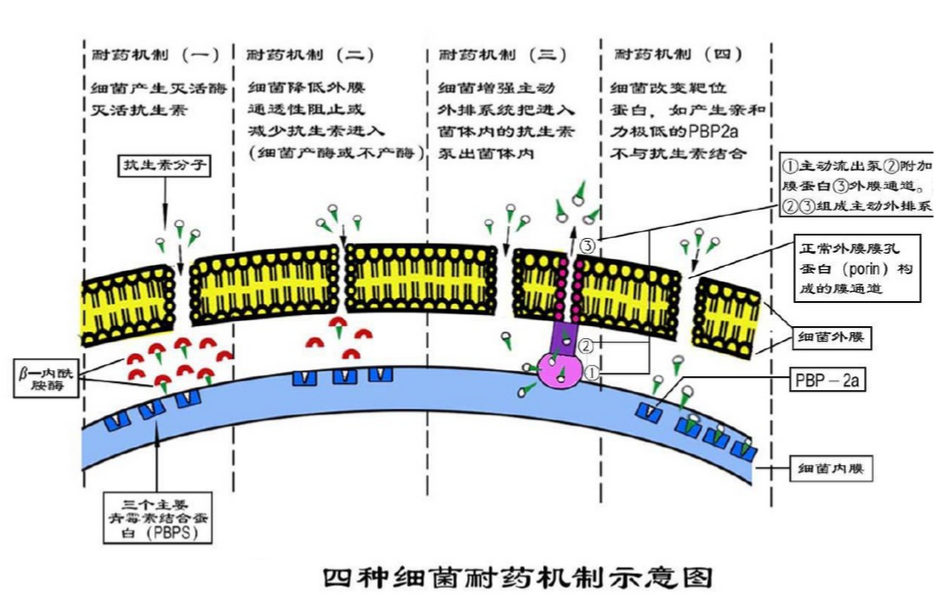
耐药性机制
1.产生灭活酶细菌产生灭活抗菌药物的酶,使抗菌药物失活是耐药性产生的最重要机制之一 。
2.改变药物靶位结构
3.降低胞浆膜通透性
4.主动转运泵作用
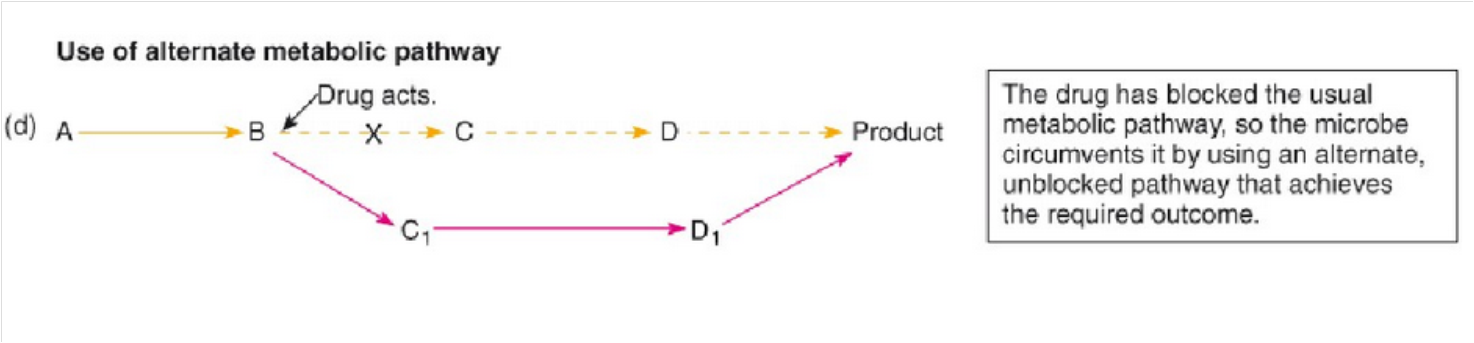
5.改变代谢途径
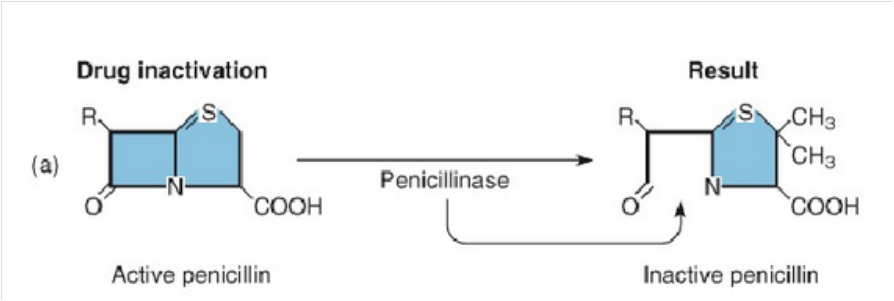
产生灭活酶:
使抗菌药物作用于细菌之前即被酶破坏而失去抗菌活性。
(1)水解酶:如β-内酰胺酶可使青霉素类、头孢菌素类的β-内酰胺环裂解,药物结构破坏而失效。
(2)钝化酶:细菌在接触到氨基苷类抗生素后产生钝化酶如乙酰化酶、腺苷化酶和磷酸化酶等,可以将乙酰基、腺苷酰基和磷酰基连接到氨基苷类的氨基或羟基上,使氨基甘类的结构改变而失去抗菌活性。
改变药物作用靶位:
细菌改变了与抗生素结合部位的靶蛋白,使该部位发生结构或位置的变化,使抗生素不能与靶位结合,导致耐药性的产生。如肠球菌对β-内酰胺类的耐药性是既产生β-内酰胺酶又增加青霉素结合蛋白的量,同时降低青霉素结合与抗生素的亲和力,形成多重耐药机制。
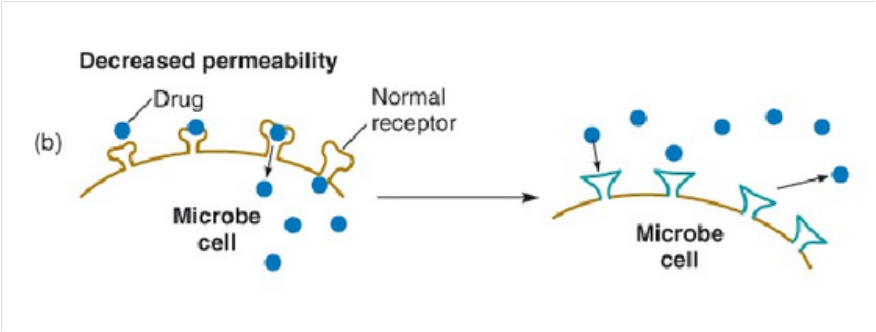
改变细菌外膜通透性:
细菌接触抗生素后,可以通过改变通道蛋白性质和数量来降低细菌的膜通透性,导致药物进入菌体内减少而产生获得性耐药性。很多广谱抗菌药都对铜绿假单胞菌无效或作用很弱,主要是抗菌药物不能进入铜绿假单胞菌菌体内,故产生天然耐药。
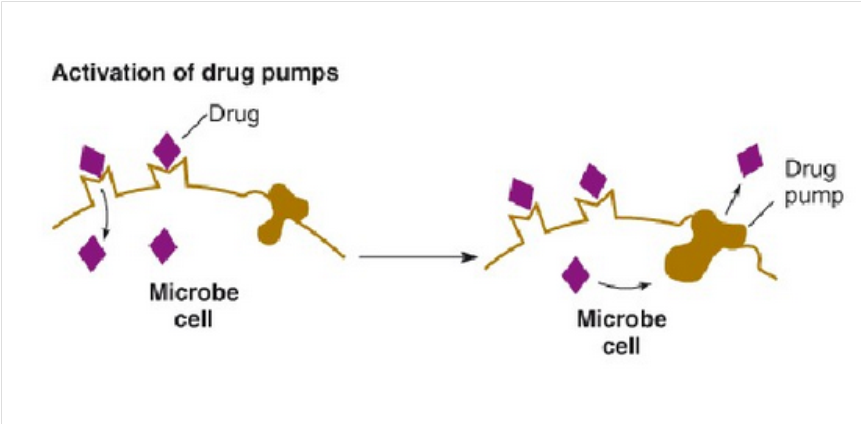
主动转运泵作用:
某些细菌能将进入菌体的药物泵出体外,这种泵因需能量,故称主动转运泵(或主动流出系统)。由于这种主动转运泵的存在使药物在菌体内的浓度降低而出现耐药性。
改变代谢途径:
细菌对磺胺类抗菌药的耐药性可能与细菌改变叶酸代谢途径,通过产生大量的PABA,或者利用外源性叶酸生成二氢叶酸有关。
抗菌药合理使用的话,是细菌的“克星”。如若滥用,细菌对抗药物化身成为“超级细菌”。
超级细菌
超级细菌的可怕之处并不在于它对人的杀伤力(不会产生新的疾病),而是它对普通抗菌药物的抵抗能力,导致被感染者“无药可救”。世卫组织称:感染“超级细菌”患者的死亡率大约是感染不耐药细菌患者的两倍。另有专家预测,按照目前的态势,新的“超级细菌”还会陆续出现,10—20年内,现在所有的抗生素对它们都将失去活性。
感染“超级细菌”距离死神就更近一步,打败、跑赢“超级细菌”的关键是规范用药。
2016年8月25日,正式公布了由国家卫生计生委等14部门联合制定的《遏制细菌耐药国家行动计划(2016-2020年)》。
预防措施
1.合理使用抗生素。防止滥用抗生素,是预防超级病菌流行的最重要的手段。公众对抗生素的使用要坚持“四不”原则:不随意买药、不自行选药、不任意服药、不随便停药。
2.注意个人卫生,尤其是正确洗手。
3.避免细菌感染。如果去医院探视耐万古霉素肠球菌(VRE)感染的患者,应听从医院有关人员的指导,做好消毒、隔离工作,避免因探视而感染此种疾病。
4.提高机体的抵抗力。 由于“超级细菌”难以治疗,自身免疫力是最好武器,对付它最好的办法是防御。加强身体锻炼,合理膳食,注意休息。
展望
美国科学家在2015年发现的新型抗生素Teixobactin,可杀死耐甲氧西林金黄色葡萄球菌MRSA、耐万古霉素肠球菌VRE、结核分枝杆菌等多种致命的病原体;不会诱发耐药。
中新网2016年9月13日电 据澳洲日报报道,墨尔本大学的华裔女博士和她的团队研发的星形蛋白质分子链“结构纳米工程抗菌肽聚合物——SNAPP”在对抗耐抗生素的超级细菌方面取得重大突破,通过“撕裂”细菌细胞壁杀死细菌,毒性低,有望用于临床。

因此,合理使用抗病原微生物药不仅可杀灭病原微生物、控制感染,而且可以有效降低药物不良反应对机体健康的危害,同时还可延缓细菌耐药性、防止药物治疗失败。