§1–2 分析方法的分类
一、分类
可以按照分析任务、对象、测定手段等来进行分类
1. 任务 定性分析:有没有
定量分析:有多少
结构分析:存在形式
2. 对象 无机分析:元素种类多,结构简单。通常只要求测定元素、离子、化合物的种类以及它们的相对含量(定性、定量)
有机分析:组成元素简单(C、H、O、N、P、S),但结构复杂,因此,除了作元素分析外,还需要作官能团和结构分析(定性、定量、结构)
3. 手段 化学分析:以化学反应为基础建立起来的分析方法。
仪器分析:借助光电仪器,通过测量试样溶液的光学性质、电学性质等物理或物理化学性质来求出待测组分含量的方法。
4. 试样用量多少 分为常量、半微量和微量分析方法。
常量分析 半微量分析 微量分析 超微量分析
(液体) >10ml 10~1ml 1~0.01ml <0.01ml
(固体) >100mg 100~10mg 10~0.1mg <0.1mg
5. 待测组分含量多少 常量组分分析 微量成组分分析 痕量组分分析
>1% 0.01~1% <0.01%
6. 工作性质 例行分析(日常分析) 仲裁分析(裁判分析)
二、化学分析法与仪器分析法
1 化学分析:以物质的化学反应为基础的分析方法,又分为重量分析法和滴定分析法
(1)重量分析法:通过化学反应及一系列操作步骤将试样中的待测组分转化为另一种纯粹的、具有固定化学组成的化合物,然后通过称量该化合物的质量求出待测组分的含量。
(2)滴定分析法:将已知浓度的溶液,滴加到待测溶液中,使其与待测组分发生反应,直到待测组分恰好完全反应,根据加入试剂的浓度和加入的准确体积,计算出待测组分的含量,这样的分析方法称为滴定分析法(又称容量分析法)。
依据反应类型的不同,滴定分析法又分为酸碱滴定法、配位(络合)滴定法、沉淀滴定法、氧化还原滴定法。
(3)滴定分析与重量分析的异同点:
共同点:适于测定高含量或中含量的组分,即待测组分的质量分数在1%以上,方法准确度高;
不同点:滴定分析操作简便,快速,仪器设备简单,实用性强。方法相对误差为0.2%。重量分析法操作烦琐,分析速度慢,耗时多,其准确度比较高,有一些测定仍以重量分析为标准方法
2 仪器分析:以物质的物理或物理化学性质为基础的分析方法(光化学、电化学、热、磁、声等)需要精密仪器。
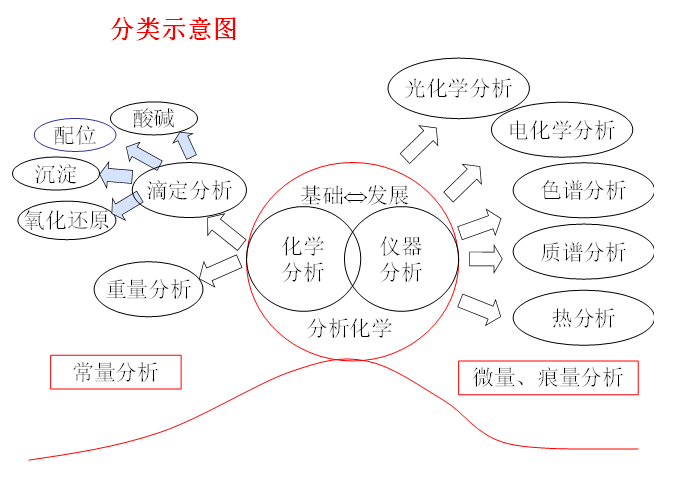
①电化学分析法:电位法、电导法、库仑法、伏安法等;
②光学分析法:紫外及可见分光光度法、原子吸收分光光度法、分子荧光法、红外分光光度法等;
③色谱分析法:液相色谱法、气相色谱法、高效液相色谱法等;
④电感耦合等离子体原子发射光谱法;
⑤质谱法;
⑥核磁共振波谱法;
⑦流动注射分析法;等。
⑦流动注射分析法;等。
特点:操作简便、快速、灵敏、所需试样量少,适合生产过程中的控制分析,特别适于微量、痕量成分分析。
仪器分析法与化学分析法的关系:
相辅相成,互为补充。


