第五节 胶体溶液型液体制剂
一、概述
胶体溶液型液体制剂(colloidalsolution)系指质点大小在1~100nm范围的分散相分散在分散介质中所形成的液体制剂。分散介质大多为 水,少数为非水溶剂。高分子化合物以单分子形式分散于溶剂中构成 的溶液称高分子溶液(polymersolutions),又称亲水胶体。分散相质点 以多分子聚集体(胶体微粒)分散于溶剂中则称为溶胶(sols),又称疏水胶体。
二、胶体溶液的种类
(一)高分子溶液
高分子化合物如蛋白质、酶类、纤维素类、右旋糖酐、聚维酮等,其分子结构中含有许多亲水基团(极性基团),如—OH、— COOH、—NH2等,能发生水化作用,水化后以分子状态分散于水中, 形成高分子溶液。高分子化合物分子结构中还有非极性基团,如— CH3 、—C6 H5及—(CH2CH2O)2 等,随着非极性基团数目的增加,高分 子的亲水性能降低,而对弱极性或非极性溶剂的亲和力增加。高分子分散在这些溶剂中时,称为高分子非水溶液,如玉米朊乙醇溶液。
有的高分子溶液如明胶水溶液、琼脂水溶液等,在温热条件下为黏稠性流动液体,但在温度降低时,呈链状分散的高分子形成网状结 构,分散介质水可被全部包含在网状结构中,形成不流动的半固体状 物,称为凝胶。【考点,(※)】形成凝胶的过程称为胶凝。凝胶可分脆性与弹性两种,前者失去网状结构内部的水分后就变脆,易研磨成粉末,如硅胶;而弹性凝胶脱水后,不变脆,体积缩水而变得有弹性,如琼脂和 明胶。
有些胶体溶液,如硬脂酸铝分散于植物油中形成的胶体溶液,在一定温度下静置时,逐渐变为半固体状溶液,当振摇时,又恢复成可 流动的胶体溶液。胶体溶液的这种性质称为触变性(thixotropy),这种胶体称为触变胶。【考点,(※)】触变胶在混悬型滴眼液或注射液中可遇到。
(二)溶胶
溶胶外观透明,但具有乳光,即丁达尔(Tyndall)现象,是一种高度分散的热力学不稳定体系。由于其质点小,分散度大,存在强烈的布 朗运动,能克服重力作用而不下沉,因而具有动力学稳定性。
溶胶在制剂中目前直接应用较少,通常是使用经亲水胶体保护的溶胶制剂,如氧化银溶胶就是被蛋白质保护而制成的制剂,用作眼、鼻收敛杀菌药。
三、胶体溶液的性质
(一)高分子溶液的性质
这里主要介绍亲水性高分子溶液的性质。
1.带电性 高分子水溶液中,高分子化合物因解离而带电,有的带正电,有的带负电。带正电荷的高分子水溶液有:琼脂、血红蛋白、碱性染料(亚甲蓝、甲基紫)、明胶、血浆蛋白等。带负电荷的有: 淀粉、阿拉伯胶、西黄蓍胶、鞣酸、树脂、磷脂、酸性染料(伊红、靛蓝)、海藻酸钠等。一些高分子化合物所带电荷受溶液pH值的影响。蛋 白质分子中含有羧基和氨基,在水溶液中随pH值不同可带正电或负 电。
在碱性 溶液 中 :NH₂—R—COOH+OH—NH₂—R—COO-+H₂O
在酸性溶液中:NH₂—R—COOH+H⁺—NH₃—R—COOH
当溶液的pH值>等电点时,蛋白质带负电荷;pH值<等电点时, 蛋白质带正电。在等电点时,高分子化合物不荷电,这时高分子溶液的许多性质发生变化,如黏度、渗透压、溶解度、电导等都变为最小 值。高分子溶液的这种性质,在药剂学中有重要用途。
高分子化合物含有大量亲水基团,能与水形成牢固的水化膜,可阻止高分子化合物分子之间的相互凝聚,这种性质对高分子化合物的 稳定性起重要作用。
2.渗透压 高分子溶液有较高的渗透压,渗透压的大小与高分子溶液的浓度有关。分子量在50000左右的高分子化合物,其溶液的渗透压可用下式表示:
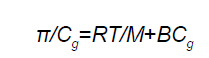 (8-3)
(8-3)
式中,π为渗透压,C,为1L溶液中溶质的克数, R为气体常数,T为绝对温度,M 为分子量,B为特定常数,它是由溶质和溶剂相互作用的大小来决定的。
3.黏性 高分子溶液是黏稠性流动液体,黏稠性大小用黏度表示。测定高分子溶液的黏度,可以确定高分子化合物的分子量。
(二)溶胶的性质【考点,(※)】
1.光学性质 当强光线通过溶胶剂时,从侧面可见到圆锥形光 束,称为丁达尔效应(Tyndalleffect)。这是由于胶粒粒度小于自然光波 长引起光散射所致。溶胶剂的浑浊程度用浊度表示,浊度愈大表明散 射光愈强。
2.电学性质 溶胶剂由于双电层结构而荷电,可以荷正电,也可以荷负电。在电场的作用下胶粒或分散介质产生移动,在移动过程中 产生电位差,这种现象称为界面动电现象。溶剂的电泳现象就是界面 动电现象所引起的。动电电位愈高电泳速度就愈快。
3.动力学性质 溶胶剂中的胶粒在分散介质中有不规则的运动,这种运动称为布朗运动。布朗运动是由于胶粒受溶剂水分子不规则地 撞击产生的。胶粒愈小运动速度愈大。溶胶粒子的扩散速度、沉降速 度及分散介质的黏度等都与溶胶的动力学性质有关。
四、胶体溶液的稳定性
(一)高分子溶液的稳定性
亲水胶体溶液的稳定性主要与水化作用有关。高分子水溶液的质点周围可形成较坚固的水化膜,水化膜可阻碍质点的相互聚集。如向高分子溶液中加入少量电解质,不会由于反离子的作用(ζ电位降低)而 聚集。但若破坏其水化膜,则会发生聚集而引起沉淀。破坏水化膜的方法之一是加入脱水剂,如乙醇、丙酮等。如图8-7所示。
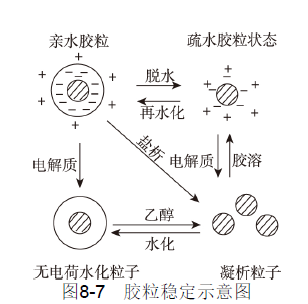
在药剂学中制备高分子物质如右旋糖酐、羧甲基淀粉钠等,都是 利用加入大量乙醇,使它们失去水化膜而沉淀。控制加入乙醇的浓度,可将不同分子量的产品分离。另一种方法是加入大量的电解质, 由于电解质强烈的水化作用,夺去了高分子质点水化膜的水分而使其沉淀,这一过程称为盐析,在制备生化制品时经常使用。引起盐析作用的主要是电解质的阴离子。不同电解质的阴离子盐析能力是不同的。按对亲水胶体的凝结能力由强到弱,将电解质的阴离子排列成的 顺序称为感胶离子序(lyotropicseries):枸橼酸离子>酒石酸离子 >SO²->CHCO0>Cl⁻>Br⁻>I⁻>CNS⁻。
高分子溶液在放置过程中也会自发地聚集而沉淀,称为陈化现 象。陈化速度受许多因素影响,如光线、空气、电解质、pH值、絮凝 剂等。高分子的质点聚集成大粒子而产生沉淀,称为絮凝,含药材提取物的制剂在放置过程中经常发生该现象。带相反电荷的两种高分子的溶液混合时,可因电荷中和而发生絮凝。这时两种高分子均失去它 们原有的一些性质,如表面活性、水化性等。
(二)溶胶的稳定性
1.溶胶的稳定性 溶胶胶粒上既有使其带电的离子,也含有一部分反离子,形成的带电层称为吸附层。另一部分反离子散布在吸附层的外围,形成与吸附层电荷相反的扩散层。这种由吸附层和扩散层构成的电性相反的电层称双电层,又称扩散双电层。由于双电层的存在,在电场中胶粒与扩散层之间发生相对移动,表现出电位差,在滑动面上的电位称ζ电位。溶胶ζ电位的高低可以表示胶粒与胶粒之间的斥力,阻止胶粒因碰撞而发生聚集,所以大多数情况下可用ζ电位作为估计溶胶稳定性的指标。溶胶质点还因具有双电层而水化,使胶粒外 形成水化膜。胶粒的电荷愈多,扩散层就愈厚,水化膜也就愈厚,溶胶愈稳定。
2.影响溶胶稳定性的因素【考点,(※)】
(1)电解质的作用 电解质的加入对ζ电位影响很大,如使扩散层变 薄,较多的离子进入吸附层,使吸附层有较多的电荷被中和,胶粒的电荷变少,使水化膜也变薄,胶粒易合并聚集。
(2)高分子化合物对溶胶的保护作用 溶胶中加入高分子溶液到一 定浓度时,能显著地提高溶胶的稳定性,使其不易发生聚集,这种现象称为保护作用,形成的胶体溶液称为保护胶体。【考点,(※)】
(3)溶胶的相互作用 胶粒带有相反电荷的溶胶互相混合,也会发生沉淀。与电解质作用的不同之处在于,两种溶胶的用量应恰使电荷 相反的胶粒所带的总电荷相等时,才会完全沉淀,否则可能不完全沉淀,甚至不沉淀。
五、胶体溶液的制备与举例
(一)高分子溶液的制备
高分子溶液制备多采用溶解法。
高分子溶液溶解首先要经过溶胀过程。溶胀是指水分子渗入到高 分子化合物分子间的空隙中,与高分子中的亲水基团发生水化作用而 使体积膨胀,使高分子空隙间充满水分子。这一过程称为有限溶胀【考点,(※)】。由于高分子空隙间存在水分子,降低了高分子的分子间作用力(范德华力),溶胀过程继续进行,最后高分子化合物完全分散在水中而形成高 分子溶液,这一过程称为无限溶胀【考点,(※)】。无限溶胀过程常需加以搅拌或加热等步骤才能完成。例如将明胶碎成小块,放于水中浸泡3~4h,使其吸水膨胀,这是有限溶胀过程,然后加热并搅拌使其形成明胶溶液,这是无限溶胀过程。琼脂、阿拉伯胶、西黄蓍胶、羧甲基纤维素钠等 在水中的溶解均属于这一过程。甲基纤维素则可直接溶于冷水中。淀粉遇水立即膨胀,但无限溶胀过程必须加热至60~70℃才能制成淀粉 浆。胃蛋白酶、蛋白银等高分子药物,其有限溶胀和无限溶胀过程都很快,制备时需将其撒于水面,待其自然溶胀后再搅拌可形成溶液,【考点,(※)】如果将它们撒于水面后立即搅拌则易形成团块,并在团块周围形成水 化层,使溶胀过程变得相当缓慢,影响制备。
(二)溶胶的制备
溶胶的制备可采用分散法和凝聚法。
1.分散法
(1)研磨法 即机械粉碎的方法,适用于脆而易碎的药物,对于柔 韧性的药物必须使其硬化后才能研磨。
(2)胶溶法 是使聚集起来的粗粒重新分散的方法,而不是使脆的 粗粒分散成溶胶。将制得的沉淀,经洗涤除去过多的电解质,加入少量的稳定剂可制得溶胶。如Fe(OH)3新鲜沉淀加入稳定剂FeCl3(起作用 的是其中的FeO+离子),经搅拌可得Fe(OH)3溶胶。
(3)超声波分散法 利用超声波(频率大于16000Hz)所产生的能量 来进行分散的方法。当超声波直接进入粗分散系统后,可产生相同频率的振动波,使粗粒分散成胶体粒子。
2.凝聚法 药物在真溶液中可因物理条件(如溶剂组成)的改变或化学反应而形成沉淀,若条件控制适度,使该溶液有合适的过饱和度, 就可以使形成的质点大小恰好符合溶胶分散相质点的要求。
例 聚维酮碘溶液
【处方】聚维酮碘100g 蒸馏水适量 共制成1000mL
【制法】称取聚维酮碘,撒布于蒸馏水面上徐徐溶解,加蒸馏水至足量,即得。
【性状】本品为红棕色液体。
【功能与主治】用于化脓性皮炎、皮肤真菌感染、小面积轻度烧烫伤,也用于小面积皮肤、黏膜创口的消毒。
【用法与用量】外用。用棉签蘸取少量,由中心向外周局部涂 搽。一日1~2次。
【规格】 100mL ∶ 10g。
【贮藏】避光,密封贮存。
【注解】聚维酮碘含有效碘8.5%~12.0%,无定形粉末,可溶于 水或乙醇,无碘的挥发性,对皮肤黏膜无刺激性,不引起过敏反应, 局部应用时不与蛋白结合。
本品为胶体溶液,属消毒防腐药,对细菌、病毒、真菌均有较强的杀灭作用,可用于黏膜或体腔。凡对碘过敏者、甲状腺患者及肾损 害的患者禁用。


