影响酶催化反应的因素
-
1 教学内容
-
2 教学课件
-
3 章节测试
-
4 拓展阅读
上一节
下一节
8.2 影响酶催化反应的因素
食品中的酶只能通过间接测定其催化活性来达到检测的目的。因此,酶催化反应动力学是研究影响酶催化反应速率的各种因素。
8.2.1 底物浓度的影响
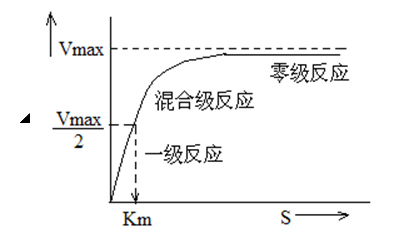
当底物浓度较低时,反应速率与底物浓度的关系呈正比关系,为一级反应;之后,随着底物浓度的增加,反应速率不是呈直线增加,表现为混合级反应。如果再继续加大底物浓度,曲线表现为零级反应,反应速率趋向一个极限,说明酶已被底物饱和。
8.2.2 pH对酶反应速率的影响
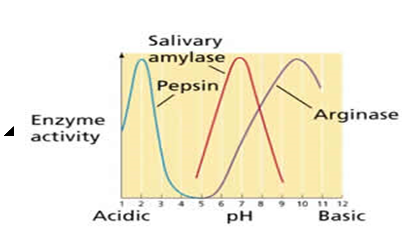
每种酶都有一最适pH值范围,通常酶只在此pH范围内才具有催化活性。食品中酶的最适pH一般是5.5-7.5。
pH影响酶催化活性的原因有以下方面:
①远离酶的最适pH的酸碱环境将影响蛋白质的构象,甚至使酶变性或失活。
②偏离酶的最适pH的酸碱环境酶虽然不变性,但由于改变了酶的活性点上产生的静电荷数量,从而影响酶活力。
③pH影响酶分子中其他基团的解离,因而也影响到酶分子的构象和酶的专一性。
8.2.3 温度对酶催化反应速率的影响
在低温范围内随温度提高,酶活性增加,但超过一定的温度范围后,酶活性则随温度的升高而下降,甚至失去酶活。温度与酶活性的关系呈钟形曲线。每一种酶都有一最适宜温度范围。酶在干燥状态比在潮湿状态对温度的耐受力要高。
各种酶的热稳定性相差较大。酶的热失活遵循一级反应动力学方程。
“D值”是指将酶活减少为原来的10-1所需要的时间。
酸性磷酸酶,其活性常用它区分生乳和巴氏杀菌乳。过氧化物酶可以指示用于使所有酶热失活的调控过程,比如评价热烫处理过程的充分与否。
酶的热失活还与pH有关。
8.2.4水分活度对酶活力的影响
水分活度较低,酶活性被抑制。只有酶的水合作用达到一定程度时才显示出活性。
8.2.5酶浓度对酶反应速率的影响
在pH、温度和底物浓度一定时,酶催化反应速率正比于酶的浓度。
8.2.6 激活剂对酶反应速率的影响
凡是能提高酶活性的物质,都称为激活剂。
(1)无机离子。金属离子对酶的作用具有一定选择性,即一种激活剂对某些酶能起激活作用,但对另外一种酶可能有抑制作用。有时离子之间还存在拮抗效应。
(2)中等大小的有机分子。如,半胱氨酸、还原型谷胱甘肽等能激活某些酶。
(3)具有蛋白质性质的大分子物质。能激活酶原,使原本无活性的酶原转变为有活性的酶。
8.2.7 抑制剂对催化反应速率的影响
酶的抑制作用是指一些物质与酶结合后,使酶活力下降,但并不引起酶蛋白变性的作用,凡是降低酶催化反应速率的物质称抑制剂。
食品组成中常存在酶抑制剂,如,豆科种子中存在的胰蛋白酶抑制剂、胰凝乳蛋白酶抑制剂、淡粉酶抑制剂等。
有酶抑制剂,一些抑制酶活性的工艺。
从对酶活性抑制的动力学角度,抑制剂可以分为两类,即可逆抑制剂和不可逆抑制剂。可逆抑制剂与酶之间以非共价键发生作用,不涉及化学反应。
通常将可逆抑制剂分为竞争性抑制、非竞争性抑制和反竞争性抑制三种类型。
8.2.8其他因素的影响
其他一些物理因素的影响。如高压、电场等影响。
8.2.8.1 HEEP对酶活的影响
HEEP又称高压电磁脉冲,能有效地降低液体食品的微生物数,延长货架周期,且对食品的感官、物理、化学性质均无明显影响。
HEEP处理食品,由于能使酶电荷及结构改变,还可抑制食品中某些酶的活性,增加食品的可贮藏性。但是,有些酶在低脉冲电场作用下对其有激活作用,只有相对较高的脉冲电场作用较长时间下才能失活。如溶菌酶。


