1.电解质的平均活度和平均活度因子
仿照化学势的定义,表示出电解质溶液中的正、负离子的化学势:
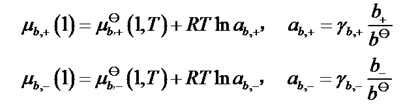
整个电解质B的化学势为各离子的化学势之和。
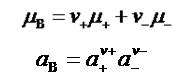
强电解质B的离子平均活度、离子平均活度因子
定义为:
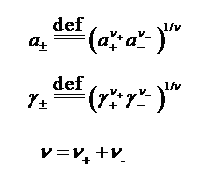
电解质的平均活度与平均活度因子之间的关系:
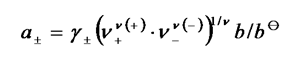
离子平均活度因子的值可由实验测定(如通过依数性或原电池电动势来间接测定),或由德拜-休克尔公式进行计算,其数值大小反映了由于离子间静电作用所导致的电解质溶液的性质与理想稀溶液热力学性质的偏离程度。
在稀溶液中,离子浓度和电解质价型是影响离子平均活度因子的主要因素。据此,路易斯和兰德尔于1921年提出了离子强度的概念。
2.电解质溶液的离子强度
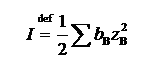
Lewis根据实验结果进一步总结出:在稀溶液范围内,一定价型电解质的平均活度因子与离子强度的关系符合如下经验规律
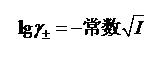
3.德拜-休克尔极限定律
1923 年,德拜和休克尔提出了强电解质溶液的离子互吸理论,认为强电解质在稀水溶液中完全解离,并且没有离子缔合,强电解质溶液对理想稀溶液规律的偏差主要来源于离子间的静电吸引力(主要是库仑力),可归结为中心离子与离子氛之间的作用。按照离子氛模型,就可以形象地将溶液中众多正、负离子间的静电相互作用,完全归结为中心离子所带的电荷与包围它的离子氛的净电荷之间的静电作用。这样,所研究的问题及理论推导就可大大简化。德拜-休克尔根据离子氛的概念,并引入几个假定,导出了强电解质稀溶液中离子平均活度因子的计算公式,称为德拜-休克尔极限定律。
![]()
该式只适用于很稀(一般b = 0.001~0.01 mol·kg-1)的电解质溶液,用于从理论上计算强电解质稀溶液的离子平均活度因子。


