第三节 肿瘤的免疫逃逸机制
肿瘤免疫编辑学说(cancer immunoediting)是当前被认可的肿瘤免疫逃逸理论。该理论根据肿瘤的发展将其分为三个阶段:首先是清除期(elimination phase),此阶段机体的免疫监视功能通过抗肿瘤免疫效应机制发挥抗肿瘤作用,如能清除突变细胞,机体则保持健康。其次是平衡期(equilibrium phase)在此阶段免疫系统和肿瘤细胞的斗争处于势均力敌的态势,免疫系统选择性地消灭一部分肿瘤细胞,另一部分肿瘤细胞通过突变等改变力图逃避免疫系统的杀伤。肿瘤细胞在此阶段通过不断改变重塑(reshape)自身特点的过程称为肿瘤免疫编辑(cancer immunoediting)。第三阶段即为免疫逃逸期(escape phase),此时肿瘤细胞具备了抵抗免疫系统清除的功能并发展为具有临床表现的肿瘤。
肿瘤的免疫逃逸机制相当复杂,涉及肿瘤细胞本身、肿瘤生长的微环境和宿主免疫系统等多个方面。
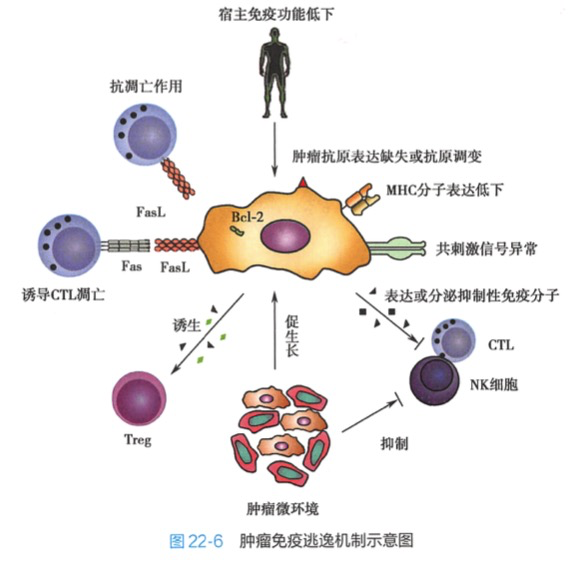
一、肿瘤细胞所具有的逃避免疫监视的能力
突变细胞在体内生长和增殖的过程中,部分免疫原性较强的细胞被机体的免疫系统所识别和杀伤,部分突变细胞通过多种机制逃避免疫系统的识别和清除,导致肿瘤的形成。肿瘤细胞通过自身改变适应机体的内环境,阻碍机体产生有效的免疫应答,且能抵抗或抑制机体的免疫效应功能。
1. 肿瘤细胞的肿瘤抗原缺失和抗原调变 肿瘤表达抗原与正常蛋白差别很小,免疫原性弱,无法诱发机体产生有效的抗肿瘤免疫应答。在机体抗肿瘤免疫的压力下,肿瘤细胞表达的肿瘤抗原减少或丢失,从而使肿瘤细胞逃避免疫识别和杀伤,此为抗原调变(antigenic modulation)。
2.肿瘤细胞 MHCI类分子表达低下 肿瘤细胞表面 MHCI类分子的表达通常缺陷或表达低下,致使肿瘤细胞不能或弱提呈肿瘤抗原,无法诱导 CTL 以杀伤肿瘤细胞。
3.肿瘤细胞共刺激信号异常 尽管某些肿瘤细胞可表达肿瘤抗原,具有一定的免疫原性(可提供T细胞活化的第一信号),但其很少表达CD80和CD86等共刺激分子,却表达PD-L1等共抑制分子,因而不能为T细胞活化提供第二信号,无法有效诱导抗肿瘤免疫应答,T细胞的失能使机体对肿瘤产生免疫耐受。
4.肿瘤细胞表达或分泌某些免疫分子抑制机体的抗肿瘤免疫功能 包括能促进肿瘤细胞生长的表皮细胞生长因子以及具有强大的免疫抑制作用、可抑制机体抗肿瘤免疫应答的TGF-β(膜结合型和分泌型)、IL-10、IL-33等。肿瘤细胞表达FasL可诱导肿瘤特异性T细胞凋亡。
5.肿瘤细胞主动诱导 Treg 和 MDSC的产生 肿瘤细胞可主动诱导荷瘤机体产生 Treg和 MDSC 等调节性细胞抑制机体的抗肿瘤免疫应答。
6.肿瘤细胞的抗凋亡作用 肿瘤细胞可高表达多种抗凋亡分子如 Bcl-2,不表达或弱表达Fas等凋亡诱导分子,从而抵抗 CTL等诱导的凋亡,逃避杀伤效应。
二、肿瘤微环境的作用
肿瘤发生的微环境内包含各种能抑制和促进肿瘤细胞分化、增殖、转移的复杂成分,也包含能抑制和促进机体免疫细胞分化、功能和效应的复杂成分,如免疫效应细胞和免疫效应分子、各种免疫抑制性细胞如Treg、MDSC、TAM及免疫抑制分子等。这些免疫激活和抑制性的细胞和分子部分来源于肿瘤细胞和肿瘤局部免疫细胞,或由机体其他部位趋化而来。肿瘤与微环境之间既相互依存,又相互促进,也存在相互拮抗和相互斗争。某些个体形成肿瘤的原因之一是肿瘤微环境促进了肿瘤细胞的生长,保护了肿瘤细胞免受免疫效应细胞的清除。
三、宿主免疫功能的影响
宿主免疫功能的高低也是肿瘤细胞实现免疫逃逸的关键。当宿主处于免疫功能低下状态时,如长期服用免疫抑制剂或HIV感染等、APC功能低下或缺陷或体内存在一定量的“增强抗体”时,都有助于肿瘤逃避宿主免疫系统的攻击:肿瘤细胞本身产生的免疫抑制因子及其诱导产生的免疫抑制细胞也能导致宿主免疫功能低下或免疫抑制,从而在免疫应答诱导和效应等多个环节抑制机体抗肿瘤免疫应答。