第四节 抗病毒免疫
病毒属于胞内病原体,通过与宿主表面的相应受体结合而进入细胞,随后在宿主细胞内进行病毒蛋白翻译和子代病毒的组装,子代病毒从已感染细胞中释放。
除直接破坏宿主细胞,非致细胞病变病毒可通过感染诱发的炎症免疫反应损伤宿主细胞导致疾病。某些病毒感染呈现潜伏感染状态,当宿主免疫力下降,潜伏态病毒会启动活化、增殖,反复导致疾病的急性发生。如潜伏水痘病毒重新活化引发带状疱疹。
一、抗病毒免疫
与胞内菌类似,抗病毒免疫主要依赖于细胞免疫。
(一)抗病毒固有免疫
1.干扰素 抗病毒免疫最重要的早期免疫分子是干扰素(I型干扰素IFN-a.IFN-β 和Ⅱ型干扰素IFN-γ)。IFN-a和IFN-β由感染局部上皮细胞、成纤维细胞和pDC等分泌,而IFN-γ早期由活化的巨噬细胞和 NK细胞分泌,后期则由活化 Th1 细胞产生。任何一种干扰素均可调节未感染细胞的代谢和酶相关事件,使细胞呈现抗病毒状态。
2.NK细胞 NK细胞是重要的早期抗病毒效应细胞,被病毒感染的宿主细胞的表面MHCI类分子下调,这一信号被NK细胞识别并对被感染细胞直接杀伤(通过天然的细胞毒作用);NK细胞还可通过分泌促炎细胞因子在感染早期起重要的防御作用;NK 细胞同时还是抗病毒 ADCC中的效应细胞。NK细胞天然的细胞毒作用和促炎因子生成是受到前述三种IFN的刺激所产生的。
3.巨噬细胞 巨噬细胞在病毒感染早期开始活化并生成大量的促炎介质。IFN-γ可以增强这一功能并且使巨噬细胞表达iNOS 酶从而生成
NO,后者可促进巨噬细胞产生 ROIs和 RNIs帮助杀灭被吞噬的病毒。另外,巨噬细胞也可通过 ADCC 机制清除病毒。
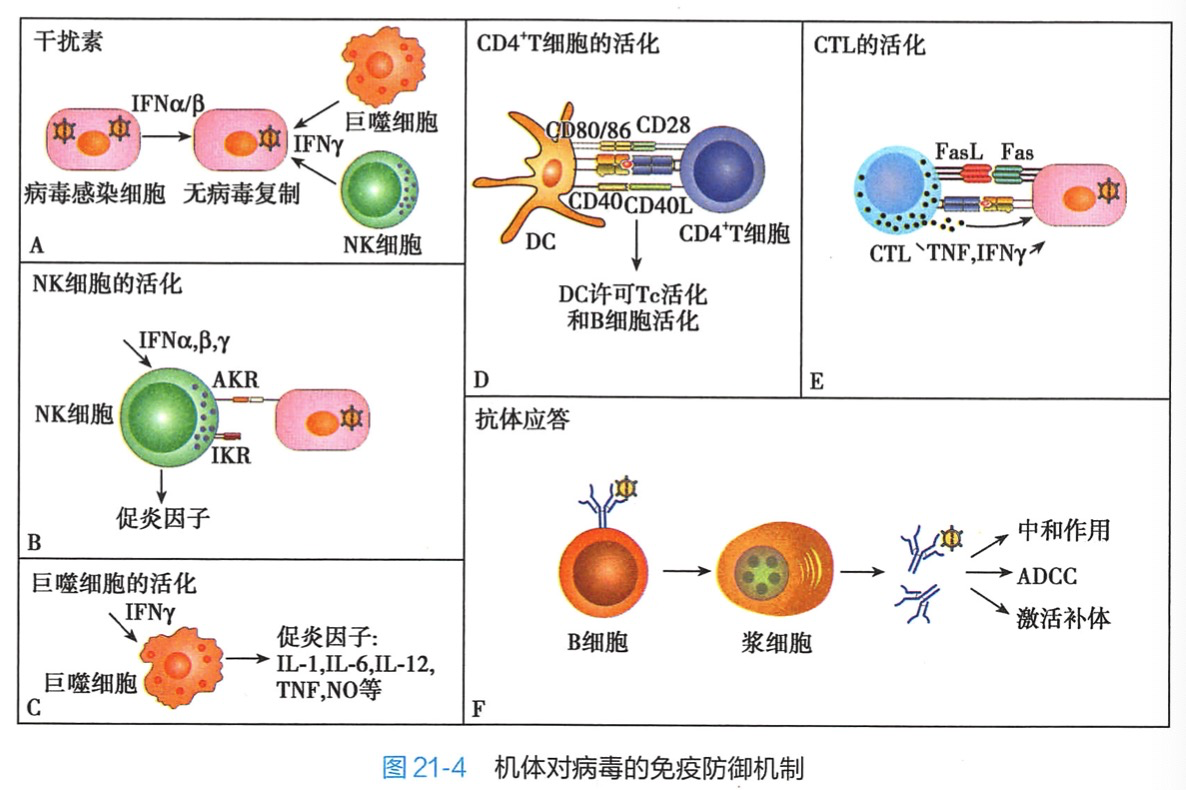
(二)抗病毒适应性免疫
1.病毒特异性CD4+T细胞应答 完整的病毒颗粒或其组分可通过胞吞和吞噬作用被DC等吞噬细胞摄取、加工,并提呈抗原;另一方面,DC的多种 TLR 可识别病毒的核酸序列或蛋白抗原使 DC更易于通过外源途径提呈病毒抗原肽与MHCⅡ类分子复合物,激活 CD4+T细胞。这对于抵抗病毒十分重要,因为这些细胞可为初始CD8+T细胞的活化提供IL-2,还可以为B细胞提供CD40L介导的共刺激信号和细胞因子,促进B细胞产生抗体。
2.病毒特异性CD8+T细胞应答
病毒特异性
CTL应答是抗病毒免疫的关键。一方面,病毒在被感染细胞内增殖,通过内源性抗原提呈途径将pMHCI提呈在感染细胞表面,成为CTL的靶;另一方面,病毒特异性CTL在引流淋巴结被激活后到达感染部位,通过颗粒酶介导的细胞毒作用、Fas介导的细胞凋亡或分泌 TNF 及IFN 杀死靶细胞。
3.病毒特异性抗体应答
B细胞能识别被提呈在感染细胞表面的病毒抗原信号,也能识别感染细胞释放的子代病毒颗粒,在T细胞帮助下,B细胞被激活,并进一步分化为浆细胞、记忆B细胞,产生中和抗体。因为病毒在细胞内,早期产生的抗体多不能发挥作用,但晚期的中和性抗体进人血液后可结合病毒、阻止病毒结合宿主细胞上的病毒受体,从而防止感染进一步扩散;抗病毒抗体可介导ADCC:也可激活补体,在有胞膜的病毒和被感染的宿主细胞表面形成MAC以杀死病毒或感染细胞。另外,补体成分还可调理吞噬细胞外的病毒颗粒。这是T-B细胞协同抗感染的经典案例。值得注意的是,一些病毒可能不需要T细胞的辅助,只通过B细胞应答就可清除(至少部分清除)。如VSV病毒表面具有高度重复的结构可引起TI应答,而TI应答比TD应答更快,目仅涉及B细胞而不需要 B-T相互作用,因此可在感染早期发挥作用,更有效减少了病毒的扩散,直到机体产生针对其 TD 抗原的抗体应答。
二、病毒的免疫逃逸机制
一是通过病毒的快速增殖能力,尤其基因组较小的病毒比基因组较大的病毒增殖更快,在免疫应答产生之前就播散到新的宿主细胞建立感染:二是病毒干扰宿主免疫应答,使其有足够的时间建立感染。一但感染建立,病毒可通过多种机制逃避抗病毒免疫攻击。

1.潜伏
病毒的固有生物特性决定其是否潜伏。病毒一旦潜伏,它在宿主细胞以一种缺陷的形式存在,使其不具有活动性。潜伏的病毒需要更强的抗病毒免疫才能清除,而机体在病毒潜伏后,抗病毒免疫多处于耗竭状态,使得病毒可长期逃逸。特别需要提醒的是某些潜伏病毒仍具有致癌风险。
2.病毒变异 在宿主免疫压力下,病毒较其他病原体更易发生基因变异,某些基因变异可导致抗原性变异,从而逃脱宿主体内预存免疫。病毒抗原基因突变导致的抗原性变异称为“抗原漂移”例如,流感病毒和 HIV 等都具有快速抗原漂移的能力,即使在同一感染个体中也可发生。
3.干扰抗原提呈 病毒感染抗原提呈细胞后可干扰抗原提呈的多个环节,从而逃逸抗病毒免疫。腺病毒、巨细胞病毒(CMV)、HIV、VSV、EBV等通过干扰
MHCI限制性抗原提呈途径不同的节点,造成CD8+T细胞活化障碍,从而逃逸抗病毒细胞免疫;腺病毒、巨细胞病毒(CMV)、HIV等还可通过干扰
MHC Ⅱ类分子介导的抗原提呈不同节点,干扰抗病毒体液免疫应答。
4.“愚弄”NK细胞 CMV表达MHCI类分子的类似物,结合NK细胞抑制性受体,使NK细胞认为它识别的是一个“没有下调的”的MHCI类分子.导致NK细胞不被活化:快速复制的WNV上调经典的宿主 MHCI类分子,也使NK细胞不能识别、活化。
5.干扰DC功能 HTLV-1感染DC前体,阻止其分化,成为不成熟的DC;HSV-1和牛痘病毒感染不成熟的DC,阻止DC成熟,这都阻碍了T细胞应答的启动。麻疹病毒感染使DC形成叫做合胞体的聚集物,病毒可在其中自由复制。麻疹病毒感染则上调DC表达FasL,从而杀死带有Fas的T细胞
CMV感染使DC变为耐受性.导致与其相遇的T细胞无能而非激活T细胞。
6.干扰抗体效应 一些病毒可直接干扰抗病毒抗体的产生和效应。麻疹病毒表达一种对B细胞的激活起抑制作用的蛋白;HSV-1则使感染的宿主细胞表达病毒形式的FcγR,后者与IgG分子结合使Fc 端被封闭,阻止ADCC 和经典的补体激活。
7.逃避补体杀伤 某些病病器和疱疹病毒分泌阻碍旁路C3转化酶形成的蛋白质,导致补休系统活化障碍。多种病毒表达RCA蛋白类似物或上调宿主RCA蛋白的表达,防止感染的细胞受MAC介导的溶解。HIV和牛痘病毒等通过在宿主细胞膜出芽的方式得到RCA蛋白、DAF和MIRL,逃避补体杀伤。
8.消除抗病毒状态 病毒通过复杂的机制干扰抗病毒状态。如
EBV表达一种生长因子的可溶性受体,后者阻断了该生长因子对巨噬细胞的作用,由于这种生长因子是巨噬细胞分泌IFN所必需的,因此引起IFN的减少,不足以激发和维持抗病毒状态。当HSV感染已建立了抗病毒状态的细胞时,病毒表达一种蛋白,逆转病毒蛋白合成受阻状态,使得病毒复制得以恢复。牛痘病毒和丙型肝炎病毒也可合成蛋白质.破坏对维持抗病毒状态所需的代谢和酶。腺病毒及KSHV则表达可干扰宿主转录因子活性或与宿主转录因子类似蛋白质,干扰宿主细胞建立抗病毒状态所需的基因转录。
9.调控宿主细胞的凋亡,被感染的宿主细胞在病毒复制完成之前凋亡导致病毒死亡,是宿主抗病毒机制之一通常由CTLFasFasTTER介导 被咸细胞有时通过内质网胁迫机制发生“利它的”凋亡(死亡对宿主有益),宿主不得不释放大量病毒蛋白而导致内质网胁迫现象。但具有大基因组的病毒已经发展出阻断这些死亡诱导途径各个环节的办法。如腺病毒合成一个蛋白复合物。引起Fas和TNFR的内化,将这些死亡受体从细胞表面清除.中断FasL或TNF介导的凋亡:一些痘病毒表达TNER的类似物,作为TNF和相关细胞因子的诱饵受体:腺病毒.疴疹病毒和病病毒表达多种蛋白质,抑制凋亡所需的酶级联反应:还有许多病毒可以增加宿主细胞存活蛋白或表达这些生存蛋白的类似物,从而阻止宿主细胞过早凋亡。
10.干扰宿主细胞因子
在病毒感染的早期,宿主细胞生成大量的细胞因子和趋化因子以协调抗病毒反应。一些痘病毒可以改变局部的细胞因子,使它不利于支撑免疫应答所必需的细胞间合作。痘病毒通过合成趋化因子类似物阻断淋巴细胞、巨噬细胞和中性粒细胞的趋化和迁移,还可分泌干扰素受体类似物,阻断IFN-a和IFN-B效应。KSHV和腺病毒表达一种蛋白质,抑制IFN诱导的基因转录,疱疹病毒下调细胞因子受体的表达,而CMV干扰趋化因子基因的转录。许多病毒抑制IL-12生成,从而干扰Th1分化和随后的抗病毒细胞免疫应答。EBV则合成IL-12的类似物,可以竞争性抑制宿主正常IL-12的活性。EBV产生IL-10的类似物,抑制巨噬细胞生成IL-12和淋巴细胞生成IFN-γ。