第二节 抗胞外菌免疫
胞外菌是不进入宿主细胞内而在宿主细胞外如血循环、结缔组织、消化道、呼吸道、泌尿生殖道等增殖的细菌。胞外菌主要通过两种机制致病:1)引发炎症,导致感染部位组织损伤,这是化脓性球菌导致人体化脓性感染的主要原因;2)释放内毒素和外毒素。革兰氏阴性菌可释放内毒素(脂多糖)。强烈活化巨噬细胞导致炎症。外毒素可破坏宿主细胞或刺激机体产生炎症反应。宿主抗胞外菌免疫主要依赖于体液免疫应答。
一、抗胞外菌固有免疫
抗胞外菌的固有免疫应答主要基于补体活化、吞噬作用和炎症反应。
(一)补体活化
革兰氏阳性菌的细胞壁所含有的肽聚糖可直接通过旁路途径活化补体系统;革兰氏阴性菌的胞壁含有的LPS,可在没有抗体存在的情况下直接通过旁路途径活化补体系统;细菌大多在其表面表达甘露糖,后者可直接结合凝集素,通过凝集素途径激活补体系统。
补体系统活化后:第一,通过补体调理作用促进免疫细胞对细菌的吞噬。第二,产生膜攻击复合物溶破细菌。第三,通过其裂解产物招募、活化白细胞,参与炎症反应。
(二)吞噬作用
宿主吞噬细胞对胞外菌非特异吞噬效率较低,但宿主细胞多通过其细胞膜表面不同受体结合胞外菌,通过受体介导的特异性吞噬高效率吞噬细菌,这些受体包括前面提及的甘露糖受体、清道夫受体、Toll 样受体及补体受体等。这些受体一方面使得吞噬细胞以更高的效率吞噬细菌,另一方面激活吞噬细胞发挥杀菌活性。
(三)炎症反应
吞噬细菌后的吞噬细胞随即被活化而分泌细胞因子,后者一方面招募白细胞浸润到感染局部,从而启动炎症反应,导致组织损伤。另一方面,引起感染的全身表现如发热、合成急性期蛋白等。
二、抗胞外菌适应性免疫
体液免疫是宿主对抗胞外菌感染的主要保护性免疫机制,通过体液免疫可清除病原体或中和毒素。
胞外菌感染所含有的蛋白质抗原作为典型的胸腺依赖抗原可激活CD4+T细胞,活化的辅助 CD4+T细胞不但通过产生细胞因子辅助B细胞产生抗体,更重要的是通过分泌细胞因子增强巨噬细胞吞噬和杀菌。这是适应性免疫与固有免疫协同的典型案例。宿主产生主要针对胞壁成分或毒素的抗体,通过中和作用、调理吞噬作用、激活补体经典途径等清除胞外菌感染。其中,中和作用主要依赖高亲和力IgG和IgA;补体激活主要靠IgM和IgG;调理作用则主要是IgG的某些亚型。
三、胞外菌的免疫逃逸机制
在免疫压力下,部分胞外菌也会进化出逃避免疫的机制。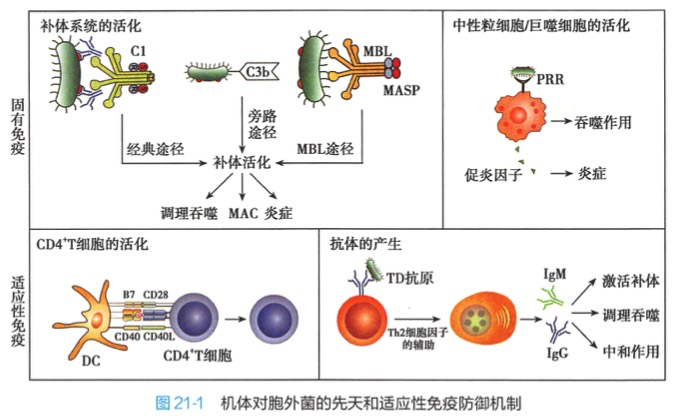
(一)逃避特异性抗体的作用
一些胞外菌(如淋球菌)常常会自发地改变其与宿主细胞表面结合的氨基酸序列,逃逸中和抗体对细菌的识别使得细菌能在机体内持续感染;另有某些细菌通过分泌蛋白酶来裂解抗体使其失活。例如,流感嗜血杆菌可表达IgA特异性的蛋白酶,从而可降解血液和黏液中的slgA。
(二)逃避吞噬细胞的吞噬
具有多聚糖“外衣”的细菌可以防止与吞噬细胞表面的受体结合而被吞噬:另一些没有多聚糖“外衣”的胞外菌可以临时进人非吞噬细胞(如上皮细胞和成纤维细胞)而“躲避”吞噬细胞的俘获。为了能进入这些非吞噬细胞,病原体会释放细菌蛋白到宿主细胞中并通过提升其巨吞饮作用或者细胞骨架的重构;进入细胞的胞外菌蛋白还具有抗吞噬的能力,例如.小肠结肠炎耶尔森菌属可以将组菌的磷酸酯酶注入巨噬细胞,当细菌的磷酸脂酶使宿主蛋白去磷酸化后,可封闭吞噬细胞的吞噬作用。
(三)逃避补体系统介导的杀伤作用
一些胞外菌凭其自身结构的特点避免受到补体介导的杀伤作用。如梅毒苍白螺旋体的外膜缺乏跨膜蛋白,导致没有合适的位点供C3b附着;另有细菌拥有胞壁LPS,因LPS具有长且突出表面的链因而阻止细菌表面上的MAC复合体的装配:有些胞外菌能够合成灭活补体片段的物质如B型链球菌的胞壁含有唾液酸,可降解C3b从而封闭补体的活化,而其他链球菌可产生能与RCA蛋白H因子结合的蛋白,并将它固定在细菌的表面,招募H因子使 C3b降解以达到补体失活。沙门菌属表达的蛋白主要干扰的是补体活化的最后阶段,而淋球菌和脑膜炎奈瑟菌可以诱导宿主产生单一类型的抗体(如IgA),从而导致补体系统不能高效激活,这些“封闭抗体”与补体结合抗体在细菌表面相互竞争能降低 MAC 的组装 干预 C3b 的附着。