抗原的加工和提呈
抗原加工(antigen processing) 或称抗原处理,是APC 将摄取入胞内的外源性抗原或者胞质内自身 产生的内源性抗原降解并加工成一定大小的多肽片段、使抗原肽适合与MHC 分子结合、抗原肽-MHC 分子复合物再转运到细胞表面的过程。 抗原提呈(antigen presentation) 是表达于APC 表面的抗原肽- MHC 分子复合物被T 细胞识别、从而将抗原肽提呈给T 细胞,诱导T 细胞活化的过程。 T 细胞只能识 别APC 提呈的抗原肽:CD4+T 细胞的TCR识别APC 提呈的抗原肽-MHC II 类分子复合物,CD8+T 细胞 的TCR 识别靶细胞提呈的抗原肽-MHC I 类分子复合物。
—、 APC提呈抗原的分类
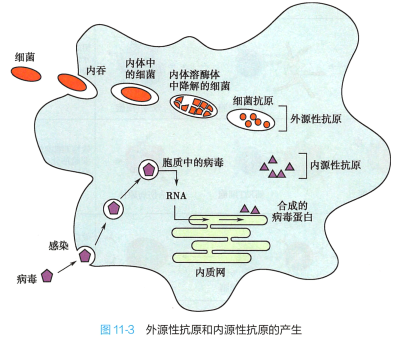
根据来源不同可将被提呈的抗原分为两大类(图11-3) :1)来自细胞外的抗原称为外源性抗原 (exogenous antigen) , 例如被吞噬的细胞、 细菌或蛋白质抗原等; 2)细胞内合成的抗原称为内源性抗原 (endogenous antigen) , 例如病毒感染细胞内合成的病毒蛋白、肿瘤细胞内合成的肿瘤抗原和某些细胞 内的自身抗原等。
二、 APC 加工和提呈抗原的途径
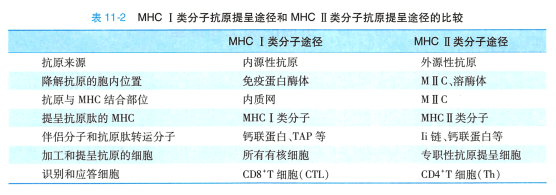
根据抗原的性质和来源不同,APC 通过四种途径进行抗原的加工和提呈:MHC I 类分子途径(内源性抗原提呈途径或胞质溶胶抗原提呈途径)、MHCII 类分子途径(外源性抗原提呈途径或溶酶体抗原提呈途径)、非经典的抗原提呈途径(MHC 分子对抗原的交叉提呈途径)、脂类抗原的CDI 分子提 呈途径。 表11-2 归纳了MHC I 类分子途径和MHCII 类分子途径的差别。
(一) MHC I 类分子抗原提呈途径
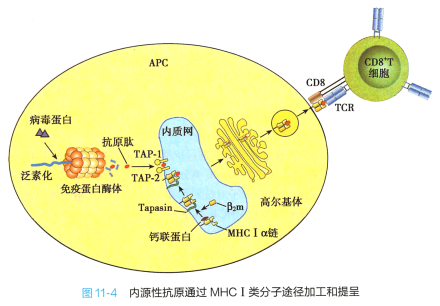
内源性抗原主要通过MHC I 类分子途径加工与提呈(图11-4) 。 由于所有有核细胞(也包括前述的专职性APC)均表达MHC I 类分子,因此,所有有核细胞均具有通过MHC I 类分子途径加工和提呈 抗原的能力。
内源性抗原的加工与转运 胞质中的蛋白抗原须首先降解成抗原肤,才能进行转运。 细胞内 蛋白首先与泛素结合,泛素化蛋白呈线性进入蛋白酶体(proteasome) 被降解。 蛋白酶体是一种胞内大 分子蛋白酶的复合体,为中空的圆柱体结构,主要负责将胞质中多余的错误合成或折叠的蛋白质降解 为多肤。 干扰素等可诱导细胞产生低分子量多肽( low molecular weight peptide , LMP) , LMP 取代蛋白 酶体催化亚单位使其酶解蛋白质的模式发生变化而成为免疫蛋白酶体( immunology proteasome) 。 免疫蛋白酶体能降解内源性抗原,产生6 ~ 30 个氨基酸残基大小的、C 端多为碱性或疏水氨基酸的抗原肽,有利于其转运和与MHC I 类分子的抗原肽槽结合,所以免疫蛋白酶体是细胞加工内源性抗原肤 的主要场所。
抗原加工相关转运物( transporter associated with antigen processing, TAP) 是由两个6 次跨膜蛋白 (TAPl 和TAP2)组成的异二聚体,在ER膜上形成孔道,其功能是将抗原肤从胞质转运至ER 腔内与
新组装的MHC I 类分子结合。 胞质中的抗原肽与TAP 结合,TAP 以 ATP 依赖的方式发生构象改变, 开放孔道,主动转运抗原肽进入ER 腔内。 TAP 可选择性地转运含8 ~ 16 个氨基酸且C 端为碱性或疏 水氨基酸的抗原肽。 TAP 也能将内质网中多余的抗原肽转运回胞质中。
2. MHC I 类分子的合成与组装 MHC I 类分子α链和β2微球蛋白(β2m) 在ER 中合成。 α链合成后立即与伴侣蛋白(chaperone) 结合。 伴侣蛋白包括钙联蛋白(calnexin) 、钙网蛋白(calreticulin) 和TAP 相关蛋白( tapasin) , 它们参与α链的折叠及α 链与β2m组装成完整的MHC I 类分子、保护α链不被降解。 其中tapasin 介导新合成的MHC I 类分子与TAP 的结合,有利于转入的抗原肽就近与 MHC I 类分子结合。
3. 抗原肽-MHC I 类分子复合物的形成与抗原提呈 在伴侣蛋白的参与下, MHC I 类分子组装 为二聚体,其抗原肽结合槽与适合的抗原肽结合,形成复合物。 在此过程中,内质网驻留的氨基肤酶 (ER resident aminopeptidase, ERAP)进一步修剪转入的抗原肽和内质网中合成的肽段为8 ~ 10 个氨基 酸的肽段,使更适合与抗原肽结合槽结合;经基氧化还原酶Erp57 则可催化MHC I 吐功能区的二硫 键断裂和重建,使抗原肤结合槽更适合结合抗原肤。 结合抗原肽的MHC I 类分子经高尔基体转运至 细胞膜上,提呈给CD8+T 细胞。
( 二) MHC II 类分子抗原提呈途径
外源性抗原主要通过MHCII 类分子途径加工与提呈(图11-5) 。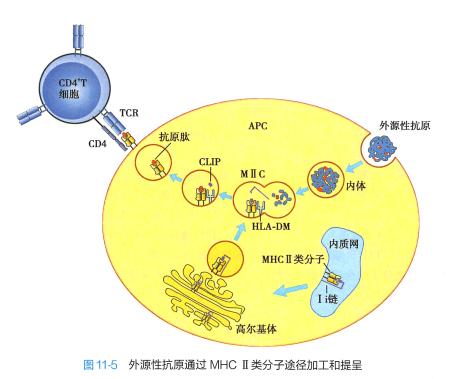
1. 外源性抗原的摄取与加工 APC 主要通过模式识别受体识别外源性抗原,通过胞饮作用、 吞噬作用、受体介导的内吞作用和内化等方式摄取抗原。 DC 通过上述方式摄取外源性抗原;单核/巨噬 细胞也能通过上述方式摄取外源性抗原,但吞噬和清除病原微生物能力很强; B 细胞主要通过受体介 导的内吞作用摄取和浓集外源性抗原,也可经胞饮作用摄取蛋白质抗原。
摄取蛋白质抗原形成的痰泡与内体(endosome) 融合;摄取的细菌等颗粒性抗原在胞内形成吞噬体(phagosome) , 吞噬体与溶酶体融合为吞噬溶酶体。 内体和吞噬溶酶体又与胞质中的MHC Il 类小 室(MHC class II compartment , M Il C) 融合。 MIl C 是富含MHCII 类分子的溶酶体样细胞器。 M II C 和 吞噬溶酶体中的多种酶类在酸性环境下活化,将抗原降解为适合千MHC Il 类分子结合的、含10 ~30 个氨基酸的短肤。 因此,MIIC 和吞噬溶酶体是APC 加工外源性抗原的主要场所,而MIl C 是抗原肽 与MHCIl 类分子结合的部位。
2. MHC Il 类分子的合成与转运 在ER 中新合成的MHCIl 类分子α链与β链折叠成二聚体, 并与Iα相关恒定链(I a-associated invariant chain, I i) 结合形成(αβli)3 九聚体。 I i 的主要功能是: CD促进MHCII 类分子a 链与β 链组装和折叠及二聚体形成;@阻止MHCII 类分子在ER 内与其他内 源性多肽结合;@促进MHCIl 类分子转运到MIl C。 MHC il /l i 九聚体由ER 经高尔基体形成MIi C。 在Mil C 腔内 I i 被特定的酶降解,仅留有称为MHC II 类分子相关的恒定链多肽(class II -associated invariant chain peptide, CLIP) 的小片段在抗原肽结合槽内防止其他肤段与之结合。3. MHC II 类分子的组装和抗原肽的提呈 MHC II 类分子的抗原肽结合槽两端为开放结构,与 之结合的最适抗原肽约含13 ~ 17 个氨基酸。 在MIIC 中,HLA-DM 分子介导抗原肽结合槽与CLIP 解 离并结合具有更高亲和力的抗原肽, 形成稳定的抗原肽-MHC II 类分子复合物。 然后,复合物被转运 至细胞膜表面,供CD4+T 细胞识别,从而将外源性抗原肽提呈给CD4+T 细胞。
此外,部分外源性抗原也可不通过I i 依赖性途径与MHCII 类分子结合,部分短肽直接与胞膜表 面的空载MHCII 类分子结合后被提呈。一些抗原被内吞入细胞内,在MII C 中被降解为多肽,随后与 再循环至胞内的空载MHCII 类分子结合,形成稳定的抗原肽-MHC II 类分子复合物,再转运到细胞膜 被提呈。
(三)非经典的抗原提呈途径 (MHC分子对抗原的交叉提呈途径)
抗原的交叉提呈(cross-presentation) 也称为交叉致敏(cross-priming) , 是指APC 能将摄取、加工的 外源性抗原通过MHC I 类分子途径提呈给cos·r 细胞;或将内源性抗原通过MHC II 类分子途径提 呈给CD4+T 细胞。 抗原的交叉提呈参与机体针对病毒(如疤疹病毒)、细菌(如李斯特菌)感染和大多 数肿瘤的免疫应答,但并不是抗原提呈的主要方式,也不涉及MHC 分子的合成。
1. 外源性抗原交叉提呈的机制 包括: 1)某些外源性抗原从内体或吞噬溶酶体中溢出进入胞质 或者直接穿越细胞膜进入胞质; 2)溶酶体中形成的抗原肽通过胞吐作用被排出细胞外,然后与细胞膜 表面的空载MHC I 类分子结合而被提呈;3)细胞表面MHC I 类分子被重新内吞进入内体,新合成的 MHC I 类分子也可进入内体,在内体中它们直接与外源性抗原肽结合形成复合物而被提呈。 有些DC 亚群优势交叉提呈外源性抗原。
2. 内源性抗原交叉提呈的机制 包括: 1)含有内源性抗原的细胞或凋亡小体被APC 摄取,形成 内体;2)细胞自噬时,自噬体可与MIIC 融合;3)内源性抗原肽被释放出细胞外,然后与细胞膜表面的空载MHCII类分子结合为复合物。
(四)脂类抗原的CD1 分子提呈途径
脂类抗原(例如分枝杆菌胞壁成分)不能被MHC 限制性T 细胞识别。 CDl 分子在APC 细胞表面吞噬体或内体细胞表面的再循环过程中,结合胞外的脂类抗原或结合进入内体的自身脂类抗原,再运至细胞膜表面进行抗原提呈,其中没有明显的抗原加工过程。 CD1 有 a - e 五个成员,均属 MHC I 类样分子,与 β2 m 结合成复合物。 CD1 也有抗原肤结合槽,可与脂类抗原的乙酰基团结合。 CD1a - c主要将不同脂类抗原提呈给T 细胞,介导对病原微生物的适应性免疫应答。 CD1d 主要将脂 类抗原提呈给NKT 细胞,参与固有免疫应答。