抗原提呈细胞(antigen-presenting cell , APC)是能够加工抗原并以抗原肽-MHC 分子复合物的形式 将抗原肤提呈给T 细胞的一类细胞,在机体的免疫识别、免疫应答与免疫调节中起重要作用。 通过MHC II 类分子途径提呈外源性抗原肽给CD4+T 细胞的APC 分为专职性APC(professional APC) 和非 专职性APC(non-professional APC) 。 专职性APC 包括树突状细胞、单核/巨噬细胞和B 细胞,它们组成性表达MHC II 类分子、共刺激分子和黏附分子,具有直接摄取、加工和提呈抗原的功能;非专职性 APC 包括内皮细胞、 上皮细胞、成纤维细胞等多种细胞,它们通常不或低表达MHC II 类分子,但在炎 症过程中或某些细胞因子的作用下,可被诱导表达MHC II 类分子、共刺激分子和黏附分子,故加工和 提呈抗原的能力较弱。 另有一类被胞内病原体感染而产生病原体抗原或细胞发生突变产生突变蛋白 抗原的细胞(又称靶细胞),可通过MHC I 类分子途径提呈这些内源性抗原肽给CD8+T 细胞而被识别 和杀伤,此类细胞也属抗原提呈细胞。
第一节 专职性抗原提呈细胞的生物学特性
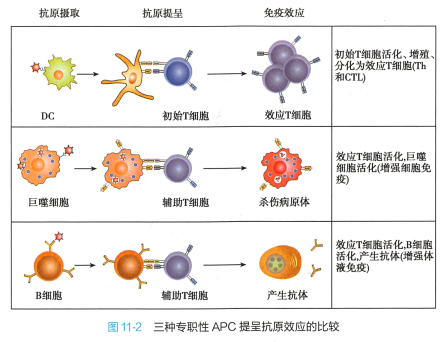
树突状细胞(dendritic cell, DC) 是体内功能最强的专职性APC,可激活初始T 细胞。 单核/巨噬细 胞和B 细胞仅能刺激己活化的效应T 细胞或记忆T 细胞,同时本身被T 细胞激活,发挥更强的作用。
—、树突状细胞
树突状细胞(dendritic cell , DC)是一类成熟时具有许多树突样突起的、 能够识别、摄取和加工外源 性抗原并将抗原肤提呈给初始T 细胞进而诱导T 细胞活化增殖的、功能最强的抗原提呈细胞。 DC 是 机体适应性免疫应答的始动者,也是连接固有免疫应答和适应性免疫应答的"桥梁”。
(一) DC 的类型
DC 主要分为经典DC(conventional DC , cDC) 及浆细胞样DC(plasmacytoid DC , pDC)两大类。 cDC根据表型和分化发育途径分为不同亚群,主要参与适应性免疫应答的诱导和启动。 根据成熟状态, DC 又分为未成熟DC 和成熟DC,它们在不同组织中有不同名称。 部分DC 具有负向调控免疫应答、 维持免疫耐受的作用,称为调节性DC(regulatory DC) 。 pDC 也能加工提呈抗原,其主要功能是活化后 可快速产生大量1 型干扰素,参与抗病毒固有免疫应答,在某些情况下也参与自身免疫病的发生发 展。 滤泡树突状细胞(follicular DC , FDC)虽呈树突状形态,但不具备抗原提呈能力,可通过负载抗原 肤刺激生发中心B 细胞发生体细胞超突变。
(二)经典DC 的成熟过程
从骨髓造血干细胞分化而来的DC 前体细胞表达多种趋化因子受体,经血液进入各种实体器官和上皮组织,成为未成熟DC(immature DC) 。 未成熟DC 摄取抗原后迁移到外周免疫器官成为成熟 DC( 图 11-1,表11-1 ) 。
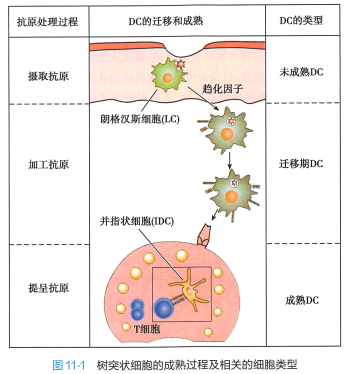

未成熟DC 未成熟DC 主要存在于各组织器官,包括分布千皮肤和黏膜的朗格汉斯细胞 (Langerhans cell , LC) 和分布于多种非免疫器官组织间质的间质DC(interstitial DC)等,其特点是:1)表达模式识别受体,能有效识别和摄取外源性抗原;2)具有很强的抗原加工能力;3)低水平表达MHCII 类分子和共刺激分子、黏附分子,故提呈抗原和激发免疫应答的能力较弱。
2. 迁移期DC 未成熟DC 在各组织器官中接触和摄取抗原或受到某些炎性刺激(如LPS、 IL-1β 、 TNF-α 等)后表达特定趋化因子受体(如CCR7) , 在趋化因子的作用下发生迁移(migration) , 由外 周组织器官(获取抗原信号)通过输入淋巴管和(或)血液循环进入外周淋巴器官。 未成熟DC 在迁移 的过程中逐渐成熟。
3. 成熟DC 迁移到外周免疫器官的DC 已是成熟DC(mature DC) , 其特点是:(j)表面有许多树 突样突起;@低表达模式识别受体,识别和摄取外源性抗原的能力弱;@加工抗原的能力弱;@高水平 表达MHCII 类分子和共刺激分子、黏附分子,故能有效提呈抗原和激活T 细胞,启动适应性免疫应 答。 外周免疫器官T 细胞区的并指状DC(interdigitating DC , IDC) 即属成熟DC。
不同组织器官中也有不同作用的成熟DC。 例如黏膜中的DC 在局部摄取抗原并发育成熟和提呈抗原,诱导黏膜局部的免疫应答;胸腺DC 摄取自身抗原并发育成熟,提呈抗原给未成熟T 细胞,诱导T 细胞的中枢免疫耐受。 外周免疫器官中也存在未成熟DC,可识别和摄取进入淋巴结或脾脏的抗 原并发育成熟和提呈抗原,启动适应性免疫应答。
(三) DC 的功能
DC 在机体的多种生理和病理过程中发挥关键作用,通过人为调节DC 的功能可增强或者抑制机体的免疫应答,对肿瘤、移植排斥、感染、自身免疫病发生机制的认识及其免疫防治具有重要价值。
1. 识别和摄取抗原,参与固有免疫应答 DC 表达多种模式识别受体(如甘露糖受体、Toll 样受体)以及Fc 受体,可识别多种病原微生物或抗原-抗体复合物,通过胞饮作用、吞噬作用、受体介导的 内吞作用I型 干扰素,参与抗病毒固有免疫应答。
2. 加工和提呈抗原,启动适应性免疫应答 这是DC 最重要的功能。 摄取和加工抗原后,DC 将 抗原以抗原肤-MHC II 类分子复合物的形式表达在细胞膜上,并提呈给CD4+T 细胞,提供初始T 细胞 活化的启动信号(或抗原刺激信号、第一信号)。 成熟DC 还高表达CD80、 CD86、 CD40 等共刺激分子, 为T 细胞充分活化提供了第二信号。 DC 产生的细胞因子进一步诱导活化T 细胞增殖和分化,从而完 整启动免疫应答。 DC 高表达ICAM-1 等黏附分子使之与T 细胞牢固结合,有利于细胞之间的相互作 用。 与已活化的或记忆T 细胞不同,初始T 细胞的活化更依赖千DC 刺激信号的存在,因此,DC 是唯 一能直接激活初始T 细胞的专职性APC。 DC 亦能以抗原肽-MHC I 类分子复合物的形式将抗原肤提 呈给CD8+T 细胞并激活之。
此外,DC 还能通过诱导lg 的类别转换和释放某些可溶性因子等促进B 细胞的增殖与分化,参与 体液免疫应答。
3. 免疫调节作用 DC 能够分泌多种细胞因子和趋化因子,通过细胞间直接接触的方式或者可 溶性因子间接作用的方式,调节其他免疫细胞的功能,例如DC 分泌大量IL-12 诱导初始T 细胞(Th0) 分化为Th1 细胞,产生Th1 型免疫应答。
4. 诱导与维持免疫耐受 未成熟DC 参与外周免疫耐受的诱导。 胸腺DC 是胸腺内对未成熟T 细胞进行阴性选择的重要细胞,通过清除自身反应性T 细胞克隆,参与中枢免疫耐受的诱导。
二、 单核/巨噬细胞
单核细胞(monocyte)来源于骨髓,从血液移行到全身组织器官,成为巨噬细胞(macrophage, MΦ) 。 单核/巨噬细胞表达多种受体(包括补体受体、Fc 受体、清道夫受体、模式识别受体等),可通过胞饮作 用吞噬作用、受体介导的内吞作用等摄取抗原物质,其吞噬和清除病原微生物能力很强。
大多数单核/巨噬细胞低水平表达MHC I 类分子、II 类分子和共刺激分子,虽然其摄取和加工抗 原的能力很强,但提呈抗原的能力很弱。 IFN-γ 等可诱导单核/巨噬细胞表达这些分子的水平升高, 抗原提呈功能增强,激活T 细胞产生细胞因子,后者进一步激活单核/巨噬细胞,使其发挥更强的清除 被吞噬病原体的能力。
三、 B 细胞
作为专职性APC,B 细胞主要以BCR 识别、浓集和内化抗原,亦可通过胞饮作用摄取抗原。 浓集抗原的效应使B 细胞在抗原浓度极低时仍能够提呈抗原。 B 细胞将抗原加工成抗原肽后,以抗原肽- MHC II 类分子复合物的形式表达于细胞表面,提呈给Th。 在激活Th 的同时B 细胞本身也受到Th 的 辅助而活化并对TD 抗原应答产生抗体。 通常,B 细胞不表达CD80、CD86 等共刺激分子,但在细菌感染等刺激后或在Th 的辅助下可以表达。 B 细胞接受T 细胞提供的第二信号而完全活化,并在T 细胞 产生的细胞因子作用下增殖、分化、产生抗体和发挥体液免疫效应。
三种专职性APC 提呈抗原效应的比较如图11-2。