Ill 型超敏反应
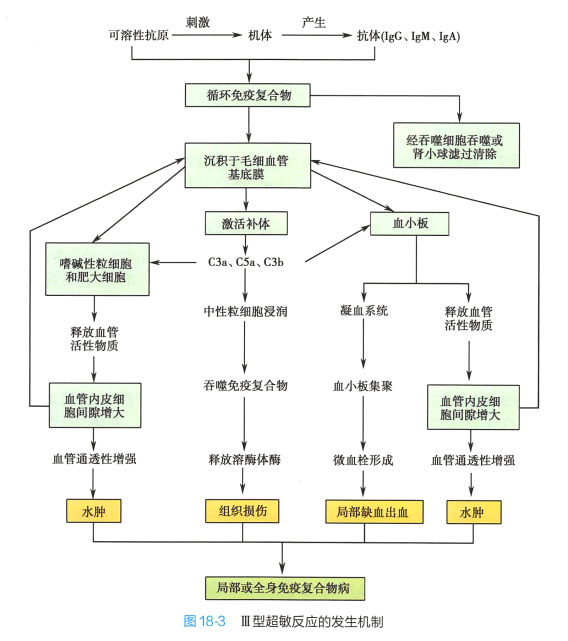
III型超敏反应是由抗原和抗体结合形成中等大小的可溶性免疫复合物沉积于局部或全身多处毛细血管基底膜后激活补体,并在中性粒细胞、血小板、嗜碱性粒细胞等效应细胞参与下,引起的以充血水肿、局部坏死和中性粒细胞浸润为主要特征的炎症反应和组织损伤。
—、发生机制
( 一) 可溶性免疫复合物的形成与沉积
血液循环中的可溶性抗原与相应抗体结合形成可溶性免疫复合物(immune complex,IC) 。 正常情况下机体通过单核-巨噬细胞吞噬可清除IC。 但在某些情况下,可溶性IC 不能被有效清除,沉积于 毛细血管基底膜引起炎症反应和组织损伤。
导致免疫复合物沉积的机制有:
1. 免疫复合物的特殊理化性质导致不被清除 1)抗原与抗体的比例影响IC 的大小:抗原抗体比例合适时,形成大分子的IC, 易被吞噬清除;抗原(或抗体)过剩则形成小分子IC,从肾小球滤过; 只有抗原抗体在一定比例形成约 1000kD 的中等分子量大小的IC 时, 才不易被吞噬,导致组织沉积。 2)免疫复合物的量过大、持续存在或吞噬细胞功能异常或缺陷,不能有效将其清除。 3)IC 的理化特点(荷电性、结合价、亲和力等)影响IC 的形成和沉积。 如荷正电的抗原( DNA 抗原等)形成的 IC 容 易与荷负电的肾小球基底膜结合,形成待久组织损伤。
2. 机体清除免疫复合物能力降低 IC 的清除主要通过调理吞噬和免疫黏附作用,补体、补体受体或FcγR 缺陷使清除IC 能力降低,导致血液中大量IC 存在。
3. 血管通透性等因素 1)血管通透性增加;IC 可激活补体产生过敏毒素( C3a 和C5a) 和C3b,使 肥大细胞、嗜碱性粒细胞和血小板活化,也可直接与血小板表面FcγR结合使之活化,释放组胺等血管活性物质。 高浓度血管活性物质可使血管内皮细胞间隙增大,血管通透性增加,有助于免疫复合物沉积。 2)血管内高压及形成涡流:肾小球基底膜和关节滑膜等处的毛细血管压较高,血流缓慢;动脉交叉口、脉络膜丛和眼睫状体等处易产生涡流。 血管内高压与涡流均有助于免疫复合物沉积。
(二)免疫复合物沉积引起的组织损伤
1. 补体的作用 免疫复合物通过经典途径激活补体,产生补体裂解片段C3a 和C5a。 C3a 和C5a与肥大细胞或嗜碱性粒细胞上的C3a 和C5a 受体结合,使其释放组胺等活性介质,致局部毛细血管通透性增加,渗出增多,出现水肿。 C3a 和C5a 同时又可趋化中性粒细胞到沉积部位。
2. 中性粒细胞的作用 聚集的中性粒细胞在吞噬免疫复合物的同时,释放多种溶酶体酶,包括蛋白水解酶、胶原酶和弹性纤维酶等,水解血管及局部组织。
3. 血小板和嗜碱性粒细胞的作用 肥大细胞或嗜碱性粒细胞活化释放的PAF 可损伤组织,使局部血小板集聚、激活,促进血栓形成,引起局部出血、坏死。 血小板活化还可释放血管活性胺类物质, 进一步加重水肿。
二、临床常见疾病
(一)局部免疫复合物病
1. Arthus 反应 是局部III型超敏反应。 用马血清经皮下免疫家兔数周后,再次重复注射同样血清后在注射局部出现红肿反应,3 -6 小时达到高峰。 红肿程度随注射次数增加而加重,注射5 -6 次后,局部出现缺血性坏死,反应可自行消退或痊愈,此为Arthus 反应。 其机制是,反复马血清免疫诱导机体产 生大量抗体,再次注射马血清后,抗体与局部抗原在血管壁相遇,结合成为IC 并沉积,引起局部血管炎。
2. 类Arthus 反应 胰岛素依赖型糖尿病患者局部反复注射胰岛素后可刺激机体产生相应IgG 类抗体,若再次注射胰岛素,在注射局部出现红肿、出血和坏死等类似Arthus 反应的炎症反应。 长期吸入抗原性粉尘、真菌袍子等,再次吸入相同抗原后也能在肺泡间形成IC, 引起过敏性肺泡炎。
(二)全身性免疫复合物病
1. 血清病 通常是在初次大量注射抗毒素(异种动物血清,如抗破伤风毒素和抗蛇毒血清)后1 -2 周发生,其主要临床症状是发热、皮疹、淋巴结肿大、 关节肿痛和一过性蛋白尿等。 这是由于患者体内新产生的针对抗毒素的抗体与大量未排除的抗毒素结合形成大量中等分子量的免疫复合物所 致。 血清病具有自限性,停止注射抗毒素后症状可自行消退。 临床应用抗TNF-α单抗、大剂量注射青霉素、磺胺等药物也可引起血清病样反应。
2. 链球菌感染导致的肾小球肾炎 一般发生于A 族溶血性链球菌感染后2 -3 周。 此时体内产生抗链球菌抗体,与链球菌可溶性抗原结合形成循环免疫复合物,沉积在肾小球基底膜上,引起免疫复合物型肾炎。 免疫复合物型肾小球肾炎也可在其他病原微生物如葡萄球菌、肺炎双球菌、 乙型肝炎病毒或疟原虫感染后发生。