T细胞的分类和功能
T细胞具有高度的异质性,按照不同的分类方法,T细胞可分为若干亚群,各亚群之间相互调节。共同发挥其免疫学功能。
一、根据所处的活化阶段分类
(一)初始T细胞
初始T细胞(naǐveTcell)是指从未接受过抗原刺激的成熟T细胞,处于细胞周期的G期存活期短,表达CD45RA和高水平的L-选择素(CD62L),参与淋巴细胞再循环,主要功能是识别抗原。初始T细胞在外周淋巴器官内接受DC提呈的pMHC刺激而活化,并最终分化为效应T细胞和记忆T细胞。
(二)效应T细胞
效应T细胞(effectorTcell,Teff)存活期短,除表达高水平的高亲和力IL-2受体外,还表达整合素,是行使免疫效应的主要细胞。效应T细胞主要是向外周炎症部位或某些器官组织迁移,并不再循环至淋巴结。
(三)记忆T细胞
记忆T细胞(memoryTcellTm)可由效应T细胞分化而来,也可由初始T细胞接受抗原刺激后直接分化而来。其存活期长,可达数年。再次接受相同抗原刺激后可迅速活化,并分化为效应T细胞。介导再次免疫应答。Tm表达CD45RO和黏附分子(如CD44),参与淋巴细胞再循环。即使没有抗原或 MHC 分子的刺激.Tm仍可长期存活,通过自发增殖维持一定数量。
二、根据 TCR 类型分类
(一)αβT细胞
αBT细胞即通常所称的T细胞,占脾脏、淋巴结和循环T细胞的95%以上。如未特指,本书所述的各类T细胞均为αBT细胞。
(二)γδT细胞
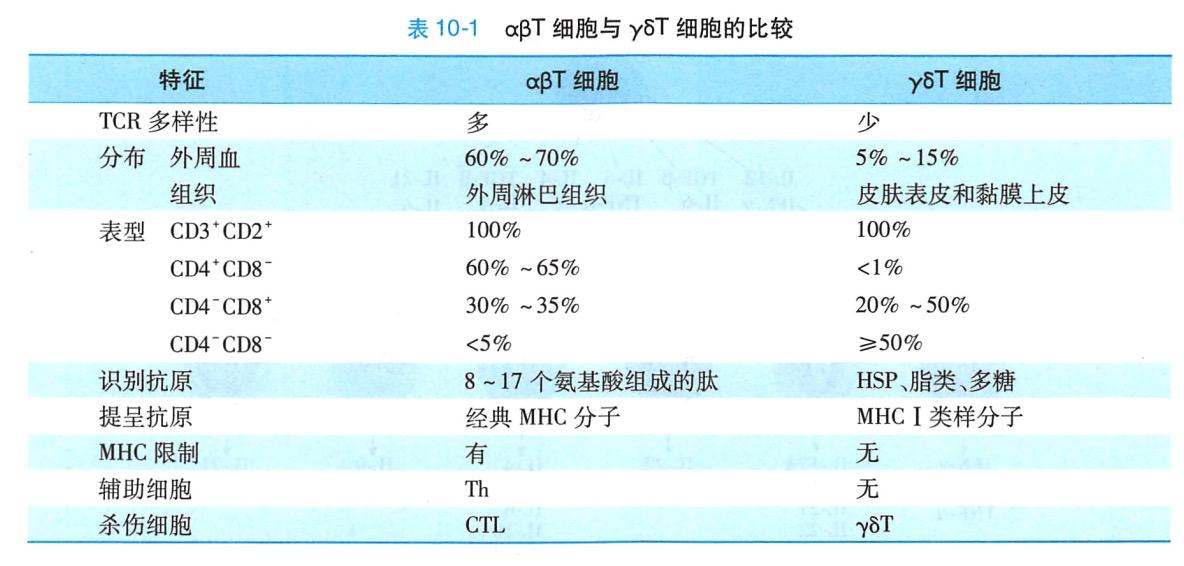
yST 细胞主要分布于皮肤和黏膜组织,其抗原受体缺乏多样性,识别抗原无 MHC 限制性,主要识别CD1分子提呈的多种病原体表达的共同抗原成分,包括糖脂、某些病毒的糖蛋白、分枝杆菌的磷酸糖和核苷酸衍生物、热休克蛋白(HSP)等。大多数γST细胞为CD4CD8,少数可表达CD8。γST细胞具有抗感染和抗肿瘤作用,可杀伤病毒或细胞内细菌感染的靶细胞,表达热休克蛋白和异常表达CD1分子的靶细胞,以及杀伤某些肿瘤细胞。活化的γsT细胞通过分泌多种细胞因子(包括IL-2、IL-3、IL-4、IL-5、IL-6、GM-CSF、TNF-Q、IFN-v等)发挥免疫调节作用和介导炎症反应。αβT细胞与ysT 细胞的特征及功能的比较列于表10-1。
三、根据 CD 分子分亚群
根据是否表达 CD4 或 CD8,T细胞分为 CD4 T细胞和CD8T细胞。
(一)CD4T细胞
CD4 表达于60%~65%T细胞及部分NKT细胞,巨噬细胞和树突状细胞亦可表达CD4,但表达水平较低。CD4*T细胞识别由13~17个氨基酸残基组成的抗原肽,受自身MHCⅡ类分子的限制,活化后,分化为Th细胞,但也有少数 CD4*效应T细胞具有细胞毒作用和免疫抑制作用。
(二)CD8T细胞
CD8 表达于30%~35%T细胞。CD8T细胞识别由8~10个氨基酸残基组成的抗原肽,受自身 MHCI类分子的限制,活化后,分化为细胞毒性T细胞(CTL),具有细胞毒作用,可特异性杀伤靶细胞。
四、根据功能特征分亚群
根据功能的不同,T细胞可分为Th、CTL和调节性T细胞。这些细胞实际上是初始CD4T细胞或初始CD8T细胞活化后分化成的效应细胞。NKT 细胞见第十四章。
(一)辅助T细胞(helper Tcell,Th)
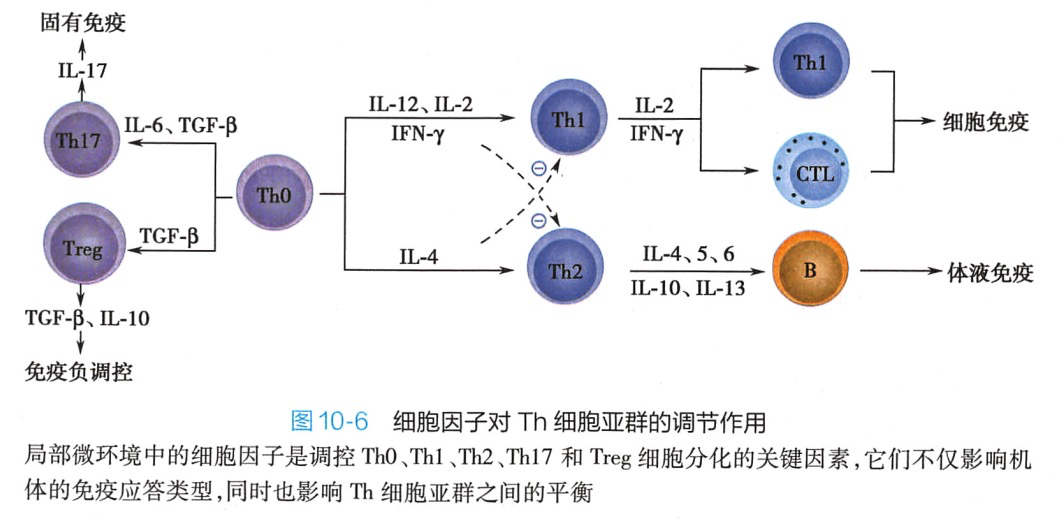
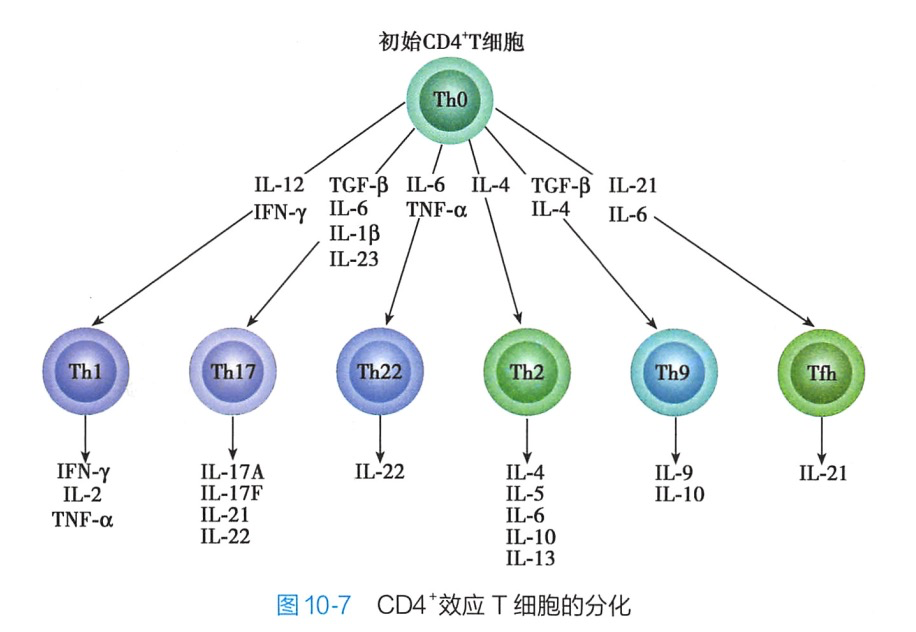
Th均表达CD4通常所称的 CD4T细胞即指 Th。未受抗原刺激的初始CD4T细胞为Th0。ThO向不同谱系的分化受抗原的性质和细胞因子等因素的调控,而最重要的影响因素是细胞因子的种类和细胞因子之间的平衡(图10-6)。例如.胞内病原体和肿瘤抗原以及IL-12、IFN-γ诱导Th0向Thl分化,其中IL-12 主要由 APC产生;普通细菌和可溶性抗原以及 IL-4 诱导 ThO 向 Th2分化,其中IL-4主要由局部环境中NKT细胞以及嗜酸性粒细胞和嗜碱性粒细胞等所产生;TGF-β和IL-4诱导Th0向 Th9分化;TGF-β和IL-6 诱导 Th0 分化为Th17;IL-6和TNF-α诱导 Th0分化为Th22;IL-21和IL-6诱导Th0分化为Tfh(图10-7)。除细胞因子外,APC表达的共刺激分子对Th0的分化方向亦发挥调节作用。例如,ICOS 可促进 Th2 的分化,而4-1BB与Th1 的分化有关。
1.Th1 主要分泌Th1型细胞因子.包括IFN-v、TNF-a、IL-2 等。它们能促进Th1的进一步增殖,进而发挥细胞免疫的效应,同时还能抑制 Th2 增殖。Thl细胞的主要效应是通过分泌的细胞因子增强细胞介导的抗感染免疫,特别是抗胞内病原体的感染。例如,IFN-γ活化巨噬细胞,增强其杀伤已吞噬的病原体的能力。IFN-γ还能促进IgG的生成。IL-2、IFN-γ和IL-12 可增强 NK细胞的杀伤能力。IL-2 和IFN-γ协同刺激 CTL的增殖和分化。 TNF-a除了直接诱导靶细胞凋亡外,还能促进炎症反应。另外,Th1也是迟发型超敏反应中的效应T细胞,故也称为迟发型超敏反应T细胞(T)。在病理情况下.Thl参与许多自身免疫病的发生和发展,如类风湿关节炎和多发性硬化症等。
2.Th2 主要分泌 Th2 型细胞因子,包括IL-4、IL-5、IL-6、IL-10 及IL-13 等。它们能促进Th2 细胞的增殖,进而辅助B细胞活化,发挥体液免疫的作用,同时抑制 Th1增殖。
Th2的主要效应是辅助B细胞活化,其分泌的细胞因子也可促进B细胞的增殖、分化和抗体的生成(见第十三章)。Th2在超敏反应及抗寄生虫感染中也发挥重要作用;IL-4和IL-5可诱导IgE 生成和嗜酸性粒细胞活化。特应性皮炎和支气管哮喘的发病与Th2 型细胞因子分泌过多有关。
3.Th9 通过分泌其特征性细胞因子IL-9在过敏性疾病、抗寄生虫感染和自身免疫病中发挥重要作用。Th9除可在TGF-β和IL-4共同存在时由ThO细胞分化形成,也可由 TGF-ß单独诱导Th2细胞分化而成。
4.Th17 通过分泌IL-17(包括IL-17A到IL-17F)、IL-21、IL-22、IL-26、TNF-等多种细胞因子参与固有免疫和某些炎症的发生,在免疫病理损伤,特别是自身免疫病的发生和发展中起重要作用。
5.Th22 是一群IL17A7IL-22IFN-v的Th.表达趋化因子受体CCR4.CCR6和CCR10通过分泌IL-22、IL-13和TNF-a参与上皮细胞的生理功能和炎性病理过程,特别是在炎性皮肤疾病(如牛皮癣和特应性皮炎)的免疫病理中发挥重要作用。
6.Tfh 滤泡辅助T细胞(follicular helper Tcell,Th)是一种存在于外周免疫器官淋巴滤泡的 CD4*T细胞,其产生的IL-21在B细胞分化为浆细胞、产生抗体和Ig类别转换中发挥重要作用,是辅助B细胞应答的关键细胞。需要指出的是,不同亚群的Th分泌不同的细胞因子只是反映了这些细胞处于不同分化状态,这种分化状态并非恒定不变,在一定条件下可以相互转变。
(二)细胞毒性T细胞(cvtotoxic Tlymphocyte,CTL)
CTL表达CD8.通常所称的CD8*T细胞即指 CTL,而同样有细胞毒作用的γST细胞和NKT细胞不属于 CTL。CTL的主要功能是特异性识别内源性抗原肽-MHCI类分子复合物,进而杀伤靶细胞(细胞内寄生病原体感染的细胞或肿瘤细胞)。杀伤机制主要有两种:一是分泌穿孔素(perforin)、颗粒酶(granzyme)、颗粒溶素(granulysin)等物质直接杀伤靶细胞;二是通过表达 FasL或分泌 TNF-α,分别与靶细胞表面的Fas或TNF受体(TNFR)结合,通过Fas-FasL途径或 TNF-TNFR途径诱导靶细胞凋亡。 CTL 在杀伤靶细胞的过程中自身不受伤害,可连续杀伤多个靶细胞。

(三)调节性T细胞(regulatoryTcell,Treg)
通常所称的Treg是CD4*CD25*Foxp3*的T细胞。Foxp3(forkhead box p3)是一种转录因子,不仅是Treg的重要标志,也参与 Treg 的分化和功能。Foxp3缺陷会使得 Treg减少或缺如,从而导致人、小鼠发生严重自身免疫病。Treg主要通过两种方式负调控免疫应答:①直接接触抑制靶细胞活化;②分泌TGF-B、IL-10等细胞因子抑制免疫应答。在免疫耐受、自身免疫病、感染性疾病、器官移植及肿瘤等多种疾病中发挥重要的作用。根据来源可分为两类(表10-2)。
自然调节性T细胞(natural Treg,nTreg)直接从胸腺分化而来,约占外周血CD4T细胞的5%~10%。
2.诱导性调节性T细胞(inducibleTrea,iTreg)或称适应性调节性T细胞(adaptive Treg),中初始 CD4T细胞在外周经抗原及其他因素(如TGF-B和IL2)诱导产生。
Tr1是iTreg的一个主要亚群,主要分泌IL-10及TGF-B,主要抑制炎症性自身免疫反应和由Thl介导的淋巴细胞增殖及移植排斥反应。此外,Tr1可通过分泌IL-10在防治超敏反应性疾病(如哮喘)中起作用。
3.其他调节性T细胞 在CD8T细胞中也存在一群 CD8调节性T细胞(CD8Treg),对自身反应性 CD4*T 细胞具有抑制活性,并可抑制移植物排斥反应。此外,Th1、Th2、IL-17*Treg、ICOS Treg、NK、NKT 以及 v8T 等细胞亚群也具有免疫调节活性。