B淋巴细胞(Blymphocyte)由哺乳动物骨髓(bonemarrow)或鸟类法氏囊(bursa of Fabricius)中的淋巴样干细胞分化发育而来,故称B细胞。成熟B细胞主要定居于外周淋巴器官的淋巴滤泡内,约占外周淋巴细胞总数的20%。B细胞不仅能通过产生抗体发挥特异性体液免疫功能,也是一类抗原提呈细胞,并参与免疫调节。
第一节 B细胞的分化发育
哺乳动物的B细胞是在中枢免疫器官--骨髓中发育成熟的。B细胞在中枢免疫器官中的分化发育过程中发生的主要事件是功能性B细胞受体(Bcellreceptor,BCR)的表达和B细胞自身免疫耐受的形成。骨髓微环境特别是基质细胞表达的细胞因子和黏附分子在诱导B细胞分化发育过程中发挥了关键作用。
一、BCR 的基因结构及其重排
BCR是表达于B细胞表面的免疫球蛋白,即膜型免疫球蛋白(membrane immunoglobulin,mIg)。B细胞通过BCR识别抗原,接受抗原刺激,启动体液免疫应答。编码BCR的基因群在胚系阶段是以分隔的、数量众多的基因片段(gene segment)的形式存在。基因重排(generearrangement)是在B细胞的分化发育过程中,BCR基因片段发生重新排列和组合,从而产生数量巨大、能识别特异性抗原的 BCR。TCR和BCR 基因结构以及重排的机制十分相似。
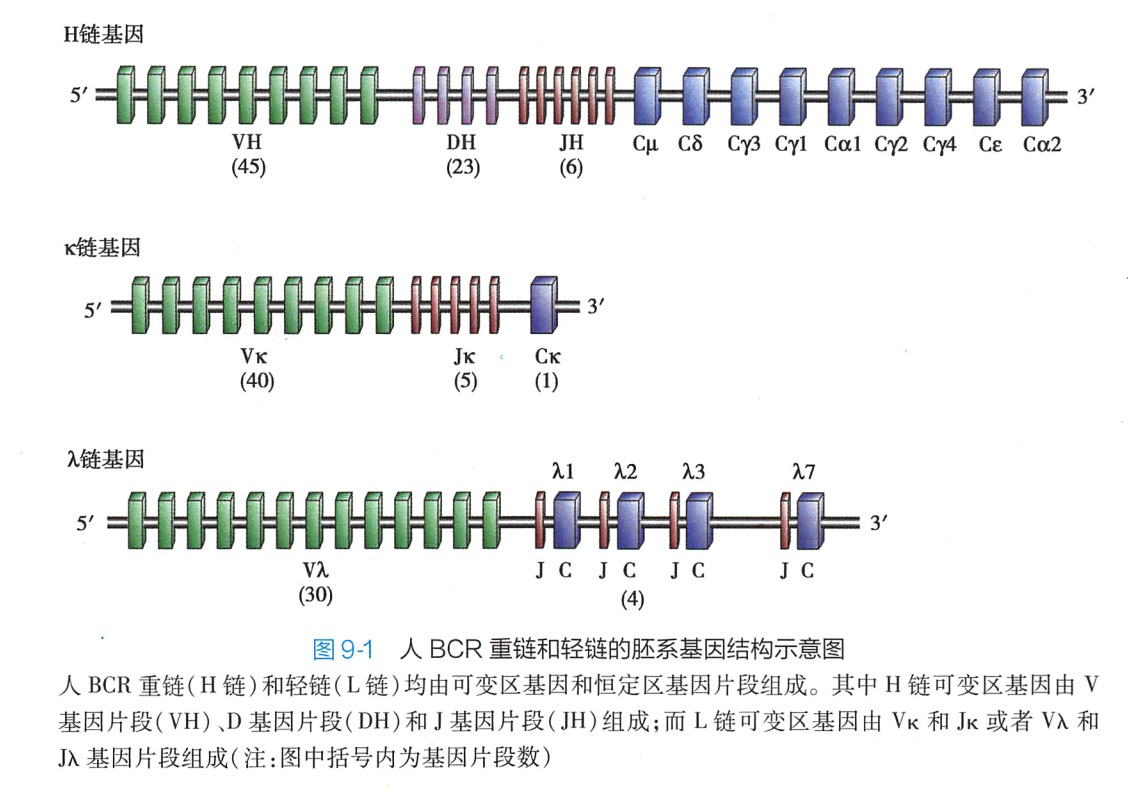
1.BCR的胚系基因结构 人Ig重链基因群位于第14号染色体长臂,由编码可变区的V基因片段(variable gene segment,VH)、D基因片段(diversity gene segment,DH)和J基因片段(joining gene seg ment.JH)以及编码恒定区的C基因片段组成。人Ig轻链基因群分为k基因和入基因,分别定位于第2号染色体短臂和第22号染鱼休长臂。轻链V区基因只有VI基因片段。轻重链基因分别有多个基因片段组成,其中人的VHDH和H的基因片段数分别为45、23和6个;Vκ和JK基因片段数分别为40和5个Vλ和Jλ基因片段数分别为30和4个;重链C基因片段有9个,其排列顺序是5'-Cμ-Cδ-Cγ3-Cγ1-Ca1-Cγ2-Cγ4-Cε-Ca2-3'(图9-1)。Cκ基因片段数只有1个. Cλ基因片段数有4个(Cλ1、Cλ2、Cλ3和Cλ7)。
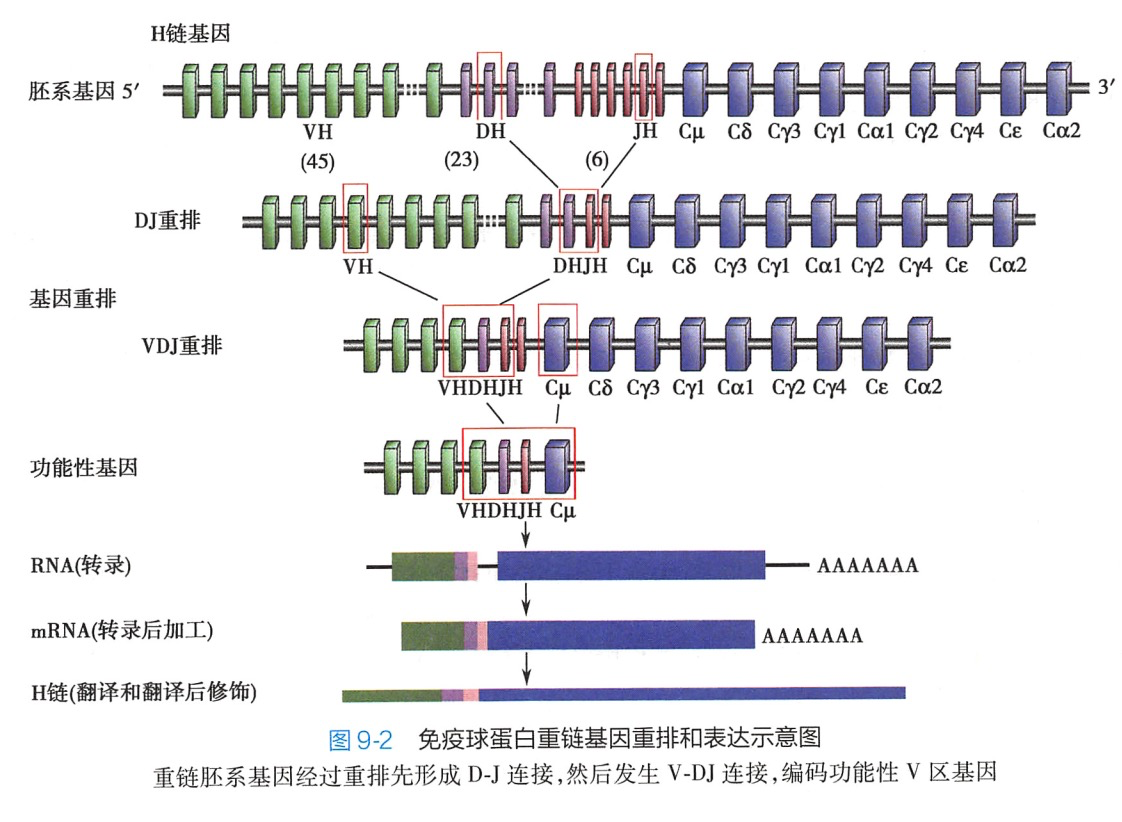
2.BCR的基因重排及其机制 Ig的胚系基因是以被分隔开的基因片段的形式成簇存在的,只有通过基因重排形成 V-D-J(重链)或V-J(轻链)连接后,再与C基因片段连接,才能编码完整的Ig多肽链,进一步加工、组装成有功能的BCR。IgV区基因的重排主要是通过重组酶(recombinase)包括重组激活酶基因(recombination activating gene,RAG)和末端脱氧核苷酸转移酶(terminal deoxyribonucle otidyl transferase,TdT)等的作用来实现的,其作用包括识别位于V(D)J基因片段两端的保守序列,切断、连接以及修复 DNA 等。
通过重组酶的作用,可以从众多的V(D)J基因片段中各选择1个V片段,1个D片段(轻链无D片段)和1个J片段重排在一起,形成V(D)J连接(图9-2),最终表达为有功能的BCR。Ig胚系基因重排的发生具有明显的程序化,首先是重链可变区发生基因重排,随后是轻链重排。经过Ig 胚系基因的重排,B细胞的DNA序列与其他体细胞有很大不同,这是存在于B细胞和T细胞中独特的生物学现象。
3.等位排斥(allelic exclusion)和同种型排斥(isotype exclusion) 一个B细胞克隆只表达一种BCR只分泌一种抗体。对干遗传上是杂合子的个体来说,保证B细胞克隆单一的特异性以及只表达一种Ig型的轻链,主要是通过等位排斥和同种型排斥的机制来实现的。等位排斥是指B细胞中一条染色体上的重链(或轻链)基因重排成功后,抑制另一条同源染色体上重链(或轻链)基因的重排。同种型排斥是指κ轻链基因重排成功后抑制入轻链基因的重排。
二、抗原识别受体多样性产生的机制
免疫系统中T细胞库和B细胞库分别包含了所有特异性不同的T细胞克隆和B细胞克隆。这和抗原识别受体的多样性在基因重排过程中产生,其机制主要包括组合多样性、连接多样性、受体编辑和体细胞高频突变。
组合多样性(combinationaldiversity) 指在免疫球蛋白 V、(D)、J基因片段重排时,只能分别在众多V、(D)、J基因片段中各取用1个,因而可产生众多V区基因片段组合。以人类Ig 重链 V区为例,其排列组合的种类可达40(VH)x25(VD)x6(VJ)=6000之多。以此类推,Vκ和Vλ的V基因片段的组合种类分别达200种和120种。理论上IgV区基因片段的组合加上轻重链组合后的多样性约为1.9x10^6。
2.连接多样性(iunctional diversitv)Ig基因片段之间的连接往往有插人、替换或缺失核苷酸的情况发生,从而产生新的序列,称为连接多样性。连接多样性包括:①密码子错位,在待接DNA断端替换或缺失3xn个核苷酸,使其产物增加或减少n个氨基酸,后续序列不变:2框架移位,替换或缺失1或2+3xn个核苷酸,后续序列完全改变;③N序列插人,TdT能将N序列插人待接DNA的断端,从而显著增加了 BCR 和Ig 的多样性。
3.受体编辑(receptorediting)指一些完成基因重排并成功表达BCR(mIgM)的B细胞识别自身抗原后未被克隆清除,而是发生RAG基因重新活化,导致轻链VJ再次重排,合成新的轻链,替代自身反应性轻链,从而使BCR获得新的特异性。若受体编辑不成功,则该细胞凋亡。受体编辑使 BCR的多样性进一步增加。
4.体细胞高频突变(somatic hypermutation)体细胞高频突变形成的多样性是在已完成Ig基因重排的基础上,成熟B细胞在外周淋巴器官生发中心接受抗原刺激后发生。体细胞高频突变主要是在编码V区CDR部位的基因序列发生碱基的点突变。体细胞高频突变不仅能增加抗体的多样性,而且可导致抗体的亲和力成熟。
三、B细胞在中枢免疫器官中的分化发育
B细胞在骨髓中的发育经历了祖B细胞(pro-Bcell)、前B细胞(pre-Bcell)、未成熟B细胞(im mature B cell)和成熟B细胞(mature Bcell)等几个阶段。
1.祖B细胞 早期pro-B开始重排重链可变区基因D-J,晚期pro-B的V-D-J基因发生重排,但此时没有mIgM的表达。pro-B开始表达Iga/Igβ异源二聚体,是B细胞的重要标记。Iga/Igβ是BCR复合物的组成部分,主要介导抗原刺激后的信号传递。
2.前B细胞 前B细胞的特征是表达前B细胞受体(pre-BCR)(图9-3),并经历大pre-B和小 pre-B两个阶段。pre-BCR由μ链和替代轻链(surrogate light chain,包括分别与轻链V区和C区同源的VpreB和λ5两种蛋白)组成,可抑制另一条重链基因的重排(等位基因排斥),促进B细胞的增殖。大pre-B细胞进一步发育成为小pre-B细胞,小pre-B细胞开始发生轻链基因V-J重排,但依然不能表达功能性 BCR。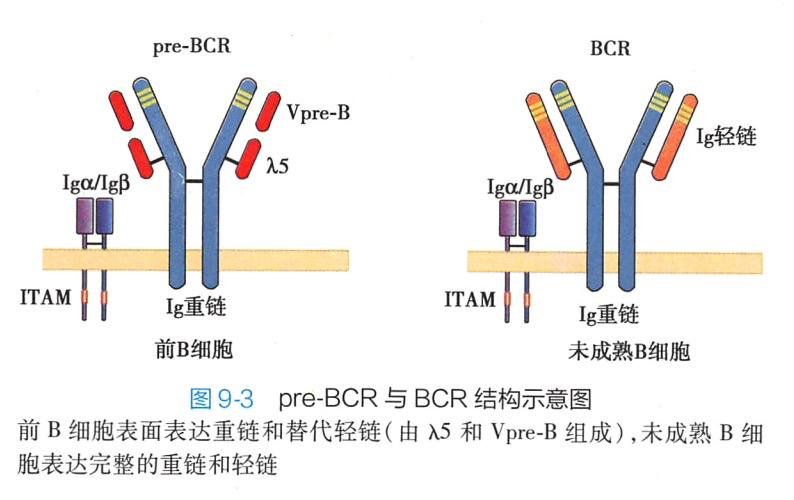
3.未成熟B细胞 未成熟B细胞的特征是可以表达完整BCR(mIgM),此时如受抗原刺激,则引发凋亡而导致克隆清除,形成自身免疫耐受。
4.成熟B细胞 又称初始B细胞(nafveBcell)。成熟B细胞表面可同时表达mIgM和mIgD,其可变区完全相同。
B细胞在骨髓的分化发育过程不受外来抗原影响,称为B细胞分化的抗原非依赖期。B细胞在骨髓微环境诱导下发育为初始B细胞,离开骨髓,到达外周免疫器官的B细胞区定居,在那里接受外来抗原的刺激而活化、增殖,进一步分化成熟为浆细胞和记忆B细胞(图9-4),此过程称为B细胞分化的抗原依赖期。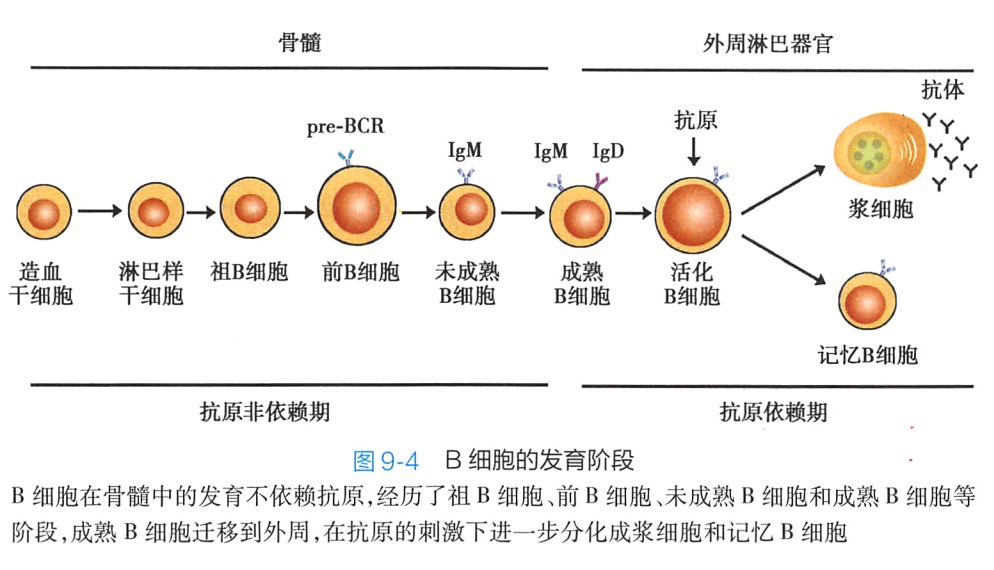
四、B 细胞中枢免疫耐受的形成--B 细胞发育过程中的阴性选择
前B细胞在骨髓中发育至未成熟B细胞后,其表面仅表达完整的 mlgM。此时的mlgM 若与骨髓中的自身抗原结合,即导致细胞凋亡,形成克隆清除(clonal deletion)。一些识别自身抗原的未成熟B细胞可以通过受体编辑改变其BCR的特异性。在某些情况下,未成熟B细胞与自身抗原的结合可引起 mIgM 表达的下调,这类细胞虽然可以进入外周免疫器官,但对抗原刺激不产生应答,称为失能(anergy)。在骨髓中发育的未成熟B细胞通过上述的克隆清除、受体编辑和失能等机制形成了对自身抗原的中枢免疫耐受,成熟的B细胞到达外周淋巴组织后仅被外来抗原激活,产生B细胞适应性免疫应答。