第二节 外周免疫器官和组织
外周免疫器官(peripheral immune organ) 或称次级淋巴器官(secondary
lymphoid organ) , 是成熟淋巴细胞(T细胞、 B细胞)定居的场所,也是淋巴细胞对外来抗原产生免疫应答的主要部位。 外周免疫
器官包括淋巴结、 脾和位于胃肠道、呼吸道及泌尿生殖道的黏膜相关淋巴组织等。
一、 淋巴结
淋巴结(lymph node)
是结构最完备的外周免疫器官,广泛分布于全身非黏膜部位的淋巴通道汇 集处。 身体浅表部位的淋巴结常位于凹陷隐蔽处(如颈部、腋窝、腹股沟等)
;内脏的淋巴结多成群分布于器官门附近,沿血管干排列,如肺门淋巴结。 组织或器官的淋巴液均引流至局部淋巴结,局部淋
巴结肿大或疼痛通常提示引流区域内的器官或组织发生炎症或其他病变。
(一)淋巴结的结构
淋巴结(lymph node) 实质分为皮质区和髓质区两个部分(图2~4) 。
1. 皮质 皮质分为浅皮质区和深皮质区。 靠近被膜下为浅皮质区,是B 细胞定居的场所,称为非胸腺依赖区(thymus-independent area) 。 在该区内,大量 B 细胞聚集成初级淋巴滤泡(primary lymphoid follicle) , 或称淋巴小结(lymphoid nodule) 。 初级淋巴滤泡主要含未受抗原刺激的初始B 细 胞,无生发中心。 受抗原刺激后,淋巴滤泡内出现生发中心(germinal center, GC) , 称为次级淋巴滤泡 (secondary lymphoid follicle) , 内含大量增殖分化的B 淋巴母细胞,后者可向内转移至淋巴结中心部髓质的髓索,分化为浆细胞并产生抗体。 B 细胞缺陷时,皮质缺乏初级淋巴滤泡和生发中心。
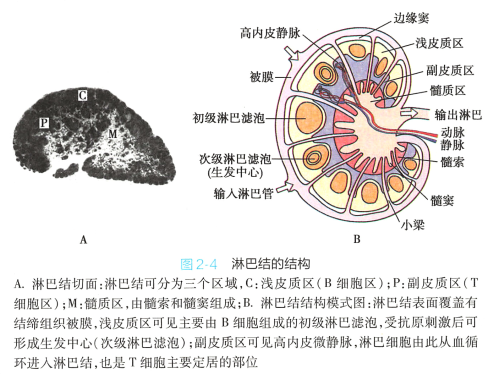
浅皮质区与髓质之间的深皮质区又称副皮质区(paracortex) , 是T细胞定居的场所,称为胸腺依赖区(thymus-dependent area) 。 副皮质区含有自组织迁移而来的DC,高表达MHCII
类分子,是专职的 抗原提呈细胞。 副皮质区有由内皮细胞组成的、呈非连续状的毛细血管后微静脉(post-capillary
venule,PCV), 也称高内皮微静脉(high endothelial venule, HEV) , 是沟通血液循环和淋巴循环的重要
通道,血液中的淋巴细胞由此部位可进入淋巴结实质。
2. 髓质 髓质由髓索和髓窦组成。 髓索由致密聚集的淋巴细胞组成,主要为B 细胞和浆细胞, 也含部分T 细胞及Mϕ 。 髓窦内富含Mϕ ,有较强的捕捉、 清除病原体的作用。
(二)淋巴结的功能
1. T 细胞和B 细胞定居的场所 淋巴结是成熟T 细胞和B 细胞的主要定居部位。 其中,T 细胞约占淋巴结内淋巴细胞总数的75% ,B 细胞约占25% 。
2. 免疫应答场所 淋巴结是淋巴细胞接受抗原刺激、发生适应性免疫应答的主要部位之一。 存在于组织中的游离抗原经淋巴液进入局部引流淋巴结,可被副皮质区内APC
摄取,或抗原在组织中被APC 摄取,随后APC 迁移至副皮质区,将加工后的抗原肤提呈给T 细胞,使其活化、增殖,分化为效 应性Th
细胞;通过T-B 细胞的相互作用,B 细胞在浅皮质区大量增殖形成生发中心,并分化为浆细 胞。
浆细胞一部分迁移至髓质区并分泌抗体,其寿命较短,而大部分浆细胞则经输出淋巴管一胸导管
一血循环,迁移至骨髓,长期、持续性产生高亲和力抗体,成为抗体的主要来源。 效应T 细胞除在淋巴
结内发挥免疫效应外,也是经输出淋巴管一胸导管,进入血循环并分布于全身,发挥免疫效应。
3. 过滤作用 淋巴结是淋巴液的有效过滤器。 侵入机体的病原微生物、毒素或其他有害异物,通常随淋巴液进入局部引流淋巴结。 淋巴液在淋巴窦中缓慢移动,有利于窦内Mϕ 吞噬、 杀伤病原微生物,清除抗原性异物,从而起到净化淋巴液、防止病原体扩散的作用。
4. 参与淋巴细胞再循环 淋巴结副皮质区的HEV 在淋巴细胞再循环中起重要作用。 随血流而来的T 细胞和B 细胞穿过HEV,分别进入副皮质区和浅皮质区,再迁移至髓窦,经输出淋巴管汇入胸导管,最终经左锁骨下静脉返回血液循环。
二、 脾
脾(spleen) 是胚胎时期的造血器官,自骨髓开始造血后,脾演变成人体最大的外周免疫器官。 脾在结构上不与淋巴管道相连,也无淋巴窦,但含有大量血窦。
(—)脾的结构
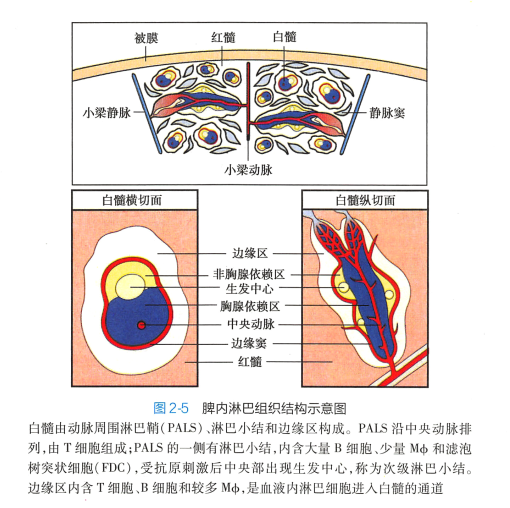
脾外层为结缔组织被膜,被膜向脾内伸展形成若干小梁,后者在脾内反复分支,形成纤维网状结构,对脾内的淋巴组织(白髓)和充满血液的红髓起支持作用。 脾实质可分为白髓和红髓(图2-5 ) 。
1. 白髓 白髓(white pulp) 为密集的淋巴组织,由围绕中央动脉而分布的动脉周围淋巴鞘(periarteriolar
lymphoid sheaths, PALS) 、脾小结(splenic nodule) 和边缘区(marginal zone)
组成,相当于淋巴结的皮质。 脾动脉入脾后,分支成为小梁动脉,小梁动脉继续分支进入脾实质,称为中央动脉。 包裹 中央动脉的PALS
是厚层弥散淋巴组织,由密集的T 细胞、 少量DC 及Mϕ 构成,为T 细胞区。 PALS 的旁侧有脾小结,内含大量B 细胞及少量Mϕ 和FDC,为B 细胞区。 未受抗原刺激时脾小结为初级淋巴滤泡,受抗原刺激后中央部出现生发中心,为次级淋巴滤泡。
白髓与红髓交界的狭窄区域为边缘区,内含T 细胞、B 细胞和较多Mϕ 。 中央动脉的侧支末端在此处膨大形成边缘窦(marginal sinus) 。 边缘窦内皮细胞之间存在间隙,是淋巴细胞由血液进入淋巴 组织的重要通道。 T 细胞经边缘窦迁入PALS,而B 细胞则迁入脾小结和脾索。 白髓内的淋巴细胞也可进入边缘窦,参与淋巴细胞再循环。
2 . 红髓 白髓和边缘区外侧的广大区域为红髓,由脾索和脾血窦(splenic sinus) 组成。 脾索为索条状组织,主要含B 细胞、浆细胞、Mϕ和DC。 脾索之间为脾血窦,其内充满血液。 脾血窦汇入小梁 静脉,再千脾门汇合为脾静脉出脾。 脾索和脾血窦中的Mϕ 能吞噬和清除衰老的血细胞、抗原抗体复合物或其他异物,并具有抗原提呈作用。
(二)脾的功能
1. T 细胞和B 细胞定居的场所 脾是成熟淋巴细胞定居的场所。 其中,B 细胞约占脾淋巴细胞 总数的60% ,T 细胞约占40% 。
2.
免疫应答发生的场所 脾也是淋巴细胞接受抗原刺激并发生免疫应答的重要部位。 作为外
周免疫器官,脾与淋巴结的主要区别在于:脾是对血源性抗原产生免疫应答的主要场所,而淋巴结主 要对由引流淋巴液而来的抗原产生应答。
脾是体内产生抗体的主要器官,在机体的防御、免疫应答中 具有重要地位。
3. 合成生物活性物质 脾可合成并分泌某些重要生物活性物质,如补体成分和细胞因子等。
4. 过滤作用 体内约90% 的循环血液流经脾,脾内的Mϕ 和DC 均有较强的吞噬作用,可清除血液中的病原体、衰老死亡的自身血细胞、免疫复合物以及其他异物,从而发挥过滤作用,使血液得到净化。
三、黏膜相关淋巴组织
黏膜相关淋巴组织(
mucosal-associated lymphoid tissue, MALT)亦称黏膜免疫系统(mucosal immune
system, MIS) , 主要指胃肠道、呼吸道及泌尿生殖道黏膜固有层和上皮细胞下散在的淋巴组织,以及带
有生发中心的淋巴组织,如扁桃体、小肠派尔集合淋巴结(Peyer patches , PP) 及阑尾等,是发生黏膜免疫应答的主要部位。
黏膜是病原体等抗原性异物入侵机体的主要部位,人体黏膜表面积约400平方米 , 机体近50% 的淋巴组织分布于黏膜系统,故MALT构成了人体重要的防御屏障。
( — ) MALT 的组成
MALT主要包括肠相关淋巴组织、鼻相关淋巴组织和支气管相关淋巴组织等。
1. 肠相关淋巴组织 肠相关淋巴组织(gut-associated lymphoid tissue, GALT) 是位于肠黏膜下的淋巴组织,由 PP、阑尾、孤立淋巴滤泡、上皮内淋巴细胞及固有层中弥散分布的淋巴细胞组成,主要作用是抵御肠道病原微生物感染。
GALT 中的PP 和上皮内淋巴细胞在摄取肠道抗原及黏膜免疫应答中发挥重要作用。
(1) 派尔集合淋巴结(PP) :PP 属小肠黏膜淋巴滤泡组织,是发生肠黏膜免疫应答的重要部位。在PP
处,肠黏膜向肠腔呈圆顶状隆起,由一层滤泡相关上皮(follicle-associated epithelium, FAE) 将其 与肠腔隔离。
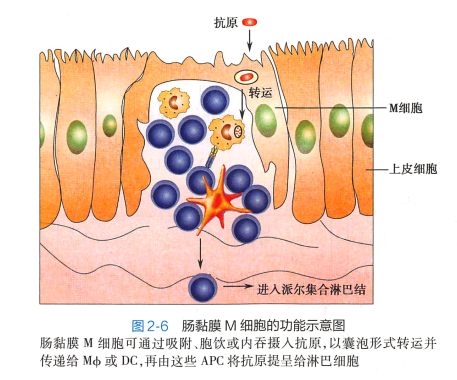
FAE 主要由肠上皮细胞构成,其中散在少数微皱褶细胞(microfold cell, M 细胞)(图2-6) 。 M
细胞是一种特化的抗原转运细胞,无微绒毛,不能分泌消化酶和黏液。 这些结构特点使其很容
易与小肠腔内微生物和颗粒接触,便于肠腔中的抗原由此进入派尔集合淋巴结。 M 细胞基膜向细胞 内凹陷形成口袋,其内有T 细胞、B
细胞、Mϕ 和DC。 M 细胞可通过吸附、胞饮和内吞等方式摄取肠腔 内抗原性异物,并以襄泡形式转运给口袋内的Mϕ
或DC。 Mϕ或DC 识别抗原后进入PP,激活T、 B 细 胞,从而启动肠道黏膜免疫应答。激活的T、 B
细胞也可进入肠系膜淋巴结并最终进入血循环。 因此, GALT 不仅参与肠道局部免疫,而且与全身免疫系统密切相关。
(2)
上皮内淋巴细胞(intraepithelial lymphocyte, IEL) : IEL 位于肠黏膜上皮细胞之间,主要为T 细 胞。
其中,约40% 的IEL 为αβT 细胞,可能是PP 中的T 细胞受抗原刺激后增殖,然后通过淋巴循环 和血液循环迁移至肠上皮。
因此,其数最多少与抗原的刺激有关。 另外,约60% 的IEL 为 γδT 细胞, 这类T
细胞为胸腺非依赖性,以造血前体的形式不经胸腺而直接由骨髓迁移至肠上皮,并在肠上皮提 供的微环境中分化成熟。 γδT
细胞属固有免疫细胞,具有较强的细胞毒作用,并能分泌多种细胞因 子。 IEL 在免疫监视和细胞介导的黏膜免疫中具有重要作用。
2. 鼻相关淋巴组织 鼻相关淋巴组织(nasal-associated lymphoid tissue, NALT) 包括咽扁桃体、腮扁桃体、舌扁桃体及鼻后部淋巴组织,其主要作用是抵御经空气传播的病原微生物的感染。 NALT 由 淋巴小结及弥散的淋巴组织组成。 NALT 表面覆盖有上皮细胞,但无结缔组织被膜,也无输入淋巴管。 抗原和异物陷入淋巴上皮隐窝中,然后被送至淋巴小结。 淋巴小结主要由B 细胞组成,受抗原刺激后 增殖,形成生发中心。
3. 支气管相关淋巴组织 支气管相关淋巴组织(bronchial-associated tissue, BALT) 主要分布千各 肺叶的支气管上皮下,其结构与派尔集合淋巴结相似,滤泡中的淋巴细胞受抗原刺激后增殖,形成生 发中心,其中主要为B 细胞。
(二) MALT 的功能及其特点
1. 行使黏膜局部免疫应答 MALT 在肠道、呼吸道及泌尿生殖道黏膜构成了一道免疫屏障,是行使局部免疫应答的主要部位,在黏膜局部抗感染免疫防御中发挥关键作用。 MALT 与肠道正常菌群 相互作用,对维持生理状态下的肠道自稳有重要意义。
2.
产生分泌型lgA MALT 中的B 细胞多为产生分泌型IgA(SigA) 的B 细胞,这是因为表达IgA 的B
细胞可趋向定居千派尔集合淋巴结和肠黏膜固有层淋巴组织; 另外,与淋巴结和脾相比,派尔集 合淋巴结含有更多可产生大量IL-5 的Th2
细胞,而IL-5 可促进B 细胞分化并产生IgA。 SigA 经黏膜 上皮细胞分泌至肠黏膜表面,成为肠道局部黏膜免疫的主要效应分子。
在肠黏膜淋巴组织中产生的 部分幼浆细胞(proplasmacyte) 可经血液循环进入唾液腺、呼吸道黏膜、女性生殖道黏膜和乳腺等部
位,产生SigA,发挥相似的免疫作用,使肠道免疫成为全身免疫的一部分。