免疫系统(immune system) 是由免疫器官和组织、免疫细胞(如淋巴细胞、树突状细胞、NK 细胞、 单核巨噬细胞、粒细胞、肥大细胞等)及免疫分子(如免疫球蛋白、补体、各种膜分子及细胞因子等)组成,其主要作用是执行免疫功能。 本章重点介绍免疫器官和组织的结构与功能,免疫细胞和免疫分子 将在后续相关章节分别介绍。
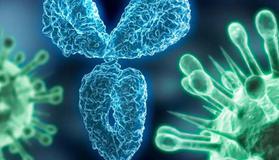
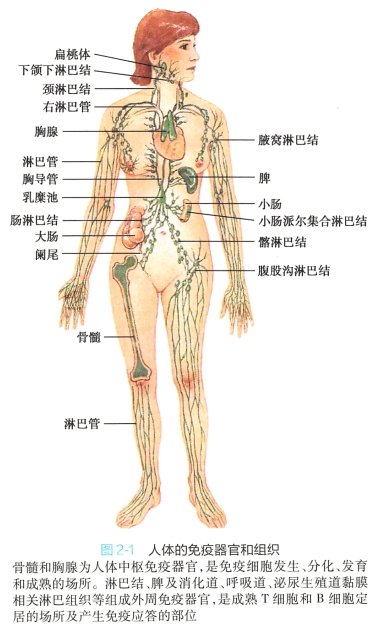
免疫组织(imnmne tissue) 又称为淋巴组织(Iymphoid tissue) , 在人体广泛分布,其中胃肠道、呼吸道、 泌尿生殖道等黏膜下含有大量弥散淋巴组织和淋巴小结(lymphoid nodule) , 在黏膜抗感染免疫中发挥主 要作用。 骨髓、胸腺、脾脏、淋巴结等属于免疫器官( immune organ) , 又称为淋巴器官(lymphoid organ) 。免疫器官按其功能不同,可分为中枢免疫器官和外周免疫器官(图2-1) , 二者通过血液循环及淋 巴循环互相联系并构成免疫系统的完整网络。
第一节 中枢免疫器官
中枢免疫器官(central immune organ) 或称初级淋巴器官(primary lymphoid organ) , 是免疫细胞发生、分化、发育和成熟的场所。 人和其他哺乳类动物的中枢免疫器官包括骨髓和胸腺。
—、骨髓
骨髓( bone marrow) 是各类血细胞(包括免疫细胞)的发源地,也是人类和其他哺乳动物B 细胞发育成熟的场所。
(—)骨髓的结构和细胞组成
骨髓位于骨髓腔内,分为红骨髓和黄骨髓。 红骨髓具有活跃的造血功能,由造血组织和血窦构成。 造血组织主要由造血细胞和基质细胞组成。 基质细胞包括网状细胞、成纤维细胞、血窦内皮细胞、巨噬细胞等。由基质细胞及其所分泌的多种造血生长因子(如IL-3 、 IL-4 、 IL-6 、 IL-7 、 SCF、 GM-CSF 等)与细胞外基质共同构成了造血细胞赖以生存、生长发育和成熟的环境,称为造血诱导微环境(hematopoietic inductive microenvironment, HIM) 。
骨髓中的造血干细胞(hematopoietic stem cell , HSC)是具有高度自我更新能力和多能分化潜能的造血前体细胞, 体内血细胞均由其分化而来。 血细胞在骨髓中生长、分裂及分化的过程称为造血 (hematopoiesis) 。 人体内的造血功能首现于2 -3 周胚龄的卵黄裂,在胚胎早期(第2 -3 个月)HSC 从 卵黄襄迁移至胎肝,继而入脾,肝和脾成为胚胎第3 -7 个月的主要造血器官。 随后,HSC 又迁至骨髓,使骨髓成为胚胎末期直到出生后的造血器官。 HSC 在造血组织中所占比例极低,形态学上难以与其他单个核细胞相区别,人HSC 的主要表面标志为CD34 和 CD117, 不表达各种成熟血细胞谱系相关的表面标志。
(二)骨髓的功能
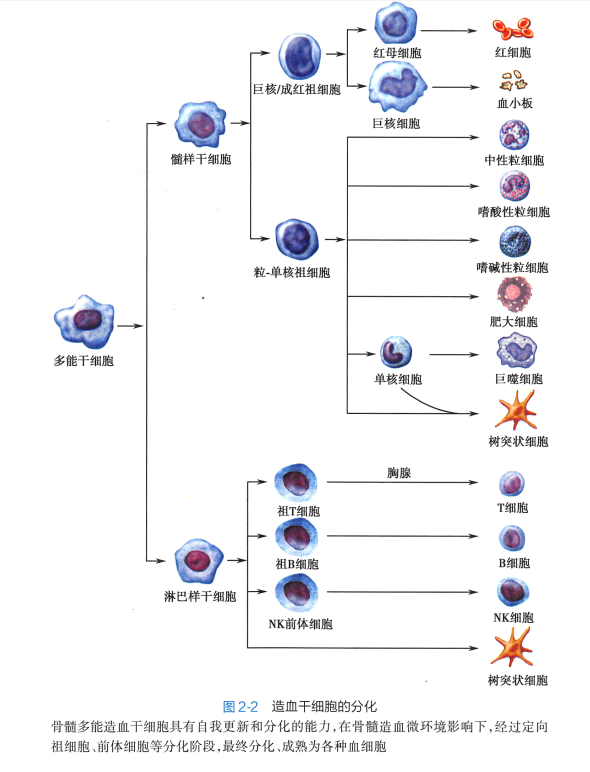
1. 各类血细胞和免疫细胞发生的场所 在骨髓造血诱导微环境中,HSC 最初分化为定向干细胞,包括髓样干细胞(myeloid stem cell ) 和淋巴样千细胞( lymphoid stem cell ) 。 髓样干细胞最终分化为粒细胞、单核细胞、红细胞和血小板等。 淋巴样干细胞分化为祖B 细胞(pro-B cell) 和祖T 细胞(pro-T cell) 。 祖B 细胞在骨髓中继续分化为成熟B 细胞;祖T 细胞则经血液循环迁移至胸腺,在胸腺微环境诱导下进一步分化为成熟T 细胞。 成熟的B 细胞、T 细胞离开骨髓或胸腺,经血循环迁移并定居于外 周免疫器官。 尚未接触过抗原的成熟T、 B 细胞被称为初始淋巴细胞(naive lymphocyte) 。 树突状细胞来自髓样干细胞和淋巴样干细胞(图2-2) 。
2. B 细胞和NK细胞分化成熟的场所 在骨髓造血微环境中,祖B 细胞(pro-B) 经历前B 细胞 (pre-B cell) 、未成熟B 细胞,最终发育为成熟B 细胞。 NK 细胞也在骨髓中发育成熟。
3. 体液免疫应答发生的场所 骨髓是发生再次体液免疫应答后产生抗体的主要部位。 记忆B细胞在外周免疫器官受抗原再次剌激而被活化,随后经淋巴液和血液迁移至骨髓,在此分化为成熟浆 细胞,持久地产生大量抗体(主要是IgG, 其次为IgA 等)并释放至血液循环,成为血清抗体的主要来源。 而在外周免疫器官发生的再次免疫应答, 其抗体产生速度快,但持续时间相对较短。
骨髓功能缺陷时,不仅会严重损害机体的造血功能,而且导致严重的细胞免疫和体液免疫功能缺陷。 如大剂量放射线照射可使机体的造血功能和免疫功能同时受到抑制或丧失,这时只有植入正常骨髓才能重建造血和免疫功能。 将免疫功能正常个体的造血干细胞或淋巴干细胞移植给免疫缺陷个体,使后者的造血功能和免疫功能全部或部分得到恢复,可治疗免疫缺陷病和白血病等。
二、胸腺
胸腺(thymus) 是T 细胞分化、发育、成熟的场所。 老年期胸腺明显缩小,皮质和髓质被脂肪组织取代,胸腺微环境改变,T 细胞发育成熟减少,导致老年人的免疫功能减退。
(—)胸腺的结构和细胞组成
胸腺由胸腺细胞和胸腺基质细胞( thymus stromal cell , TSC)组成。 胸腺细胞是处于不同分化阶段的T 细胞。 TSC 包括胸腺上皮细胞(thymus epithelial cell, TEC) 、巨噬细胞(macrophage, Mø)、 树突状细胞(dendritic cell, DC) 和成纤维细胞等。 胸腺上皮细胞呈星形,其突起相互连接成网状,间隙中充满 胸腺细胞和少量Mø。
1. 皮质 胸腺皮质分为浅皮质区(outer cortex) 和深皮质区(inter cortex) 。 皮质内85% -90% 的细胞为胸腺细胞(主要是未成熟T细胞),并含有TEC、 Mø 和 DC 等。 胸腺浅皮质区内的胸腺上皮细 胞可包绕胸腺细胞,称为胸腺抚育细胞(thymic nursing cell) , 可产生某些促进胸腺细胞分化发育的激素和细胞因子。 深皮质区内主要为体积较小的皮质胸腺细胞。
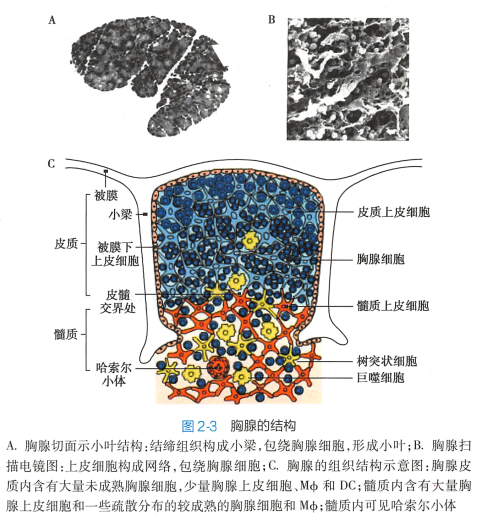
2. 髓质 髓质内含有大量胸腺髓质上皮细胞和疏散分布的较成熟的胸腺细胞、Mø和DC。 髓质内常见胸腺小体(thymic corpuscle) , 又称哈索尔小体(Hassall corpuscle) , 由聚集的上皮细胞呈同心圆状包绕排列而成,是胸腺结构的重要特征。 胸腺小体在胸腺发生炎症或肿瘤时消失。
(二)胸腺微环境
胸腺微环境( thymic microenvironment) 主要由胸腺基质细胞、 细胞外基质及局部活性因子组成,是决定T 细胞分化、增殖和选择性发育的重要条件。 胸腺上皮细胞是胸腺微环境最重要的组分,其以两种方式影响胸腺细胞的分化、发育。
分泌细胞因子和胸腺肽类分子 胸腺上皮细胞可产生SCF、 IL-I 、 IL-2 、 IL-6 、 IL-7 、 TNF-α、 GM-CSF 和趋化因子等多种细胞因子,这些细胞因子通过与胸腺细胞表面相应的一些因子受体结合,调节胸腺细胞的发育和细胞间相互作用。 胸腺上皮细胞分泌的胸腺肽类分子包括胸腺素(thymosin) 、胸 腺肽(thymulin) 、胸腺生成素( thymopoietin) 等,具有促进胸腺细胞增殖、分化和发育等功能。
2. 细胞-细胞间相互接触 胸腺上皮细胞与胸腺细胞间可通过细胞表面分子的相互作用,诱导和促进胸腺细胞的分化、发育和成熟。
细胞外基质(extracellular matrix) 也是胸腺微环境的重要组成部分,包括多种胶原、网状纤维蛋白、葡萄糖胺聚糖等。 它们可促进上皮细胞与胸腺细胞接触,并帮助胸腺细胞由皮质向髓质移行及成熟。
(三)胸腺的功能
1. T 细胞分化、成熟的场所 胸腺是T 细胞发育的主要场所。 从骨髓迁入到胸腺的T 细胞前体(胸腺细胞)循被膜下一皮质一髓质移行,在胸腺微环境中,经过阳性选择和阴性选择过程,约 90%以上的胸腺细胞发生凋亡,少部分胸腺细胞获得MHC 限制性和自身免疫耐受,发育成熟为初始T 细 胞(naive T cell ) , 离开胸腺经血循环至外周免疫器官。 若胸腺发育不全或缺失,则导致T细胞缺乏和细胞免疫功能缺陷。 如迪格奥尔格综合征(DiGeorge's syndrome) 患儿因先天性胸腺发育不全,缺乏T 细胞,极易反复发生病毒性和真菌性感染,甚至死亡。
2. 免疫调节作用 胸腺基质细胞所产生的多种细胞因子和胸腺肽类分子,不仅能调控胸腺细胞的分化、发育,而且对外周免疫器官和免疫细胞也有调节作用。
3. 自身免疫耐受的建立与维持 T 细胞在胸腺发育过程中,自身反应性T 细胞通过其抗原受体 (TCR)与胸腺基质细胞表面表达的自身抗原肽-MHC 复合物发生高亲和力结合,引发阴性选择,启动细胞程序性死亡,导致自身反应性T 细胞克隆消除或被抑制, 形成对自身抗原的中枢免疫耐受。 若胸腺基质细胞缺陷,阴性选择机制发生障碍,不能消除或抑制自身反应性T 细胞克隆,出生后易患自身免疫病。