黏附分子
细胞黏附分子(celladhesionmoleculeCAM)是介导细胞间或细胞与细胞外基质(extracellular matrix,ECM)间相互结合和作用的分子。黏附分子以受体-配体结合的形式发挥作用,使细胞与细胞间或细胞与基质间发生黏附,参与细胞的附着和移动,细胞的发育和分化,细胞的识别、活化和信号转导,是免疫应答、炎症发生、凝血、肿瘤转移以及创伤愈合等一系列重要生理和病理过程的分子基础。
黏附分子属于白细胞分化抗原,大部分黏附分子已有 CD编号,但也有部分黏附分子尚无 CD编号。黏附分子根据其结构特点可分为免疫球蛋白超家族、整合素家族、选择素家族、钙黏蛋白家族。此外还有一些尚未归类的黏附分子。
一、免疫球蛋白超家族
参与细胞间相互识别、相互作用的黏附分子中,有许多分子具有与免疫球蛋白相似的V区样或C区样结构域,其氨基酸组成也有一定的同源性,属于免疫球蛋白超家族(immunoglobulin superfamily, IgSF)的成员。IgSF黏附分子在免疫细胞膜分子中最为庞大,不仅种类繁多、分布广泛,功能也十分多样和重要,其配体多为IgSF黏附分子以及整合素,主要参与淋巴细胞的抗原识别,免疫细胞间相互作用,并参与细胞的信号转导。
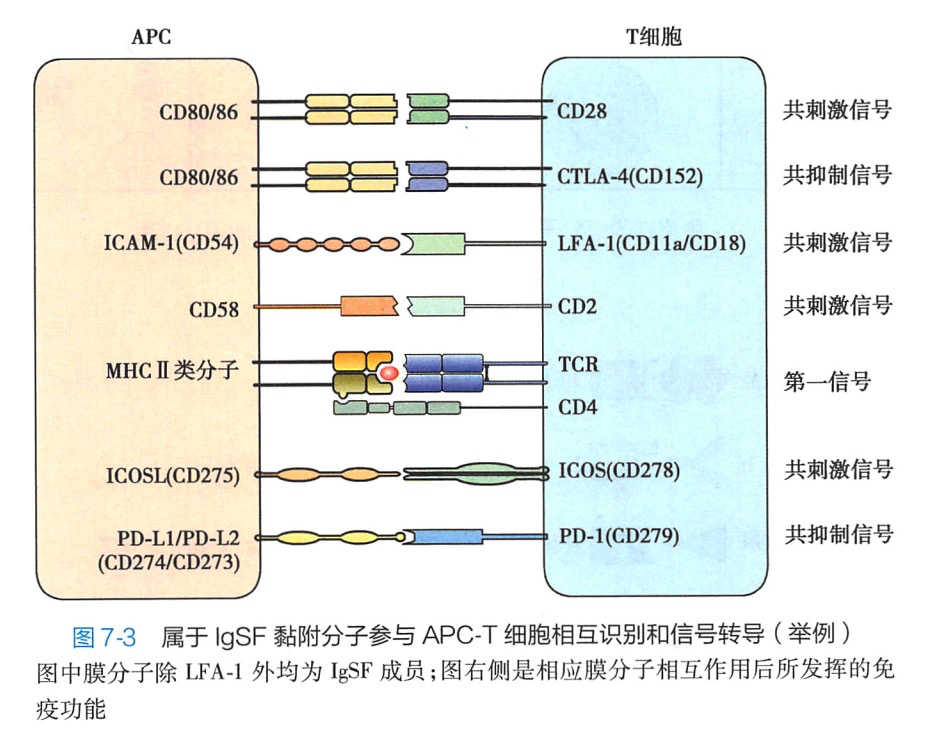
此处以APC与T细胞相互作用为例,对属于IgSF的黏附分子CD4、CD28、CTLA-4(CD152)、CD80(B7-1)CD86(B7-2)、ICOS(CD278)、ICOSL(CD275)ICAM-1(C54)、PD-1(CD279)、PD-L1/PD-L2(CD274/CD273)的相互识别所介导的APC对T细胞的激活或抑制作用加以简单介绍(图7-3)。
二、整合素家族
整合素家族(integrin family)是因该类黏附分子主要介导细胞与细胞外基质的黏附,使细胞得以附着形成整体(integration)而得名。
(一)整合素分子的基本结构
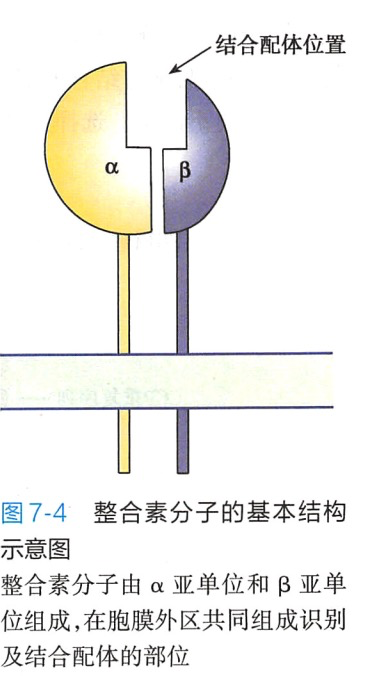
整合素家族的成员都是由a、8两条链(或称亚单位)经非共价键连接组成的异源二聚体。a、ß链共同组成识别配体的结合点(图7-4)。
(二)整合素家族的组成
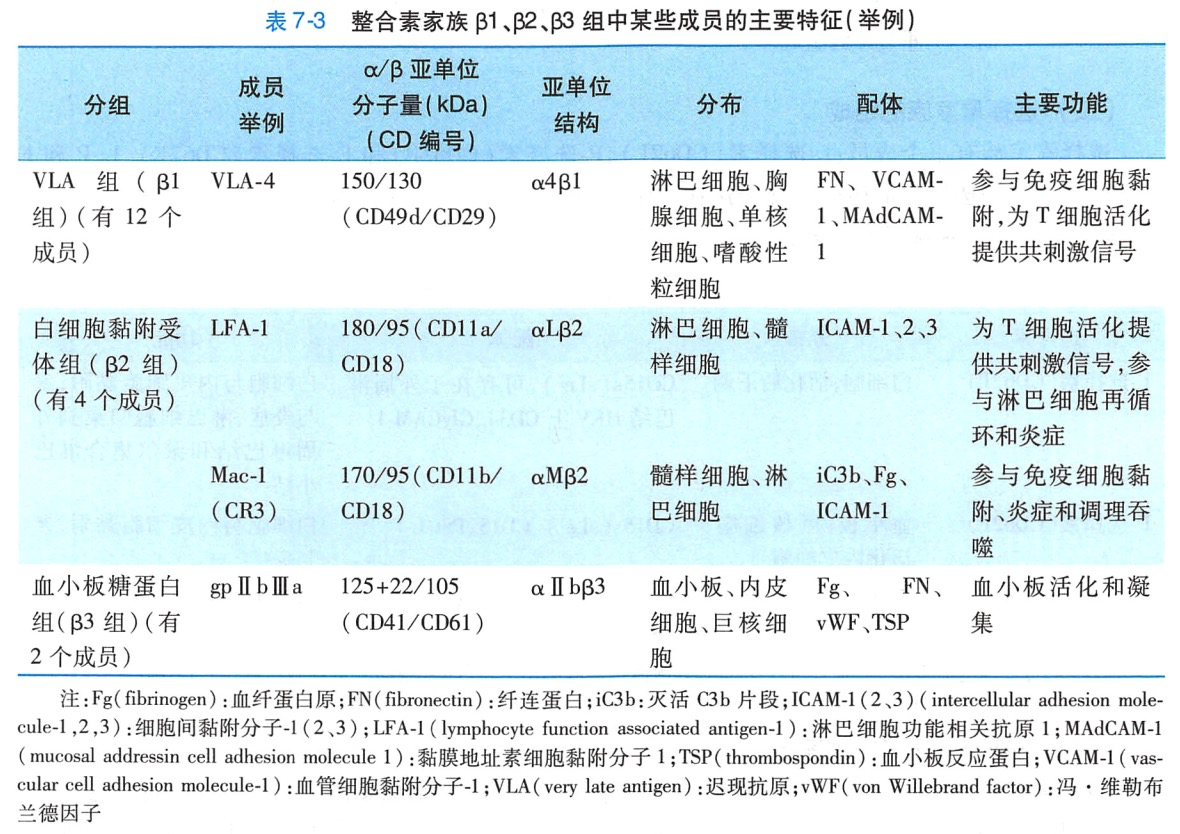
整合素家族中至少有18种a亚单位和8种β亚单位,以B亚单位的不同将整合素家族分为8个组(β1~β8 组)。同一个组中,ß链均相同,α链不同。大部分α链结合一种β链,有的α链可分别结合两种或两种以上的β链。已知α链和β链之间有24种组合形式。表 7-3 列举了整合素家族 β1、β2、β3 三个组中某些成员的结构、分布、相应配体和主要功能。
(三)整合素分子的分布
整合素分子在体内分布十分广泛,一种整合素可分布于多种细胞,同一种细胞也往往有多种整合素的表达。某些整合素的表达有显著的细胞类型特异性,如白细胞黏附受体组(β2组)主要分布于白细胞,gpⅡbⅢa分布于巨核细胞/血小板和内皮细胞。整合素分子的表达水平可随细胞活化和分化状态不同而发生改变。
三、选择素家族
选择素家族(selectin family)有L-选择素、P-选择素和E-选择素三个成员,在白细胞与内皮细胞黏附、炎症发生以及淋巴细胞归巢中发挥重要作用。
(一) 选择素分子的基本结构
选择素为跨膜分子,选择素家族各成员胞膜外区结构相似,均由C型凝集素样(CL)结构域、表皮生长因子(EGF)样结构域和补体调节蛋白(CCP)结构域组成。其中CL结构域可结合某些碳水化合物,是选择素与配体结合的部位;EGF样结构域则对于维持选择素分子的构象是必需的,而CCP结构域的作用尚不清楚。选择素分子胞质区与细胞骨架相连(图7-5)。
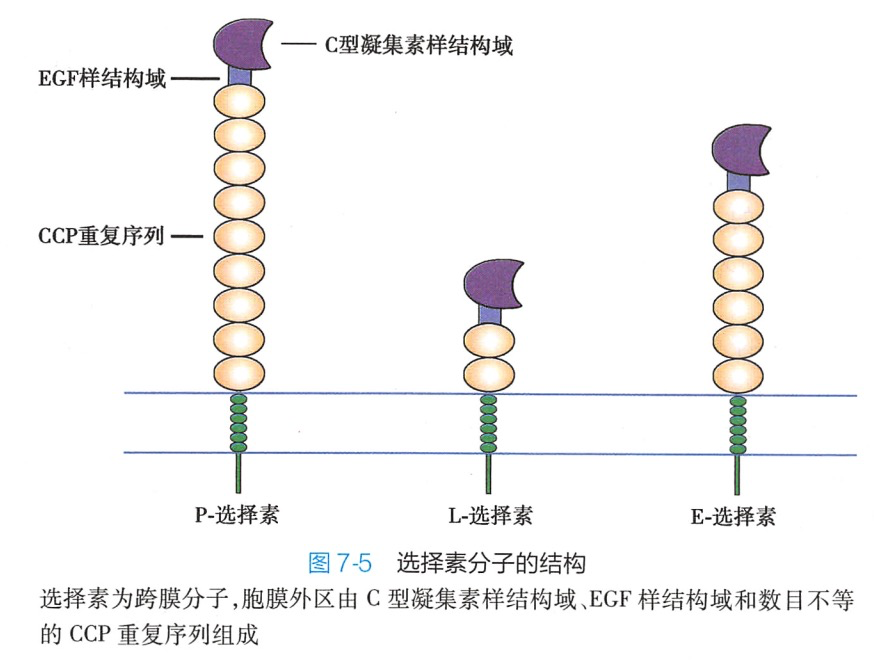
(二)选择素家族的组成
选择素家族有三个成员:L-选择素(CD62L)、P-选择素(CD62P)和E-选择素(CD62E)。L、P和E分别表示这三种选择素最初被发现表达在白细胞(leukocyte)、血小板(platelet)或血管内皮细胞(en dothelial cell)。三种选择素的分布、配体和主要功能如表 7-4。
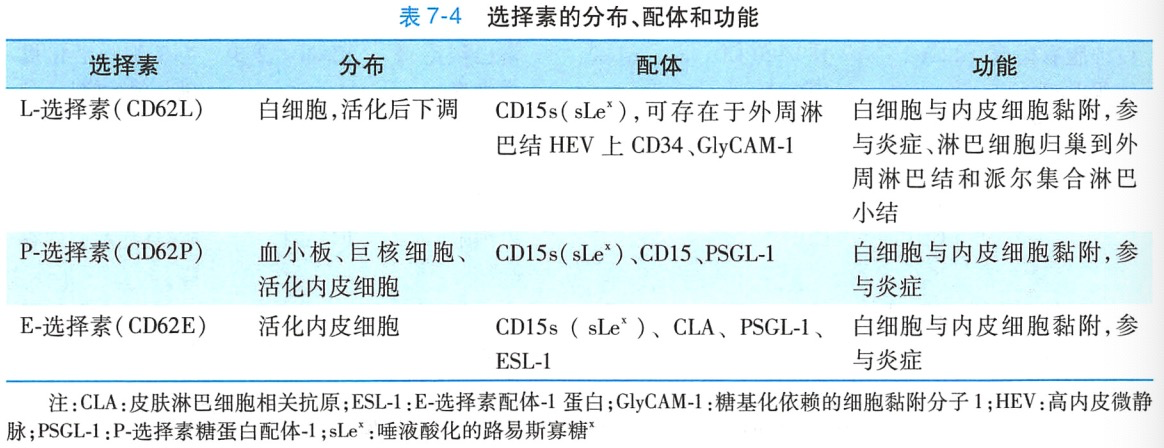
(三)选择素分子识别的配体
与大多数黏附分子所结合的配体不同,选择素识别的是一些寡糖基团,主要是唾液酸化的路易斯寡糖(sialyl-Lewis*.sLe*即CD15s)或类似结构的分子,这些配体主要表达于白细胞和内皮细胞表面。
四、钙黏蛋白家族
钙黏蛋白(cadherin)是同亲型结合(两个相同分子相互结合)、Ca依赖的细胞黏附分子,对胚胎发育中的细胞识别、迁移和组织分化以及成体组织器官构成具有重要作用。(表7-5)

(一) 钙黏蛋白的分子结构
钙黏蛋白分子均为单糖链蛋白,由胞质区、跨膜区和胞膜外区三部分组成。其胞膜外区有数个重复功能区,分子外侧 N端的113 个氨基酸残基构成 Cadherin 分子的配体结合部位。此外胞膜外区具有结合钙离子的作用。Cadherin 分子的胞质区高度保守,并与细胞内骨架相连。
(二)钙黏蛋白家族组成
钙黏蛋白家族拥有20多个成员,由经典的钙黏蛋白和原钙黏蛋白(如钙黏蛋白相关神经受体)两个亚家族组成。其中经典的钙黏蛋白亚家族包括E-cadherin、N-cadherin和P-cadherin等,E N和P分别表示上皮(epithelial)、神经(neural)和胎盘(placental),是三种钙黏蛋白最初被发现的组织。不同的钙黏蛋白分子在体内有其独特的组织分布,它们的表达随细胞生长、发育状态不同而改变。
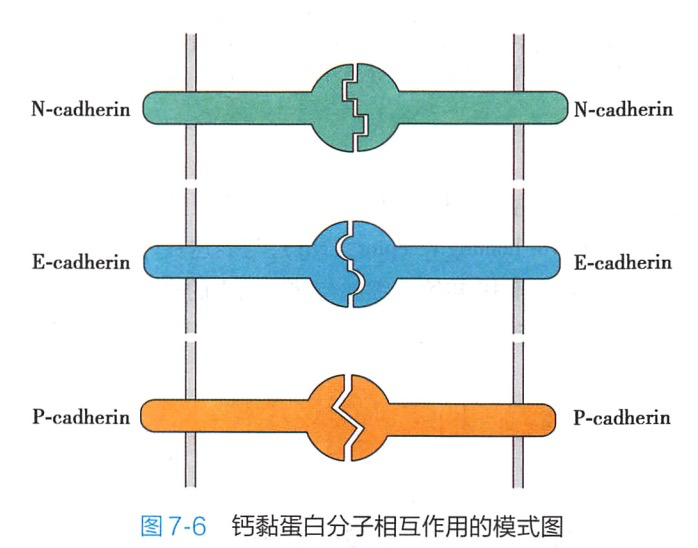
(三)钙黏蛋白识别的配体
钙黏蛋白分子以其独特的方式相互作用,其配体是与自身相同的钙黏蛋白分子(图7-6)。以这种方式相互作用的还有属干免疫球蛋白超家族的 CD31(PECAM)和CD56(NCAM)。
五、黏附分子的功能
黏附分子参与机体多种重要的生理功能和病理过程。
(一)参与免疫细胞之间的相互作用和活化
免疫细胞之间的相互作用均有黏附分子参与。例如,DC 与T细胞以及 CTL与靶细胞相互作用时,首先是两种细胞通过黏附分子的疏松结合。如果 DC与T细胞间或 CTL 与靶细胞间能发生特异性结合,则细胞间相互作用继续进行;如果无特异性结合,则细胞解离。
T细胞除了通过 TCR 识别抗原,还需要共受体(co-receptor)CD4/CD8与MHC分子结合,以加固结合和共同提供细胞活化第一信号。
共刺激信号是指免疫细胞在接受抗原刺激提供的第一信号的同时,由共刺激分子提供的辅助活化信号(第二信号)。共刺激分子的种类很多,在不同的环境中发挥的作用也不同。T细胞-APC 识别时最为常见的提供共刺激信号的黏附分子有.CD28-CD80或CD86、CD2-CD58.LFA-1-ICAM-1等(图7-3)。如果APC不表达CD80/CD86,则T细胞缺乏CD80/CD86-CD28相互作用提供的共刺激信号。抗原刺激后的T细胞会处于免疫应答失能(anergy)状态。
(二)参与炎症过程中白细胞与血管内皮细胞黏附
细胞表达的不同黏附分子是其介导炎症不同阶段的重要分子基础。以中性粒细胞为例,在炎症发生初期,中性粒细胞表面的唾液酸化的路易斯寡糖(sLe*)与内皮细胞表面炎症介质所诱导表达的E-选择素的相互作用,介导了中性粒细胞沿血管壁的滚动和最初的结合;随后,中性粒细胞表面的IL-8受体结合内皮细胞表面的膜型IL-8,从而刺激细胞表面LFA-1和Mac-1等整合素分子表达上调和活化,并同内皮细胞表面的ICAM-1结合,介导中性粒细胞与内皮细胞紧密的黏附和穿出血管内皮细胞到炎症部位发挥作用(图7-7)。
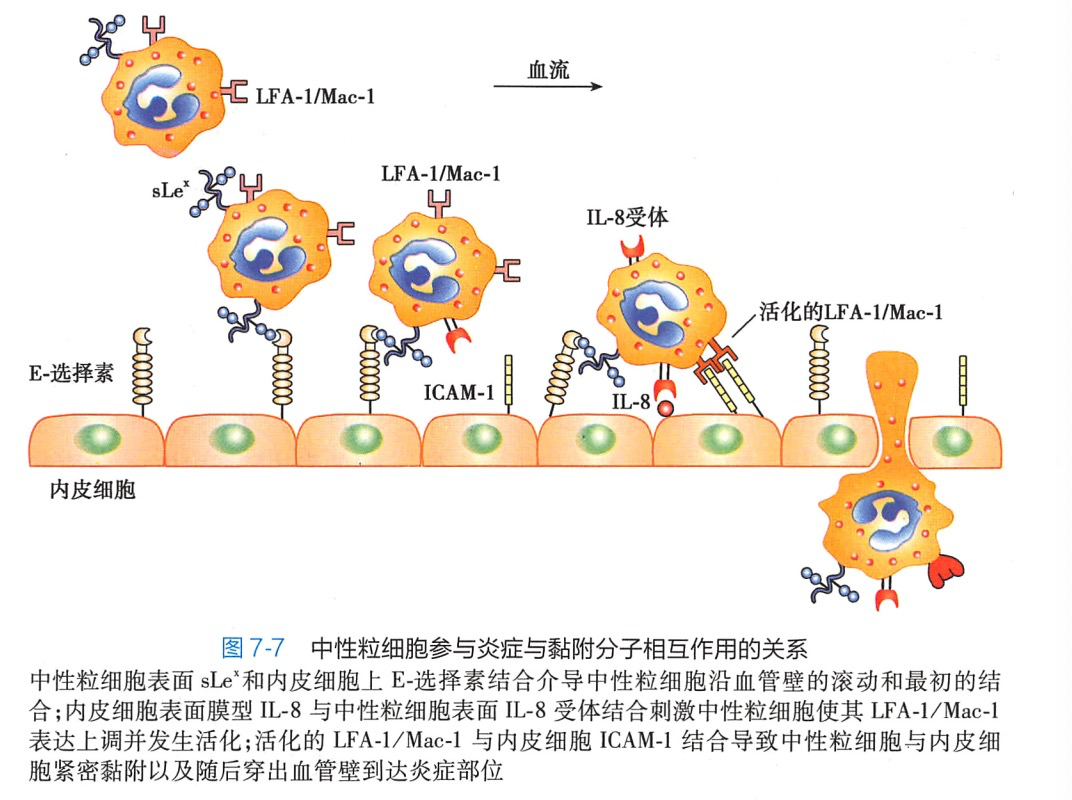
(三)参与淋巴细胞归巢
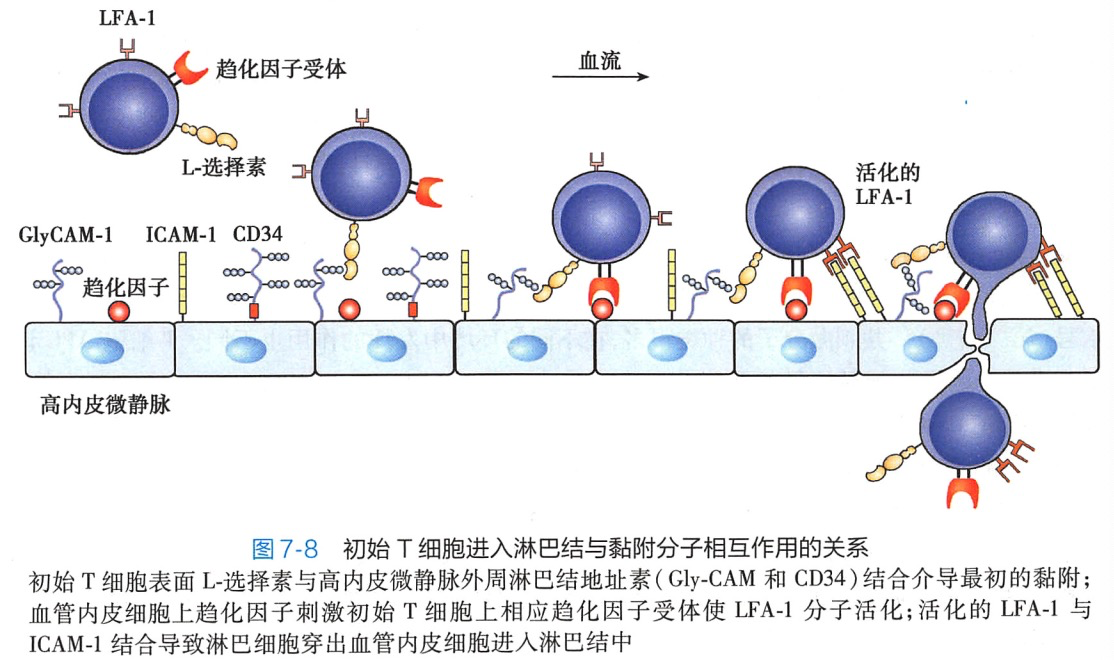
淋巴细胞归巢是淋巴细胞的定向迁移,包括淋巴细胞再循环和淋巴细胞向炎症部位迁移。其分子基础是表达在淋巴细胞上的淋巴细胞归巢受体(lymphocyte homing receptor,LHR),与表达在内皮细胞上的血管地址素的相互作用。图 7-8 列举了在淋巴细胞再循环中,初始T细胞与淋巴结中的高内皮微静脉(HEV)结合,并穿出血管内皮细胞进入淋巴结过程中所参与的黏附分子。
(四)参与细胞的发育、分化、附着和移动
在胚胎发育过程中,不同类型的细胞按照既定的规律形成细胞与细胞之间及细胞与细胞外基质的附着,有序地发育分化并组合在一起构成不同的组织和器官。在此过程中,黏附分子发挥着重要作用。细胞间的附着及细胞移动是细胞发育、分化的基础,参与其中的主要为钙黏蛋白家族成员以及属于IgSF的黏附分子 NCAM(CD56) PECAM(CD31)等。而细胞与细胞外基质的附着对于细胞生存和增殖是必需的,主要由表达于各种组织细胞表面的整合素家族黏附分子来介导。
(五)参与多种疾病的发生
黏附分子介导了多种疾病的发生,如CD18(B2整合素)基因缺陷导致 LFA-1(CD11a/CD18)、Mac-1(CD11h/CD18)等整合素分子功能不全白细胞不能黏附和穿过血管内皮细胞。由此引起一种称为白细胞黏附缺陷症(leukocyte adhesion deficiency,LAD)的严重免疫缺陷病。CD4 分子是人类免疫缺陷病毒(human immunodeficiency virusHIV)糖蛋白 gp120识别的部位,是HIV的主要受体。HIV能够感染并破坏CD4+T细胞,进而损伤了CD4T细胞所介导的辅助T细胞和B细胞应答的功能,因此患者出现获得性免疫缺陷综合征即艾滋病(acauired immunodeficiencvsvndrome AIDS)。