(一)补体的生物功能
补体活化的共同终末效应是在细胞膜上组装MAC,介导细胞溶解效应。 同时,补体活化过程中生成多种裂解片段,通过与细胞膜相应受体如 I 型补体受体(CR1 、 C3b/C4b 受体)、 II 型补体受体 (CR2、 C3b 受体、CD21 ) 、 III 型补体受体(CR3) 、 IV型补体受体(CR4) 、 C5aR、 C3aR、 C1qR 等结合而介 导多种生物学功能。
1. 细胞毒作用 补体系统激活后,最终在靶细胞表面形成MAC,从而使细胞内外渗透压失衡,导致细胞溶破。 该效应的意义为: 参与宿主抗细菌(主要是G- 细菌)、抗病毒及抗寄生虫等防御机制; 参与机体抗肿瘤免疫效应机制; 某些病理情况下引起机体自身细胞破坏,导致组织损伤与疾病(如血型 不符输血后的溶血反应以及自身免疫病)。
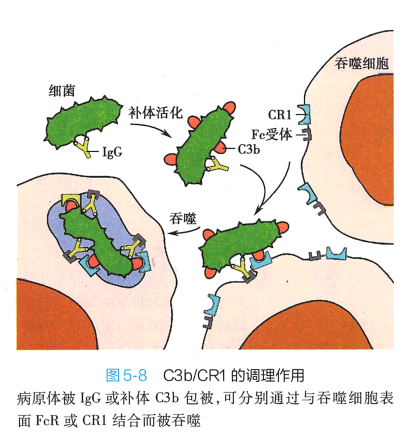
2. 调理作用 (opsonization) 补体激活产生的C3b、 C4b、 iC3b 等片段直接结合千细菌或其他颗粒物质表面,通过与吞噬细胞表面相应补体受体结合而促进吞噬细胞对其吞噬(图5- 8) 。 这种调 理吞噬的作用是机体抵御全身性细菌感染和真菌感染的重要机制之一。
3. 炎症介质作用 补体活化过程中产生多种具有炎症介质作用的片段,如C5a、 C3a 和C4a 等。 三者均可与肥大细胞或嗜碱性粒细胞表面相应受体结合,触发靶细胞脱颗粒,释放组胺和其他生物活性物质,引起血管扩张、毛细血管通透性增高、平滑肌收缩等,从而介导局部炎症反应。 C5a 对中性粒 细胞有很强的趋化活性,并可刺激中性粒细胞产生氧自由基、前列腺素和花生四烯酸等。
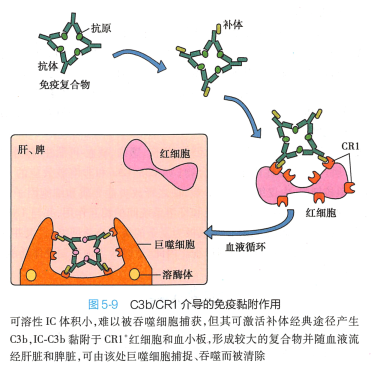
4. 清除免疫复合物 补体成分可参与清除循环免疫复合物(IC) , 其机制为:C3b 与IC 结合,同 时黏附于CR1+红细胞、血小板,从而将IC 运送至肝脏和脾脏被巨噬细胞吞噬、清除,此作用被称为免疫黏附(immune adherence) (图 5-9) 。
(二)补体的病理生理学意义
机体抗感染防御的主要机制 在抗感染防御机制中,补体是固有免疫和适应性免疫间的桥梁。 病原微生物侵入机体后,补体旁路途径或MBL 途径通过识别微生物表面或其糖链组分而触发级联反应,所产生的裂解片段和复合物通过调理吞噬、炎症反应和溶解细菌而发挥抗感染作用。 在特异 性抗体产生后,可通过经典途径触发C3 活化,与旁路途径中C3 正反馈环路协同作用,形成更为有效 的抗感染防御机制。
2. 参与适应性免疫应答 补体活化产物、补体受体及补体调节蛋白可通过不同机制参与适应性免疫应答。 例如:补体介导的调理作用可促进抗原提呈细胞摄取和提呈抗原,启动适 应性免疫应答;又如感染灶的过敏毒素(C3a、 C5a、 C4a) 可招募炎症细胞,促进抗原的清除。
3. 补体系统与血液中其他级联反应系统的相互作用 补体系统与体内凝血系统、纤溶系统和激肽系统存在密切关系:(1)四个系统的活化均依赖多种成分级联的蛋白酶裂解作用,且均借助丝氨酸蛋 白酶结构域发挥效应; (2)一个系统的活化成分可对另一系统发挥效应, 如 C1INH 不仅负调节活化的 C1r、 C1s, 也可抑制激肽释放酶、血浆纤溶酶、凝血因子VII 和VI 。 某些疾病状态下(如弥散性血管内凝血、 急性呼吸窘迫综合征等),四个系统的伴行活化具有重要病理生理意义。综上所述,补体的生物学意义远超出单纯非特异性防御的范畴,而涉及包括适应性免疫应答在内的广泛生理功能:补体系统既是固有免疫防御的一部分,又是特异性体液免疫应答的重要效应机制; 补体可调节适应性免疫应答,并与体内其他蛋白系统相互联系。