补体激活途径
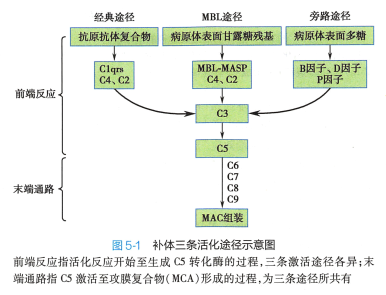
补体固有成分以非活化形式存在千体液中,通过级联酶促反应被激活,产生具有生物学活性的产 物。 已发现三条补体激活途径,它们有共同的终末反应过程(图5-1 ) 。
(一)经典途径
经典途径(classical pathway) 指激活物与C1q 结合,顺序活化C1r、 Cls、 C4、 C2、 C3,形成C3 转化酶(C4b2a) 与C5 转化酶(C4b2a3b) 的级联酶促反应过程(图5-2) 。 C1 通常以C1q(C1r)2(C1s)2 复合 大分子形式存在于血浆中。 C2 血浆浓度很低,是补体活化级联酶促反应的限速成分。 C3 是血浆中 浓度最高的补体成分,是三条补体激活途径的共同组分。
1. 激活物 经典途径的激活物主要是与抗原结合的lgG、 IgM 分子。 此外,血清中C 反应蛋白 (CRP)、淀粉样蛋白p 成分(SAP) 和五聚素3(PTX3) 等蛋白能识别并结合微生物表面成分,如磷脂胆碱、磷脂酰乙醇胺等,进而激活C1q;某些细菌细胞壁上的蛋白成分以及G+菌的胞壁酸(LTA) 还能直 接激活C1q。 人类不同类型抗体活化C1q 的能力各异(IgM>lgG3 >IgG1> lgG2) , IgG4 无激活经典途径的能力。
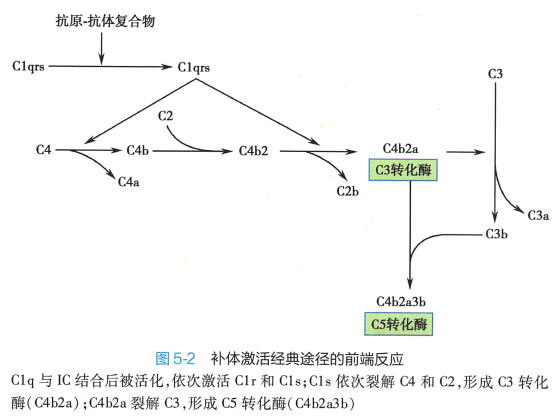
2. 活化过程 C1q 与2 个以上抗体Fc 段结合可发生构型改变,使与C1q 结合的C1r 活化,活化的C1r 激活C1s 的丝氨酸蛋白酶活性。活化的Cls 的第一个底物是C4。 在Mg2+存在下,C1s 使C4 裂解为C4a 和 C4b,其中部分C4b 结合至紧邻抗原抗体结合处的细胞或颗粒表面。
C1s 的第二个底物是C2 分子。 在Mg2+ 存在下,C2 与C4b 形成复合物,被C1s 裂解而形成C2a 和C2b;C2a 可与C4b 结合成C4b2a 复合物即C3 转化酶(C3 convertase) , 后者使C3 裂解为C3a 和C3b, 此乃补体活化级联反应中的枢纽性步骤。 新生的C3b 可与C4b2a 中C4b 结合,形成C4b2a3b 即C5 转化酶(C5 convertase) , 进入补体激活的末端通路(图5-2) 。 C3a 游离于液相,是重要的炎症介质。 另 外,C3b 还可进一步被裂解为C3c、 C3dg、 C3d 等小片段,其中C3d 可参与适应性免疫应答。
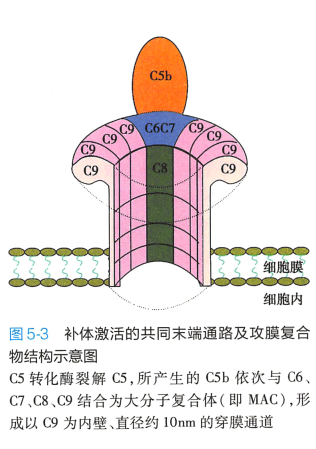
C5 转化酶(C4b2a3b)将C5 裂解为C5a、C5b;C5a 游离于液相,是重要的炎症介质,C5b 可与C6 稳定结合为C5b6;C5b6 自发与C7 结合成C5b67,暴露膜结合位点,与附近的细胞膜非特异性结合;结合于膜上的C5b67 可与C8 结合,所形成的C5b678 可促进与多个C9 分子聚合,形成C5b6789n 复合 物,此即攻膜复合物(membrane attack complex, MAC) (图 5-3) 。 插入细胞膜的MAC 通过破坏局部磷 脂双层而形成"渗漏斑",或形成穿膜的亲水性孔道,可容许水、离子及可溶性小分子等经此孔道自由 流动。 由于胞内胶体渗透压较胞外高,故大量水分内流,导致胞内渗透压降低、细胞逐渐肿胀并最终 破裂(溶破)。
(二)旁路途径
旁路途径(alternative pathway) 又称替代激活途径, 其不依赖千抗体,而由微生物或外源异物直接激活C3, 在B 因子、D 因子和备解素P 因子参与下,形成C3 转化 酶和C5 转化酶,启动级联酶促反应过程。 在生物进化 的种系发生上,旁路途径是最早出现的补体活化途径, 是抵御微生物感染的非特异性防线。
1. 激活物 某些细菌、内毒素、酵母多糖、 葡聚糖 均可成为旁路途径“激活物”,它们实际上是为补体激活提供保护性环境和接触的表面。
2. 活化过程此途径从C3 开始。 生理条件下,血清C3 受蛋白酶等作用可发生缓慢而持久的水解,产生低水平C3b。 自发产生的C3b 绝大多数在液相中快速 失活,少数可与附近的膜表面结构共价结合,膜表面结构不同,产生不同的结果:1)结合千自身组织细胞表面 的 C3b, 可被多种调节蛋白降解、灭活;2)结合于“激活物”表面的C3b,可与B 因子结合,在MG2+存在下,结合的 B 因子被D 因子裂解为Ba 和Bb,Bb 仍与C3b 结合,形成C3bBb, 即旁路途径C3 转化酶。
旁路途径中,备解素(P) 可结合细菌表面,稳定C3b 与 Bb 结合形成C3 转化酶,防止其被降解。结合于激活物表面的C3bBb 可裂解更多C3 分子,新生的C3b 又可与Bb 结合为新的C3bBb,形成旁 路激活的正反馈放大效应(图5-4) 。
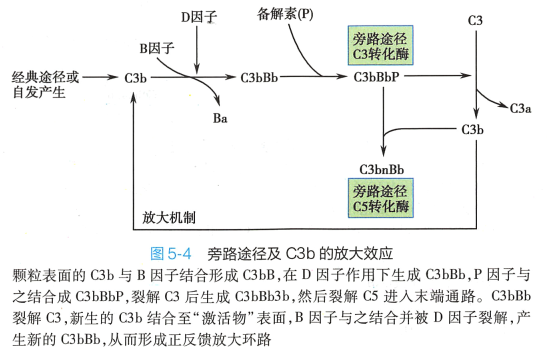
C3b 可与C3bBb 复合物结合为C3bBb3b,此即旁路途径C5 转化酶。 其后的末端通路与经典途径 完全相同。
(三)凝集素途径
凝集素途径( lectin pathway) 又称 MBL 途径(MBL pathway) , 指血浆中甘露糖结合凝集素(mannose-binding lectin, MBL) 、纤维胶原素(ficolin , FCN) 等直接识别病原体表面糖结构,依次活化 MBL 相关丝氨酸蛋白酶(MEL-associated serine protease, MASP) 、 C4、 C2、 C3,形成与经典途径中相同的 C3 转化酶与C5转化酶的级联酶促反应过程。
1. 激活物 凝集素途径的激活物是病原体表面的糖结构。 MBL 和FCN 可选择性识别多种病原 体表面以甘露糖、甘露糖胺等为末端糖基的糖结构。 含这些末端糖基的糖结构在哺乳动物细胞罕见 (因其被唾液酸等所覆盖),但却是细菌、真菌及寄生虫细胞表面的常见成分。
2. 活化过程 MBL-MASP 或FCN-MASP 复合物与病原体表面糖结构结合后,MBL或FCN 发生构 象改变,使与之结合的MASPl 和MASP2 被分别激活。
活化的MASP2 发挥其丝氨酸蛋白酶活性,裂解C4, 所产生的C4b 片段共价结合于病原体表面,随后与C2 结合,后者也被MASP2 裂解,生成与经典途径相同的C3 转化酶C4b2a, 继之裂解C3 产生C5转化酶C4b2a3b,最后进入补体激活的末端通路(图5-5 ) 。
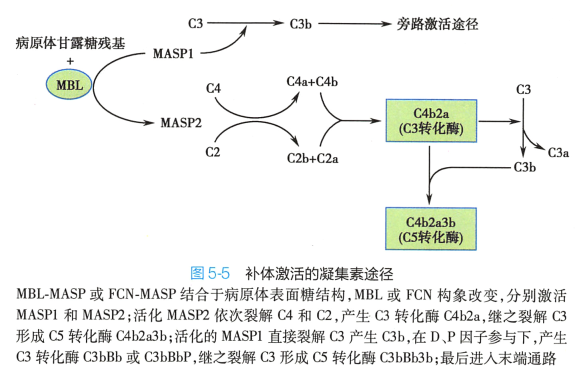
另外,活化的MASP1可直接裂解C3 产生C3b,在D 因子和P 因子参与下,激活补体旁路途径(图 5-5) 。 因此,凝集素途径对经典途径和旁路途径的活化具有交叉促进作用。
(四)三条补体激活途径的特点
在生物种系进化中,三条补体激活途径出现的先后顺序是旁路途径->MBL 途径->经典途径。 三条途径起点各异,但存在相互交叉,并具有共同的末端通路(图5-6) 。
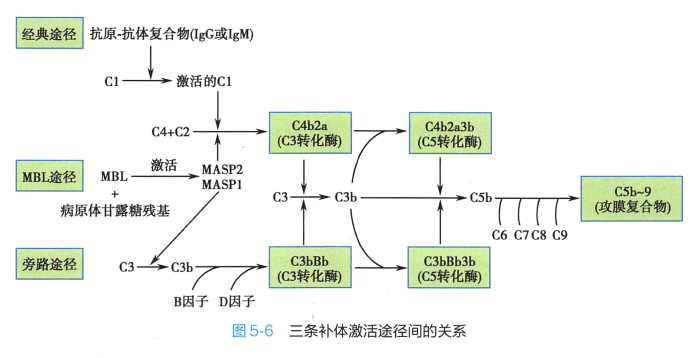
1. 经典途径 主要特点为:(1)激活物主要是由IgG 或IgM 结合膜型抗原或游离抗原所形成的免疫复合物(IC) ,C1q 识别抗原-抗体复合物是该途径的起始步骤;(2)C3 转化酶和C5 转化酶分别是 C4b2a 和C4b2a3b; (3)其启动有赖于特异性抗体产生,故在感染后期(或恢复期)才能发挥作用,并参与抵御相同病原体再次感染机体。 现在发现有些微生物可直接或通过C 反应蛋白等结合后间接激活C1q, 启动经典激活途径。
2. 旁路途径 主要特点为: (1)激活物是细菌、真菌或病毒感染细胞等,为自发产生的C3b 提供反应表面;(2)C3 转化酶和cs 转化酶分别是C3bBb 和C3bBb3b; (3)存在正反馈放大环路;(4)无需抗体存 在即可激活补体,故在抗体产生之前的感染早期或初次感染即可发挥作用。
3. 凝集素途径 主要特点为:(1)激活物质非常广泛,主要是多种病原微生物表面的N 氨基半乳糖 或甘露糖,由 MBL 和FCN 等识别; (2)除识别机制有别千经典途径外,后续过程基本相同;(3)对经典途径 和旁路途径具有交叉促进作用;(4)无需抗体参与即可激活补体,可在感染早期或初次感染中发挥作用。