抗体(antibody , Ab) 是介导体液免疫的重要效应分子,是免疫系统在抗原刺激下,由 B 细胞或记忆B 细胞增殖分化成的浆细胞所产生的、 可与相应抗原发生特异性结合的免疫球蛋白 ( immunoglobulin, lg) , 主要分布在血清中,也分布于组织液、外分泌液及某些细胞膜表面。
免疫球蛋白是血清中一类主要的蛋白,由 α1 、α2、 β 和γ 球蛋白等组成。1968 年和 1972 年世界 卫生组织和国际免疫学会联合会的专业委员会先后决定,将具有抗体活性或化学结构与抗体相似的 球蛋白统一命名为免疫球蛋白。
第一节 抗体的结构
—、抗体的基本结构
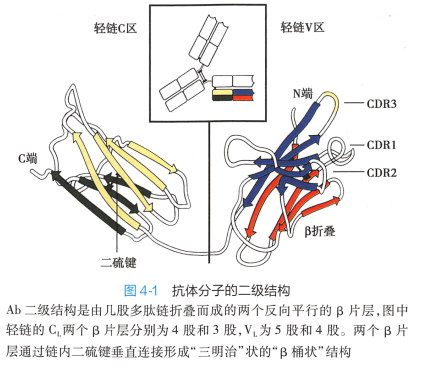
尽管抗体与抗原的特异性结合导致聚集、沉淀或中和反应等现象为人们熟知,但是直到20 世纪 50 年代末才由 Gerald M Edelman 与Rodney R Porter 共同阐明抗体的结构特征。 抗体的基本结构是由 两条完全相同的重链和两条完全相同的轻链通过二硫键连接的呈Y 形的单体。 每条肤链分别由2 ~5 个约含110 个氨基酸,序列相似但功能不同的结构域(又称功能区)组成。 结构域的二级结构是由几股 多肤链折叠形成的两个反向平行的B 片层经一个链内二硫键连接稳定的“β桶状”结构(图4-1) 。
(一)重链和轻链
重链 重链(heavy chain, H) 分子量约为50 -75kD, 由 450 - 550 个氨基酸残基组成。 根据H链恒定区抗原性的差异可将其分为5 类( class) : µ 链、 γ链、a 链、δ链和ε 链,不同的重链与轻链组成 完整的抗体分子,分别被称为IgM、 IgG、 IgA、 IgD 和IgE。 不同类的抗体分子具有不同的特征,如链内二硫键的数目和位置、连接寡糖的数量、结构域的数目以及饺链区的长度等均不完全相同。 即使是同 一类抗体,较链区氨基酸组成和重链二硫键的数目、位置也不同,据此可将其分为不同的亚类(sub class) 。 如人IgG 可分为lgG1 - lgG4 ; lgA 可分为lgA1 和lgA2。 lgM、 lgD 和lgE 尚未发现有亚类。
2. 轻链 轻链( light chain , L) 分子量约为25 kD, 由约214 个氨基酸残基构成。 轻链分为k 链和 入 链,据此可将Ab 分为两型(type) , 即 κ 型和λ型。一个天然Ab 分子上两条轻链的型别总是相同的,但同一个体内可存在分别带有κ 或λ链的抗体分子。 五类Ab 中每类Ab 的轻链都可以有κ链或λ链,两型轻链的功能无差异。 不同种属生物体内两型轻链的比例不同,正常人血清免疫球蛋白 κ:λ 约为2: 1, 而在小鼠则为20 : 1 。 κ :λ比例的异常可能反映免疫系统的异常,例如人类免疫球蛋白λ链 过多,提示可能有产生λ链的B 细胞肿瘤。 根据入链恒定区个别氨基酸的差异,又可分为λ1、λ2、λ3和λ4 四个亚型(subtype) 。
(二)可变区和恒定区
通过分析不同抗体分子重链和轻链的氨基酸序列,发现重链和轻链靠近N 端的约110 个氨基酸的序列变化很大,其他部分氨基酸序列则相对恒定。 抗体分子中轻链和重链靠近N 端的氨基酸序列变化较大,形成的结构域称为可变区(variable region, V 区),分别占重链和轻链的1/4 和 1/ 2; 靠近C端的氨基酸序列相对恒定的区域称 为恒定区(constant region, C 区),分别占重链 和轻链的3/4 和1/2( 图4-2) 。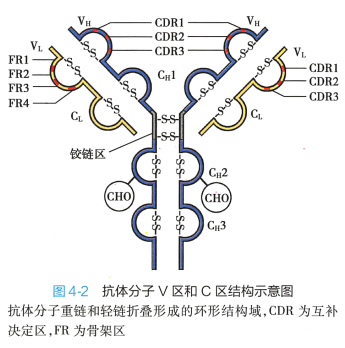
1. 可变区 重链和轻链的V 区分别称 VH和VL。 VH和VL各 各有3 个区域的氨基酸 组成和排列顺序高度可变,称为高变区(hypervariable region , HVR) ; 该区域形成与抗原表位互补的空间构象,又被称为互补决定区(complementarity determining region, CDR ) , 分别用 CDR1(HVR1 ) 、 CDR2 (HVR2) 和 CDR3 (HVR3)表示,一般CDR3 变化程度更高。 按照Kabat 编码模式,VH的3 个高变区分别位于
29 -31 、49 -58 和95 - 102 位氨基酸,VL 的3 个高变区分别位于28 -35、49 -56 和91 -98 位氨基酸。 VH和VL共6 个CDR 共同组成Ab 的抗原结 合部位(antigen-binding site) , 决定着抗体的特异性,负责识别及结合抗原,从而发挥免疫效应。 CDR 区氨基酸的多样性是抗体与数量庞大的不同抗原特异性结合 的分子基础。 V 区中CDR 之外区域的氨基酸组成和排列顺序相对变化不大,称为骨架区(framework region,FR) 。 VH或VL各有4 个骨架区,分别用FR1 、 FR2、 FR3 和FR4 表示(图4-2) 。 FR 区的主要作 用是稳定CDR 区的空间构型,以利于抗体CDR 与抗原决定簇间的精细、特异性结合。
2. 恒定区 重链和轻链的C 区分别称为CH和CL。 不同型(κ 或λ)Ab 其CL的长度基本一致,但 不同类Ab CH的长度不一,IgG、 IgA 和IgD 重链C 区有CH1 ,CH2 和CH3 三个结构域,IgM 和IgE 重链C 区有CH1、 CH2 、 CH3和CH4 四个结构域。 同一种属的个体,所产生针对不同抗原的同一类别 Ab,尽管 其V 区各异,但其C 区氨基酸组成和排列顺序比较恒定, 其免疫原性相同。 例如:针对不同抗原的人 IgG 抗体,它们的V 区不同,所以只能与相应的抗原发生特异性结合,但C 区是相同的,均含γ链,因 此抗人IgG 抗体均能与之结合。
(三)铰链区
铰链区( hinge region) 位于CH1与CH2 之间,含有丰富的脯氨酸,因此易伸展弯曲,能改变Y 形两个臂之间的距离,有利于两臂同时结合两个相同的抗原表位。铰链区易被木瓜蛋白酶、胃蛋白酶等水解,产生不同的水解片段(见水解片段部分)。 不同类或亚类的Ab 铰链区不尽相同,例如IgG1 、 IgG2 、 IgG4 和IgA 的铰链区较短, 而IgG3 和IgD 的铰链区较长。 IgM 和IgE 无铰链区。
二、抗体的辅助成分
除上述基本结构外,某些类别的Ab 还含有其他辅助成分,如J 链和分泌片。
(—) J 链
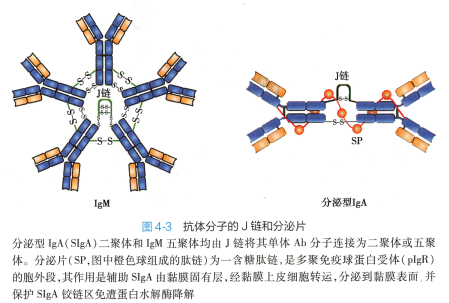
J 链(joining chain) 是由 124 个氨基酸组成,富含半胱氨酸的酸性糖蛋白(图4-3), 分子量约15kD, 由浆细胞合成,主要功能是将单体Ab 分子连接为二聚体或多聚体。 2 个IgA 单体由J 链连接形 成二聚体,5 个IgM 单体由二硫键相互连接,并通过二硫键与J 链连接形成五聚体。 IgG、 IgD 和IgE 常为单体,无J 链。
(二)分泌片
分泌片(secretory piece , SP) 又称分泌成分(secretory component, SC) (图 4-3),是分泌型lgA 分子上的辅助成分,分子量约为75kD,为含糖的肽链,由黏膜上皮细胞合成和分泌,并结合于IgA 二聚体 上,使其成为分泌型IgA(SIgA) 。 分泌片具有保护SIgA 的铰链区免受蛋白水解酶降解的作用,并介导 SIgA 二聚体从黏膜下通过黏膜上皮细胞转运到黏膜表面。
三、抗体分子的水解片段
在一定条件下,抗体分子铰链的某些部分易被蛋白酶水解为各种片段(图4-4) 。 木瓜蛋白酶 (papain) 和胃蛋白酶(pepsin ) 是最常用的两种蛋白水解酶,借此可研究Ab 的结构和功能,分离和纯化特定的Ab 多肽片段。
(—)木瓜蛋白酶水解片段
木瓜蛋白酶从铰链区的近N 端,将Ab 水解为2 个完全相同的抗原结合片段(fragment of antigen binding, Fab) 和1 个可结晶片段(fragment crystallizable, F c) (图4-4 ) 。 Fab 由 VL和VH 、CL和CH1结构域 组成,只与单个抗原表位结合(单价)。 Fc 由一对CH2 和CH3结构域组成,无抗原结合活性,是Ab 与 效应分子或细胞表面Fc 受体相互作用的部位。
(二)胃蛋白酶水解片段
胃蛋白酶在较链区的近 C 端将Ab 水解为 1 个 F (ab') 2 片段和一些小片段pFc'( 图 4-4) 。F(ab')2由2 个Fab 及铰链区组成,因此为双价,可同时结合两个抗原表位。 由于F(ab')2片段保留了 结合相应抗原的生物学活性,又避免了Fc 段抗原性可能引起的副作用和超敏反应,因而被广泛用作生物制品,如白喉抗毒素、破伤风抗毒素经胃蛋白酶水解后精制提纯的制品。 pFc'最终被降解,不发挥生物学作用。
四、免疫球蛋白超家族
在抗体分子中,除了CDR 区的氨基酸高度变化外,其余结构域的氨基酸序列相对保守,这些序列折叠成特定的球形结构,被称为免疫球蛋白折叠(immunoglobulin fold) 。 免疫球蛋白折叠提示具有这 种折叠模式的分子可能是由共同的祖先基因进化而来,被称之为免疫球蛋白超家族( immunoglobulin superfamily, IgSF) 。
免疫球蛋白超家族分子至少包含一个70 -110 个氨基酸组成的lg 结构域,折叠成反平行的β片层结构,片层间呈现疏水性,通过二硫键相连,形成免疫球蛋白折叠。 lgSF 分子分布广泛,大部分与 免疫系统相关,如T 细胞的抗原受体、T 细胞的辅助受体CD4 和CD8 、 B 细胞的辅助受体CD19、大 部分免疫球蛋白FC 受体、协同刺激分子以及部分细胞因子及其受体等。