完全互溶双液相图的绘制
一、 实验目的:
1. 掌握阿贝折射仪的使用方法通过测定混合物的折射率确定其组成。
2. 学习常压下完全互溶双液系统气-液平衡相图的测绘方法,加深对相律、恒沸点的理解。
二、 实验原理:
相图是描述相平衡系统温度、压力、组成之间关系的图形,可以通过实验测定相平衡系统的组成来绘制。
两种液体物质混合而成的两组分体系称为双液系。若两液体能以任意比例互溶,称其为完全互溶双液系统;若两液体只能部分互溶,称其为部分互溶双液系统。当纯液体或液态混合物的蒸气压与外压相等时,液体就会沸腾,此时气-液两相呈平衡,所对应的温度就是沸点。双液系统的沸点不仅取决于压力,还与液体的组成有关。表示定压下双液系统气-液两相平衡时温度与组成关系的图称为T-XB图或沸点-组成图。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-X),根据体系对乌拉尔定律的偏差情况,可分为三类:
(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(а)
所示。
(2)最大负偏差:混合物存在着最高沸点,如盐酸-水体系,如图1(b)所示。
(3)最大正偏差:混合物存在着最低沸点,如正丙醇-水体系,如图1(c)所示。
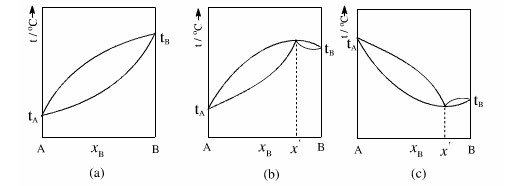
图1完全互溶双液系统的气-液平衡相图
在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气-液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加、液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。压力不同,同一双液系统的相图不同,恒沸点及恒沸组成也不同。
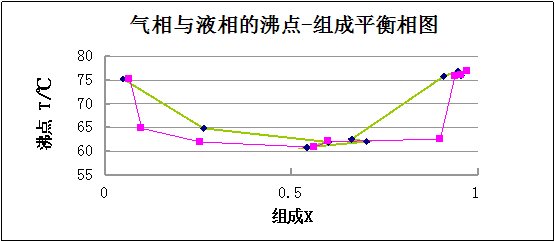
本实验采用回流冷凝的方法绘制乙醇-环己醇体系的T-XB图。该体系属于上述第三种类型,在沸点仪中蒸馏不同组成的混合物,测定气沸点及相应的气、液二相的组成,即可作出T-X相图。
本实验中两相的成分分析均采用折光率法。
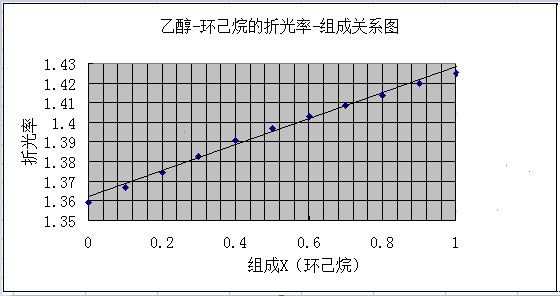
折光率是物质的一个特征数值,它与物质的浓度及温度有关,溶液的浓度、组成不同,折光率也不同。因此可先配制一系列已知组成的溶液,在恒定温度下测其折光率,作出折光率-组成工作曲线,便可通过测折光率的大小在工作曲线上找出未知溶液的组成。
三、 实验仪器和试剂:
仪器:WAY型阿贝折射仪1台;带有冷凝管的沸点仪1台;数字式温度计1台;长、短胶头滴管若干;移液枪,异丙醇,环己烷,。
试剂:异丙醇(AR);环己烷(AR)
四、 实验步骤与数据记录:
1. 已知浓度混合液折射率的测定
取异丙醇和环己烷,以及环己烷摩尔分数分别为0.2、0.4、0.6、0.8四种组成的混合液,在25度室温下,逐次用阿贝折射仪测定其折射率,并绘制组成-折射率的关系曲线。
2. 测定异丙醇-环己烷体系的沸点与组成的关系
(1)安装好沸点仪,打开冷却水,由进样口加入25 ml异丙醇,通电电压为10mV,是液体沸腾,回流并观察温度计的变化,待温度恒定,记录沸腾温度。然后将加热电压调至零处,停止加热。充分冷却后,用长吸管从气相冷凝管取样口吸取气相样品,把所取的样品迅速滴入阿贝折射仪中,测其折射率ng。将阿贝折射仪镜面用洗耳球吹干,用另一支短吸管从沸点仪进样口吸取一滴溶液,测其折射率nl。
按照上述方法依次测定加入1 mL、2 mL、3 mL、4 mL、5 mL、10 mL时各液体混合物的沸点及气-液平衡时的气、液相折光率。
(2)将蒸馏瓶内的液体回收,利用25 mL环己烷清洗,然后取25ml环己烷,注入蒸馏瓶内,按照(1)的步骤进行,以后分别加入0.2 mL、0.3 mL、0.5 mL、1 mL、4 mL、5 mL,测定其沸点及气液的折射率。
五、 实验结果与数据处理:
表1异丙醇醇-环己烷标准溶液的折光率
表2异丙醇-环己烷混合液测定数据
六、实验讨论及误差分析:
1,测定折光率,动作应迅速,以避免样品中易挥发成分损失
2,一定要先加溶液在加热,应注意切断加热丝电源
3实验中可通过调节电加热套的温度,或调整沸点仪的高程,回流速度的快慢
4使用阿贝折射仪时,不能触及硬物,用完用洗耳球吹干
七、实验思考题:
1、作出工作曲线的目的是什么?
答:可以更清楚明了地知道液相、气相的折射率与组成直接的关系,两种的温度需要保持一致,否则对折射率会有较大影响。
2、在连续测定法实验中,样品的加入量必须十分精确吗?为什么?
答:因为实验的目的就是测定其折射率和组分的关系,只有样品足够纯,不一定使加入量必须十分精确,其结果不受影响。
3、为何测定纯物质沸点时要求蒸馏瓶必须是干的,而测混合液沸点和组成时则可不必要求蒸馏瓶是干的?
答:测定纯样时,如沸点仪不干净,所测沸点就不是纯样的沸点。测定混合样时,其沸点和气、液组成都是实验直接测定的,绘制图像时只需要这几个数据,并不需要测试样的准确组成,也跟试样的量无关。
实验操作见附件视频:


