沉淀的溶解和转化
上一节
下一节
若难溶性强电解质解离生成的离子,与溶液中存在的另一种沉淀剂结合而生成一种新的沉淀,我们称该过程为沉淀的转化。
例如:白色 PbSO4 沉淀和其饱和溶液共存于试管中,向其中加入Na2S 溶液并搅拌,观察到的现象是沉淀变为黑色¾¾ 白色的 PbSO4 沉淀转化成黑色的 PbS沉淀。这就是由一种沉淀转化为另一种沉淀的转化过程。
此过程可表示为:
由一种难溶物质转化为另一种更难溶的物质,过程是较容易进行的。我们来讨论转化的条件,若上述两种沉淀溶解平衡同时存在,则有

反过来,由溶解度极小的PbS转化为溶解度较大的PbSO4 则非常困难。从上面的讨论中可以看出,只有保持 [ SO42-] 大于 [ S2-] 的 3.2×1019 倍时,才能使 PbS转化为 PbSO4 。这样的转化条件等于告诉我们这种转化是不可能的。实际上要完成PbS向 PbSO4 转化,是通过氧化反应实现的。
如果两种沉淀的 Ksp值比较接近,倍数不大,由一种溶解度较小的沉淀物转化为溶解度较大的沉淀物,还是有可能的,也才是有意义的。例如
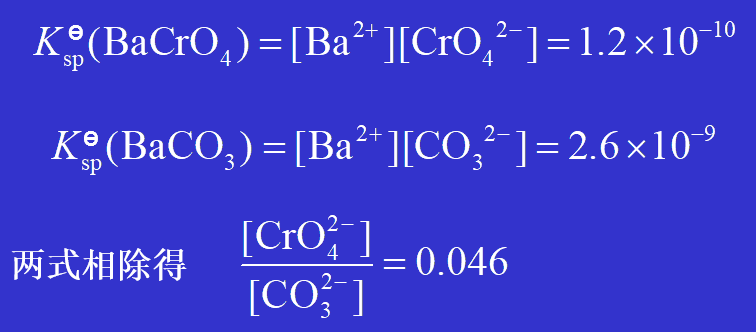
这说明只要能保持 [ CrO42-] > 0.046 [ CO32-],则BaCO3 就会转变为BaCrO4 ;反过来,只有保持 [ CO32-] 大于 [ CrO42-] 的 22 倍时,才能使BaCrO4 转化为BaCO3 ,这样的转化条件在实验室中是可以实现的。




