善待实验动物是指在饲养管理和使用实验动物过程中,要采取有效措施,使实验动物免遭不必要的伤害、饥渴、不适、惊恐、折磨、疾病和疼痛,保证动物能够实现自然行为,受到良好的管理与照料,为其提供清洁、舒适的生活环境,提供充足的、保证健康的食物、饮水,避免或减轻疼痛和痛苦等。
善待实验动物包括倡导“减少、替代、优化”的 “3R”原则,科学、合理、人道地使用实验动物。
实验动物应用过程中,应将动物的惊恐和疼痛减少到最低程度。实验现场避免无关人员进入。在符合科学原则的条件下,应积极开展实验动物替代方法的研究与应用。 在对实验动物进行手术、解剖或器官移植时,必须进行有效麻醉。术后恢复期应根据实际情况,进行镇痛和有针对性的护理及饮食调理。 保定实验动物时,应遵循“温和保定,善良抚慰,减少痛苦和应激反应”的原则。保定器具应结构合理、规格适宜、坚固耐用、环保卫生、便于操作。在不影响实验的前提下,对动物身体的强制性限制宜减少到最低程度。 处死实验动物时,须按照人道主义原则实施安死术。处死现场,不宜有其他动物在场。确认动物死亡后,方可妥善处置尸体。在不影响实验结果判定的情况下,应选择“仁慈终点”,避免延长动物承受痛苦的时间。
(保定:为使动物实验或其它操作顺利进行而采取适当的方法或设备限制动物的行动,实施这种方法的过程称为保定。仁慈终点:是指动物实验过程中,选择动物表现疼痛和压抑的较早阶段为实验的终点。)
相关人员应接受实验动物基本知识和操作技能的培训,其中包括对生物安全防护知识和技能的培训,同时配备个人安全防护装备。
在使用实验动物时,应重视动物福利(animal welfare)。




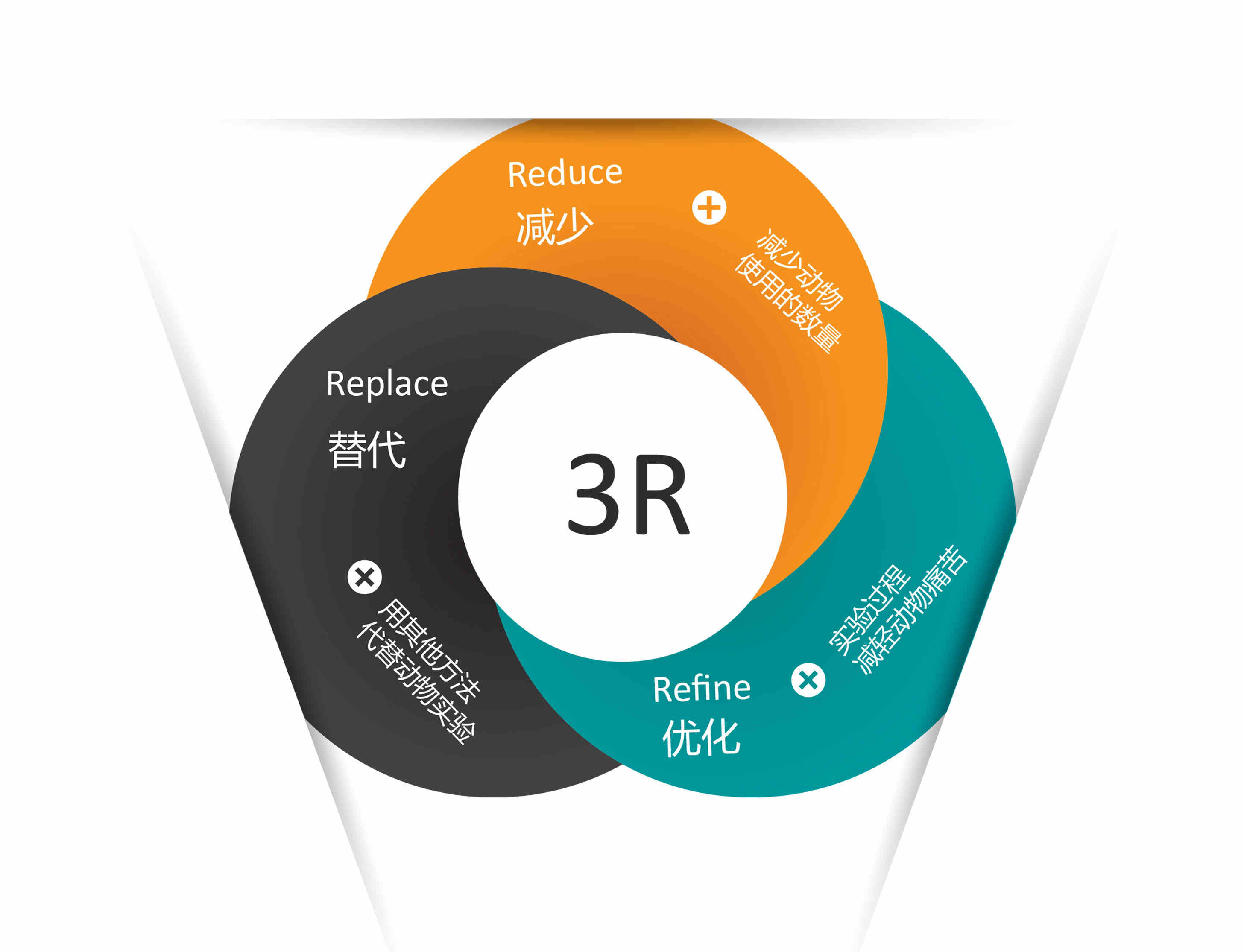
实验动物的使用应遵守3R(减少、替代、优化)原则:
减少(Reduction):是指如果某一研究方案中必须使用实验动物,同时又没有可行的替代方法,则应把使用动物的数量降低到实现科研目的所需的最小量。
替代(Replacement):是指使用低等级动物代替高等级动物,或不使用活着的脊椎动物进行实验,而采用其它方法达到与动物实验相同的目的。
优化(Refinement):是指通过改善动物设施、饲养管理和实验条件,精选实验动物、技术路线和实验手段,优化实验操作技术,尽量减少实验过程对动物机体的损伤,减轻动物遭受的痛苦和应激反应,使动物实验得出科学的结果。
严禁虐待实验动物!
有下列行为之一者,视为虐待实验动物。情节较轻者,由所在单位进行批评教育,限期改正;情节较重或屡教不改者,应离开实验动物工作岗位;因管理不妥屡次发生虐待实验动物事件的单位,将吊销单位实验动物生产许可证或实验动物使用许可证。
1、非实验需要,挑逗、激怒、殴打、电击或用有刺激性食品、化学药品、毒品伤害实验动物的;
2、非实验需要,故意损害实验动物器官的;
3、玩忽职守,致使实验动物设施内环境恶化,给实验动物造成严重伤害、痛苦或死亡的;
4、进行解剖、手术或器官移植时,不按规定对实验动物采取麻醉或其他镇痛措施的;
5、处死实验动物不使用安死术的;
6、在动物运输过程中,违反本意见规定,给实验动物造成严重伤害或大量死亡的;
7、其它有违善待实验动物基本原则或违反本意见规定的。
#科学与人文#
世界实验动物日The World Lab Animal Day,是每年4月24日。
1979年,由英国反活体解剖协会(NAVS)发起,定于每年的4月24日为“世界实验动物日”,前后一周则被称为“实验动物周”。
世界实验动物日已经受联合国认可的、国际性的纪念日,在世界各地都有动物保护者在这一天以及前后的一周举行各种活动纪念为人类健康事业做出贡献的实验动物。


