请通过本章学习,回答下列问题:
[1]B细胞的表面分子及作用?
[2]T细胞的表面分子及作用?
[3]T细胞的分类和功能?
[4]简述中性粒细胞、巨噬细胞、NK细胞、树突状细胞等固有免疫细胞的特点?
[5]抗原提呈细胞的定义和分类?
[6]简述抗原提呈的四条途径的特点?
第一节 B淋巴细胞
成熟B淋巴细胞主要定居于外周淋巴器官的淋巴滤泡内,约占外周淋巴细胞总数的20%。
一、B细胞的分化发育
B细胞在骨髓中产生、分化、发育和成熟。在此过程中主要完成两方面工作,一是特异性B细胞受体(BCR)的表达,二是B细胞自身耐受的建立。
1. BCR的表达
(1)BCR的基因结构及其重排:①所有B细胞在胚系阶段具有完全相同的BCR基因群,但以分隔的、数量多的基因片段形式存在,在发育过程中,基因需要重新排列和组合,形成大量的、特异性的、与众不同的BCR。②重链和轻链都需要基因重排,表达后再组合连接在一起,成为完整的BCR。
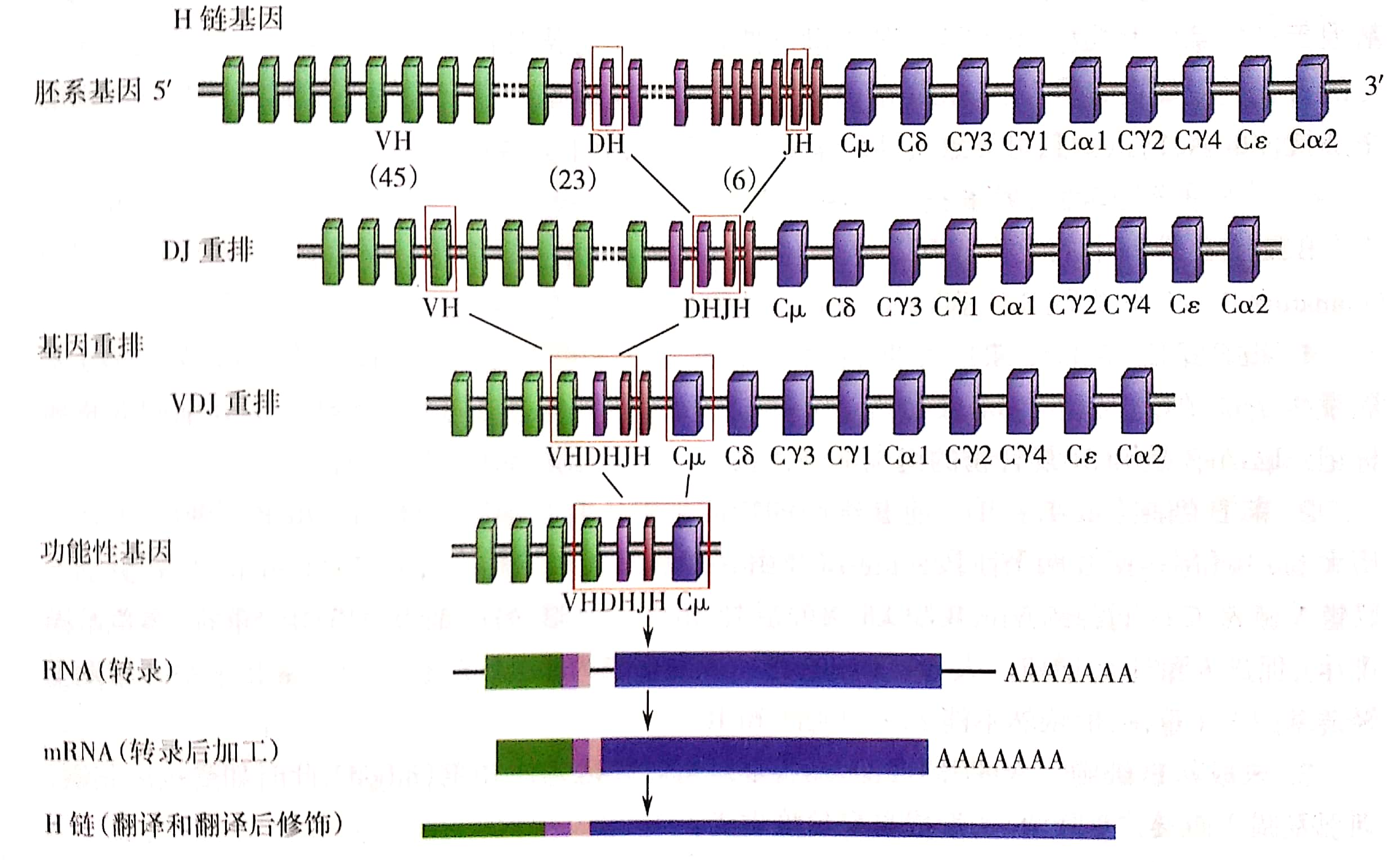
(2)BCR多样性产生机制:组合多样性、连接多样性、受体编辑、体细胞高频突变,最终BCR的多样性可达。
(3)B细胞不同发育阶段BCR的基因重排和表达
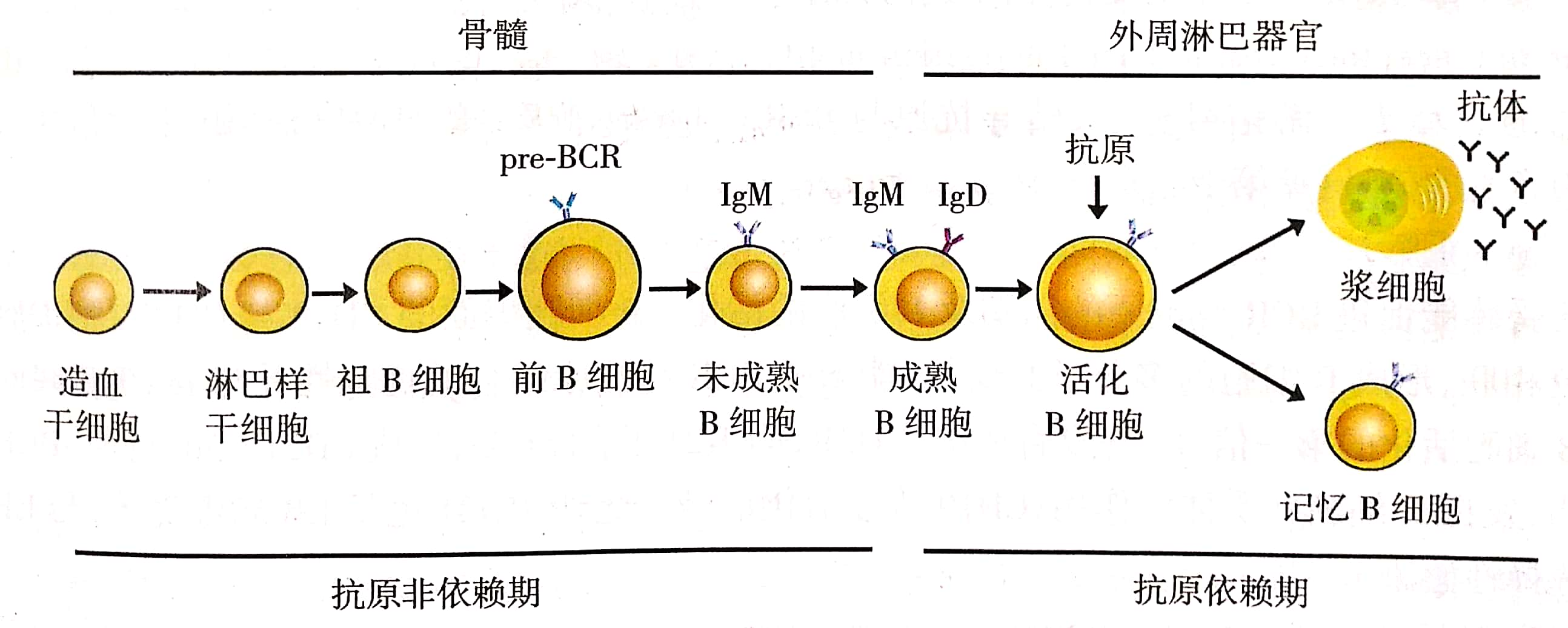
2. B细胞自身耐受的建立(阴性选择)
(1)克隆清除:B细胞发育过程中,BCR与骨髓中的自身抗原结合,导致细胞凋亡,不与自身抗原结合的BCR存活并发育成熟,成熟后的B细胞不识别自身抗原,即为自身耐受的建立。
(2)受体编辑:某些未成熟的B细胞,与自身抗原结合后,导致BCR基因被重新编辑,特异性被改变,而成为不识别自身抗原的B细胞。
(3)失能:某些未成熟的B细胞与自身抗原结合,导致BCR表达下调,这些细胞虽然未被清除,且可以进入外周免疫器官,但对抗原刺激不产生应答。
二、B细胞的表面分子及其作用
1. BCR复合物:包括BCR(mIg)和Igα/Igβ(CD79a/CD79b),识别抗原并向细胞内传递第一信号。
2. B细胞共受体:包括CD19、CD21、CD81,促进BCR对抗原的识别及B细胞的活化,辅助传递第一信号。
3. 共刺激分子
(1)CD40:组成性表达于B细胞表面,可与活化T细胞表面的CD40L结合,作为B细胞活化的第二信号;
(2)CD80(B7-1)和CD86(B7-2):静息B细胞不表达或低表达,活化B细胞表达增强,可与T细胞表面的CD28和CTLA-4相互作用,通过CD28向T细胞提供活化第二信号,通过CTLA-4抑制T细胞活化;
(3)黏附分子:包括ICAM-1(CD54)、LFA-1(CD11a/CD18)等,有助于T、B细胞间相互作用。
4. 其他表面分子:包括CD20、CD22、CD32等。
三、B细胞的分类

四、B细胞的功能
主要包括三方面,产生抗体、提呈抗原、调节免疫。
第二节 T淋巴细胞
成熟T淋巴细胞主要定居于外周淋巴器官的胸腺依赖区,约占外周淋巴细胞总数的65%~75%。
一、T细胞的分化发育
骨髓中的多能造血干细胞分化为淋巴样祖细胞,二者进入胸腺中分化、发育,最终成为成熟的T细胞。在此过程中主要完成三方面工作,一是特异性T细胞受体(TCR)的表达,二是获得MHC限制性,三是B细胞自身耐受的建立。
1. TCR的表达
(1)T细胞的发育过程
①在胸腺微环境下,T细胞发育经历了从淋巴样祖细胞到成熟T细胞的几个发育阶段,不同各阶段的T细胞表达不同的表型和功能。
②根据CD4分子和CD8分子的表达,T细胞又可分为双阴性细胞(DN细胞,两种分子都不表达)、双阳性细胞(DP细胞,两种分子都表达)、单阳性细胞(SP细胞,两种分子只表达其中之一)。
③在表型变化的同时,基因也在发生着重排。
(2)T细胞发育中TCR的基因重排:TCR的基因重排过程与BCR基因相似,构成特异性TCR两条链的β和α两个基因群分别重排,最终两条链组装成完整的TCR,表达于未成熟T细胞表面。通过组合多样性和连接多样性,最终TCR的多样性可达。
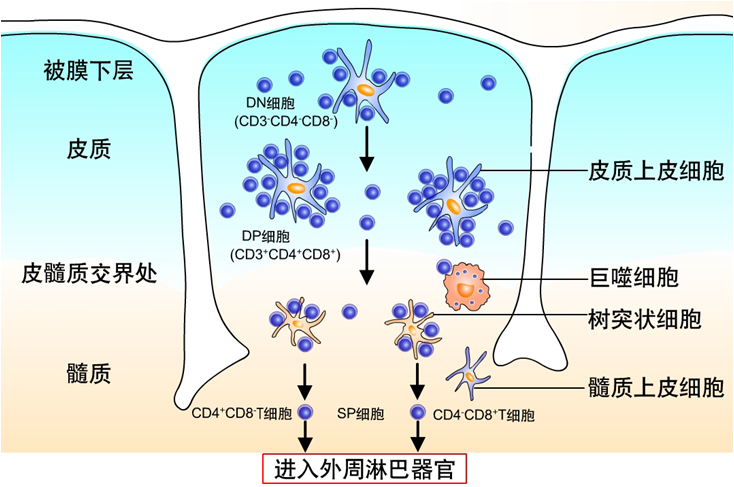
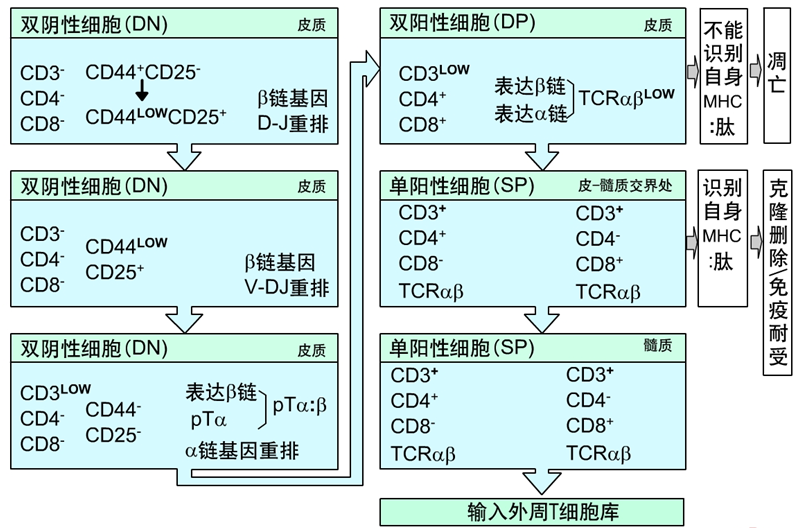
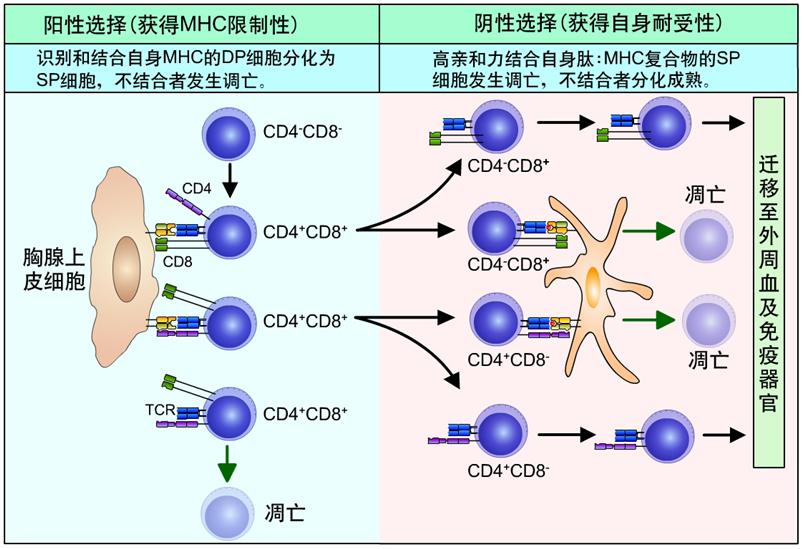
2. T细胞MHC限制性的获得(阳性选择):能与MHC分子结合的T细胞存活,不能结合的T细胞凋亡。
(1)一方面保证了所有存活细胞都可以识别MHC分子,从而能被MHC分子提呈的抗原激活,T细胞从此不能识别天然抗原,只识别MHC分子上的抗原肽,此即为MHC限制性;
(2)另一方面,双阳性T细胞上CD4分子或CD8分子随机的与MHC的Ⅱ类分子或Ⅰ类分子结合,一旦结合则保留该分子,而关闭另一分子表达,T细胞发育成为单阳性细胞,只表达CD4分子或只表达CD8分子,表达不同分子的T细胞功能也完全不同。
3. T细胞自身耐受的建立(阴性选择):能与MHC提呈的自身抗原肽结合的T细胞凋亡,不结合的存活。
(1)经过阳性选择后,T细胞都能与MHC分子结合,即获得了T细胞识别抗原的功能,但仍需确保功能正常。
(2)胸腺微环境将自身抗原肽提呈于MHC分子上,再次让T细胞识别,对自身抗原肽视而不见者可存活,结合者则被凋亡,经过阴性选择,确保了所有存活的T细胞均不能识别自身抗原肽,也不会引起自身免疫。
二、T细胞的表面分子及其作用
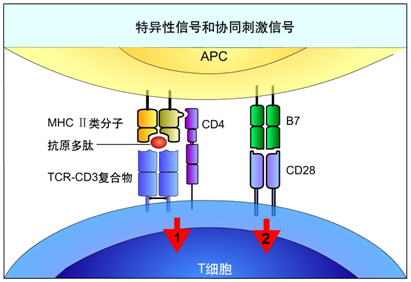
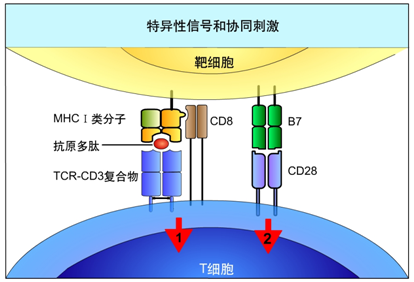
1. TCR复合物:包括TCR和CD3分子,TCR识别MHC抗原肽后,由CD3分子向细胞内传递第一信号。
2. T细胞共受体:包括CD4分子或CD8分子,用于辅助TCR对MHC抗原肽的识别以及T细胞活化信号的转导。成熟T细胞只表达CD4分子或CD8分子之一,分别称为CD4+T细胞和CD8+T细胞,前者与表达HLAⅡ类分子的抗原提呈细胞结合介导辅助功能,后者与表达HLAⅠ类分子的有核靶细胞结合介导杀伤功能。
3. 共刺激分子:为T细胞活化提供第二刺激信号,主要为CD28家族成员(下述前四种分子,活化或抑制)。
(1)CD28:可与抗原提呈细胞上的CD80和CD86结合,接受信号刺激,促进T细胞增殖和分化。
(2)CTLA-4(CD152):与CD28结合的配体相同,但亲和力更高,介导相反的抑制性作用。
(3)ICOS:诱导共刺激分子,配体为ICOSL,促进活化T细胞多种细胞因子的产生,促进T细胞增殖。
(4)PD-1:程序性死亡受体-1,与配体PD-L1和PD-L2结合,抑制T细胞和B细胞的增殖。
(5)CD40L(CD154):与抗原提呈细胞上的CD40分子结合,具有双向激活作用。
(6)黏附分子:LFA-1与ICAM-1互为配体受体,介导细胞间的黏附作用。
4. 其他表面分子:CD2、丝裂原受体等。
三、T细胞的分类和功能
1. 根据活化阶段分类:可分为初始T细胞、效应T细胞、记忆T细胞。
2. 根据TCR类型分类

3. 根据CD分子亚群分亚群
(1)CD4+T细胞:占60%~65%,分化为Th细胞,少数CD4+T细胞也具有细胞毒和免疫抑制作用。
(2)CD8+T细胞:占30%~35%,分化为细胞毒性T细胞(CTL),具有杀伤靶细胞作用。
4. 根据功能特征分亚群
(1)辅助性T细胞(Th):即CD4+T细胞,未受刺激时为Th0,受不同刺激可分化为不同的T细胞。
①Th1:胞内病原体、肿瘤抗原、IL-12、IFN-γ→Th0→Th1→IFN-γ、TNF、IL-2→Th1、Mφ、NK、CTL
②Th2:普通细菌、可溶性抗原、IL-4→Th0→Th2→IL-4、IL-5、IL-10、IL-13→Th2、B
③Th3:TGF-β、IL-4、IL-10→Th0→Th3→TGF-β→免疫抑制作用
④Th17:TGF-β、IL-17→Th0→Th17→IL-17、IL-21、IL-22、IL-26、TNF-α→固有免疫、自身免疫
⑤Tfh:TGF-β、IL-2→Th0→Tfh→IL-21→辅助B细胞应答(B细胞分化为浆细胞、抗体产生、类别转换)
(2)细胞毒性T细胞(CTL):即CD8+T细胞,通过两种方式杀伤靶细胞。
①颗粒酶、穿孔素:分泌穿孔素、颗粒酶、颗粒溶素、淋巴毒素等直接杀伤。
②凋亡途径:Fas/FasL途径诱导靶细胞凋亡。
(3)调节性T细胞(Treg):即CD4+CD25+Foxp3+T细胞,主要通过两种方式进行免疫应答负调控。
①直接接触抑制靶细胞活化。
②分泌TGF-β、IL-10等细胞因子抑制免疫应答。
第三节 固有免疫细胞
一、吞噬细胞
吞噬细胞包括中性粒细胞、单核/巨噬细胞和树突状细胞。
1. 中性粒细胞:小吞噬细胞、寿命短(2~3天)、更新快(1×个/分钟,1×
个/天)、数量多(占白细胞总数60%~70%),具有强大的趋化、吞噬和杀菌能力,包括氧依赖杀菌系统(氧氮中间物)、氧非依赖系统(各种酶)、MPO杀菌系统(MPO、过氧化氢、氯化物)。
2. 单核/巨噬细胞:单核细胞由骨髓进入血液,停留数小时至数日,进入组织器官,发育为巨噬细胞,寿命可达数月。组织中的巨噬细胞不再返回血液,但可在组织中定居或游走。具有多种重要的生物学功能,包括杀伤清除病原体、杀伤胞内菌和肿瘤细胞、参与炎症反应、提呈抗原、免疫调节等。

3. 吞噬细胞的生物学功能
(1)募集和迁移:①穿出血管:局部血管内皮细胞黏附分子表达增加,吞噬细胞黏附并穿越血管内皮渗出至组织间隙。②定向移动:吞噬细胞沿着趋化因子浓度梯度向感染灶定向移动。
(2)识别:吞噬细胞表达多种表面受体,可识别微生物及分泌产物,统称为模式识别受体(PRR)。主要包括甘露糖受体、清道夫受体、Toll样受体等,以及IgG Fc受体、补体受体等。
(3)吞噬:微生物与受体结合,通过内化而被摄入细胞内,形成内体,再与溶酶体融合成为吞噬溶酶体。
(4)杀菌:吞噬溶酶体内,微生物通过氧依赖(中间氧或中间氮)或氧非依赖途径(乳酸、溶菌酶、防御素、蛋白水解酶等)被杀伤。
(5)消化和清除:病原体被消化和降解后,通过胞吐作用排除胞外,部分被MHC分子提呈。
二、NK细胞
1. NK细胞的一般特征
(1)基本特征:无TCR或BCR,内含嗜苯胺颗粒,又称大颗粒淋巴细胞(LGL)。
(2)来源及分布:骨髓内产生和分化,功能却与CTL细胞相似;主要分布于外周血、脾和肝。
(3)表面标志:缺少特异性标志。①CD16:一种低亲和力IgG Fc受体(FcεRⅢ),中性粒细胞和嗜碱性粒细胞也表达;②CD56:也表达于T细胞。目前将TCR-mIg-CD56+CD16+表型的淋巴样细胞鉴定为NK细胞。
2. NK细胞的杀伤功能相关的受体:NK细胞表达对其杀伤作用有正负调节作用的两类受体,即活化性杀伤受体(AKR)和抑制性杀伤受体(IKR),两种受体都能结合自身MHCⅠ类分子,抑制性受体亲和力高占优势。
3. NK细胞的主要生物学功能:抗细胞内感染、抗肿瘤、免疫调节等。
三、树突状细胞
1. DC的生物学特征:表达模式识别受体,胞内无溶酶体,有髓系来源和淋巴系来源。
(1)DC前体细胞:无DC表型和功能(单核细胞即为髓样DC的前体),经血液和淋巴循环进入组织器官,在感染、炎症、细胞因子等刺激下发育为未成熟DC。
(2)未成熟DC:多数DC处于未成熟状态,高表达模式识别受体,抗原摄取加工能力强,低表达MHCⅡ类分子、共刺激分子和黏附分子,提呈和激活能力弱,受刺激后由组织向外周淋巴器官迁移,并发育为成熟DC,功能翻转。
(3)成熟DC:表面有许多树突样突起,低表达模式识别受体,抗原识别和摄取能力减弱;高表达MHCⅡ类分子、共刺激分子和黏附分子。
2. DC的分类
(1)根据DC来源分类:髓样DC(MDC)/常规DC(cDC)和淋巴样DC(LDC)/浆细胞样DC(pDC)。
(2)根据DC分布分类:滤泡状DC(FDC)、并指DC(IDC)、胸腺树突状细胞、郎格汉斯细胞(LC)、间质树突状细胞、循环树突状细胞。
3. DC的生物学功能:提呈抗原、激活初始T细胞、参与T细胞分化发育、诱导免疫耐受、参与免疫调节等。
四、固有免疫样淋巴细胞
主要包括B1细胞、γδT细胞、NKT细胞等。
五、其他免疫相关细胞
主要包括嗜酸性粒细胞、嗜碱性粒细胞、肥大细胞、红细胞、血小板等。
第四节 抗原提呈细胞
一、抗原提呈细胞的种类与特点
1. 抗原提呈细胞(APC):能摄取、加工、处理抗原,将抗原信息提呈给T细胞。
2. 抗原提呈细胞的分类
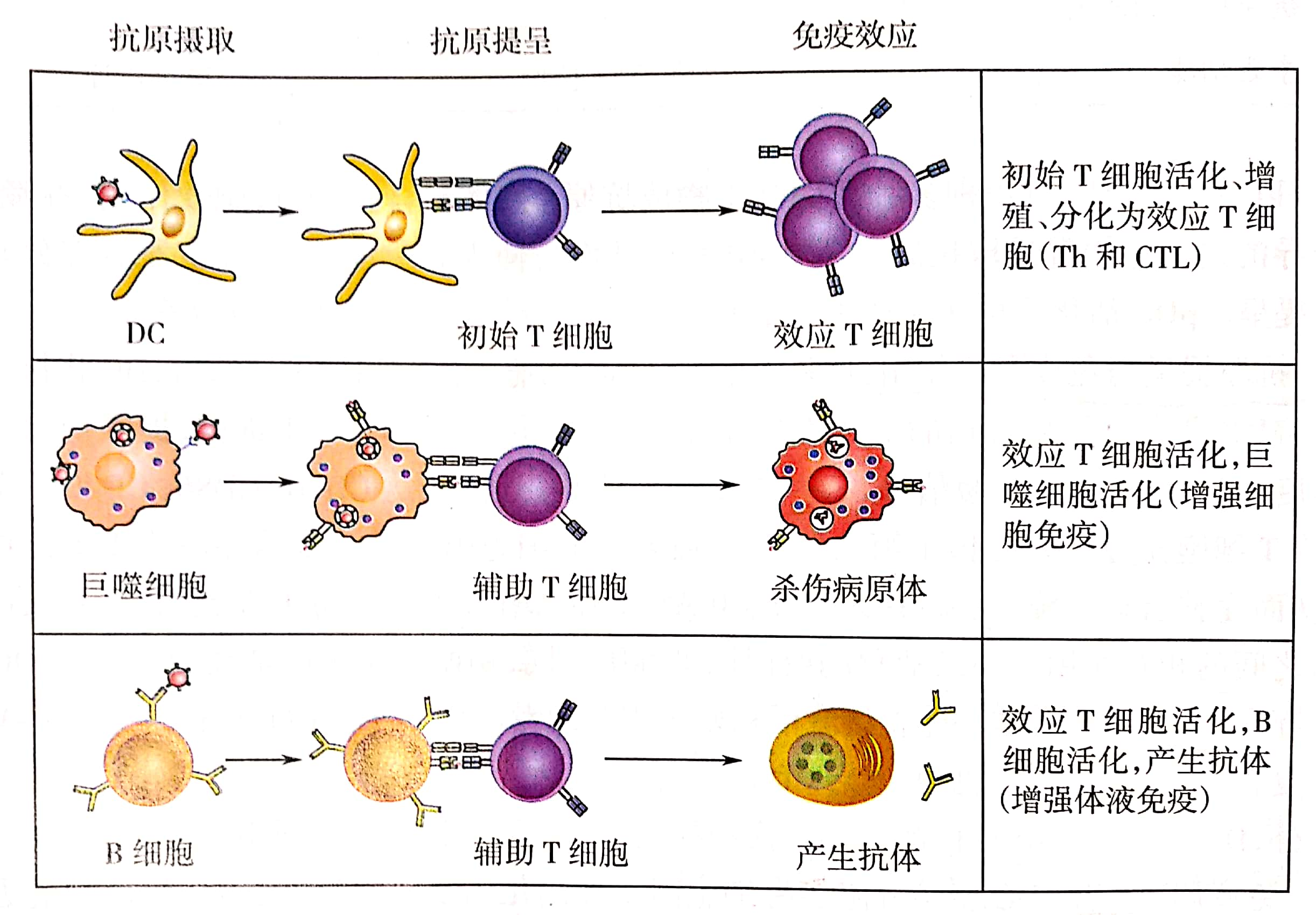
(1)专职APC:能组成性表达MHCⅡ类分子、共刺激分子和黏附分子,包括DC、Mφ和B细胞。
(2)非专职APC:通常不表达或低表达MHCⅡ类分子等,但在炎症或细胞因子作用下,可被诱导表达,包括内皮细胞、上皮细胞、成纤维细胞、活化的T细胞等。
(3)广义APC:所有表达MHCⅠ类分子的细胞,都能对内源性抗原加工处理和提呈,也可被认为是APC。
二、抗原提呈细胞对抗原的加工和提呈
1. 提呈抗原的分类:根据所提呈抗原的来源不同,可分为外源性抗原(来源于细胞外的抗原)和内源性抗原(来源于细胞内的抗原),两类不同的抗原,提呈过程、激活细胞、产生效应等完全不同。
2. 提呈抗原的途径
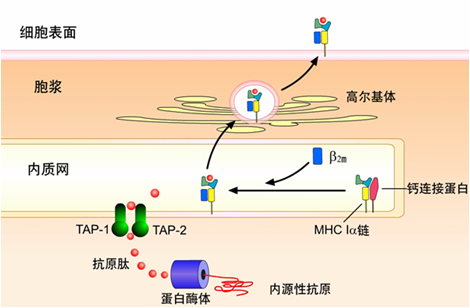
(1)经典MHCⅠ类分子抗原提呈途径(胞质溶胶提呈途径):内源性蛋白抗原→蛋白酶体降解→TAP转运至ER内→形成抗原肽-MHCⅠ类分子复合物→经高尔基体转运至细胞膜上→供CD8+T细胞识别
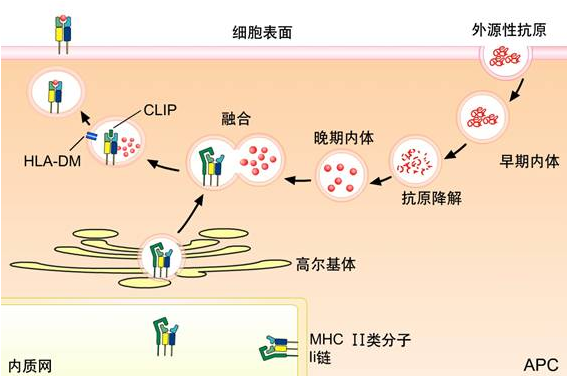
(2)经典MHCⅡ类分子抗原提呈途径(溶酶体提呈途径):APC摄取外源性抗原→形成内体/吞噬体→与溶酶体融合→抗原被降解为多肽→转运至MⅡC→置换MHCⅡ类分子抗原结合槽内CLIP→形成抗原肽-MHCⅡ类分子复合物→转运至APC膜表面→提呈给CD4+T
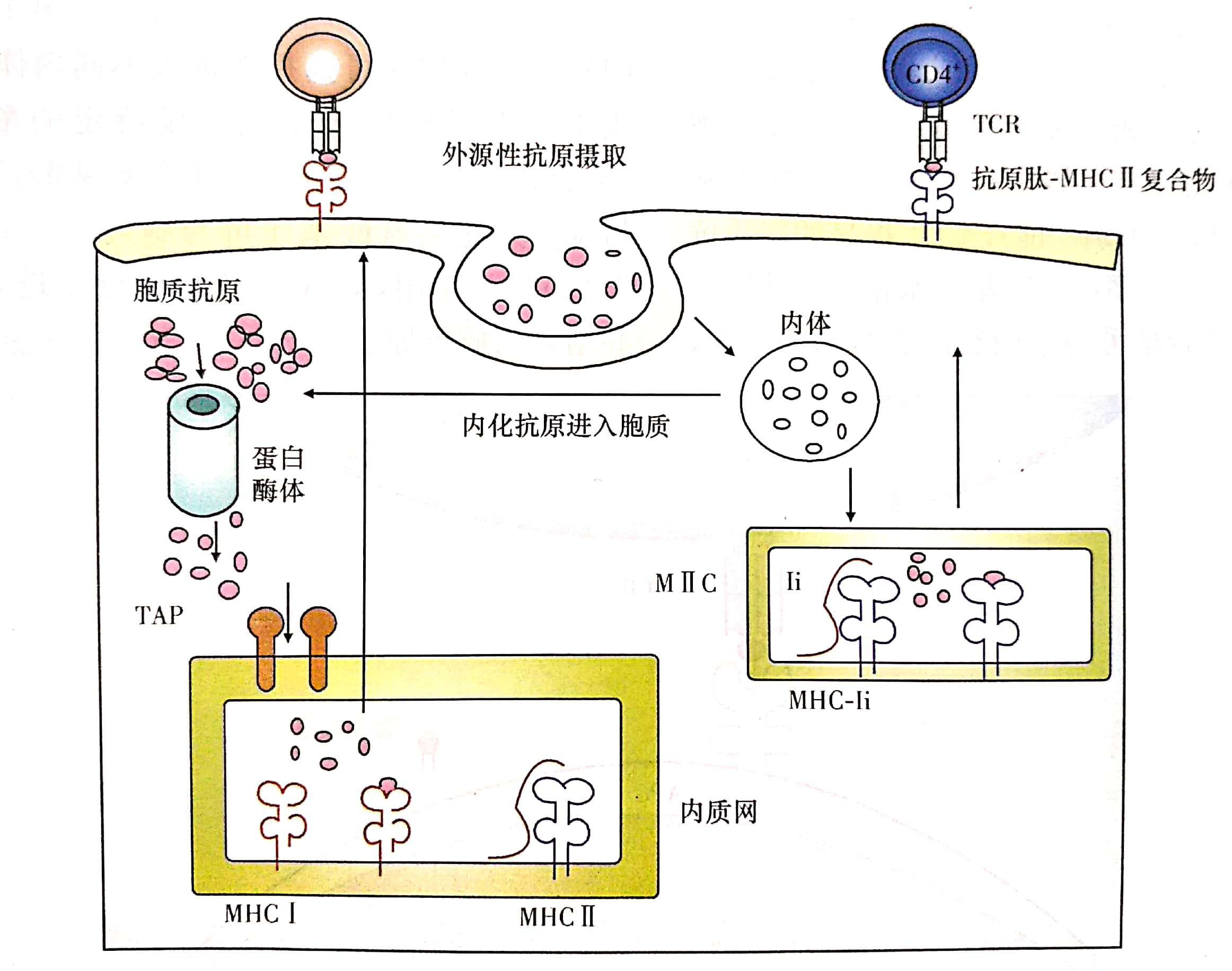
(3)非经典抗原提呈途径(交叉提呈途径):APC将外源性抗原提呈给MHCⅡ类分子,将内源性抗原提呈给MHCⅠ类分子,交叉提呈不是主要提呈方式,但在抗感染免疫、肿瘤免疫及自身耐受维持中发挥作用。
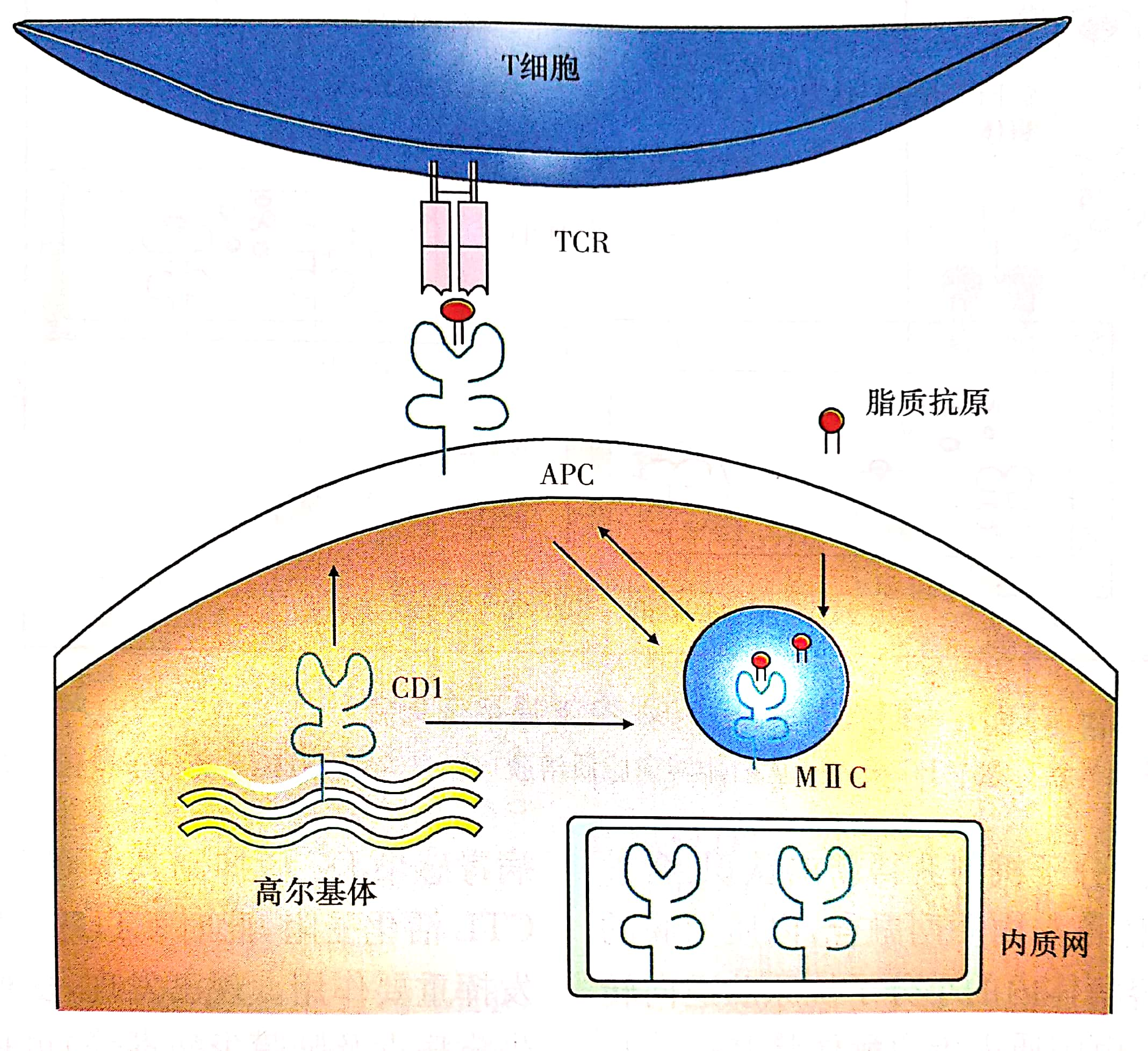
(4)非MHC分子CD1提呈途径(脂类抗原提呈途径):脂类抗原不是蛋白多肽,不能结合MHC分子,但能结合APC中的CD1分子而被提呈。