第二节 气体的交换与运输
一、气体交换
(一)气体交换原理
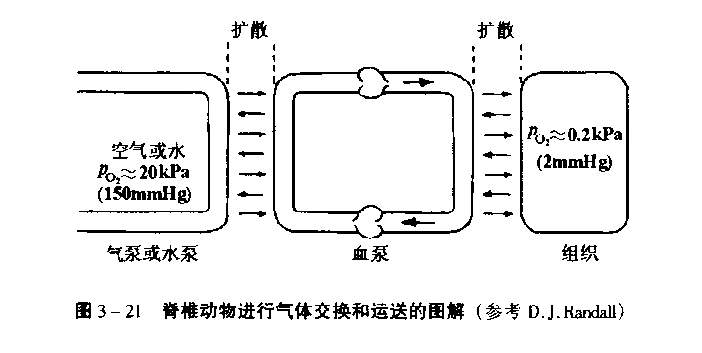
气体交换是通过物理性扩散实现的,气体分压差是气体的交换的动力。
PO2:水 › 血液 › 组织
PCO2:水 ‹ 血液 ‹ 组织
(二)气体交换过程
动物的气体交换包括两个过程:1、呼吸器官内的气体交换;2、组织内的气体交换
(三)影响呼吸器官内气体交换的因素
1、呼吸膜的厚度;
2、呼吸膜的面积;
3、气体分压差;
4、气体的溶解度和相对分子质量。
二、气体运输
经过气体交换后,进入血液的气体首先溶解于血液中,然后才进一步成为化学结合状态,溶解气体和结合气体之间保持着一定的动态平衡。两步气体交换的中间一步过程是气体在血液中的运输。
(一) 氧的运输
1、血红蛋白的氧合作用
化学结合:98%;物理溶解:2%

氧容量:100ml血液中,血红蛋白结合氧的最大量。随鱼种不同,氧容量在4-20ml变动。
氧含量:血红蛋白实际结合的氧量。
氧饱和度:一定氧分压下血红蛋白的氧含量与氧容量的百分比。
2、氧离曲线
(1)概念:血红蛋白氧饱和度与氧分压的关系曲线。
(2)形态及产生原因
氧离曲线为S形。
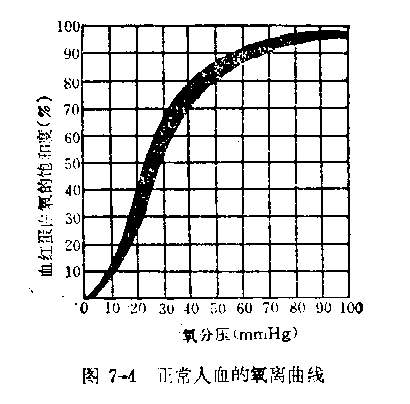
S形氧离曲线的形成机制分析如下:
1、血红蛋白分子结构特征
血红蛋白分子由两条α链和两条β链组成,是一个含有两种不同亚基的四聚体。每一个亚基含有一个血红素辅基。2个α亚基之间有一个4个盐键,α亚基和β亚基之间各有一个盐键,β亚基内部各有一个盐键。这些盐键约束血红蛋白分子的立体构型,使之稳定,不易与氧结合。

2、血红蛋白与氧结合的方式
当一个α亚基的Fe2+与氧结合后,Fe2+的直径发生了变化,改变了它与卟啉环的相对位置关系,并进而引起整个亚基三级结构的变构现象,结果使2个α亚基之间的2个盐键断裂。若2个α亚基与氧结合,则会使α亚基之间的4个盐键全部断裂,并进而使α亚基与β亚基之间的盐键断裂。盐键断裂使各亚基所受的约束力减弱,对氧的亲和力增大。
当氧分压很低时,去氧血红蛋白对氧的亲和力也低,这是氧离曲线下段坡度较缓的原因。随着氧分压的升高,一部分亚基 与氧结合,由于变构效应提高了其它亚基对氧的亲和力,所以,氧离曲线的坡度变陡。氧分压继续升高时,则大部分血红蛋白都已经与氧结合,可以结合的血红蛋白所剩不多了,所以曲线坡度又变缓。
(3) 氧离曲线形态特点的生理意义
a 血红蛋白氧饱和度随氧分压升高而增大,有利于血液在鳃内结合氧;随氧分压下降而变小,有利于在组织内释放氧;
b在呼吸器官,氧分压较大。在这个范围内,氧分压有很大变化时,血氧饱和度变化不大,这样可以保证对氧的摄取。
c在组织内,氧分压较低。在这个范围内,氧分压有较小变化时,血氧饱和度变化较大,这样有利于血液向组织内释放氧。
(4) 不同鱼类氧离曲线的差异及其适应意义
不同鱼类血红蛋白对氧亲和力相差较大,氧离曲线的特点也不相同。
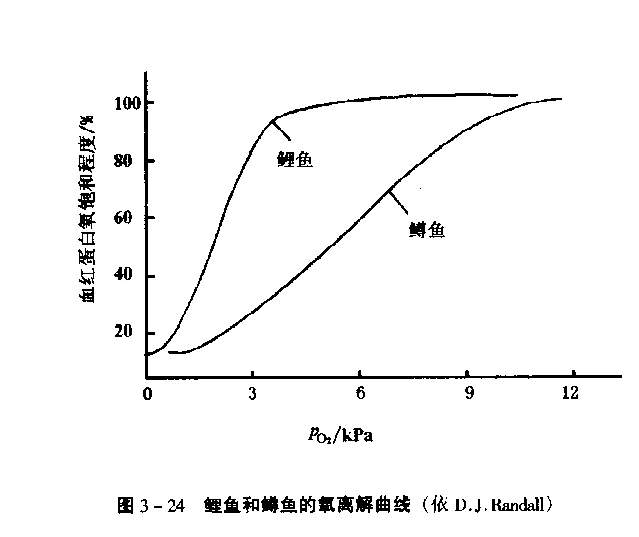
淡水鱼氧离曲线坡度陡,在低氧分压条件下即达到血红蛋白饱和,说明淡水鱼类与氧亲和力大,这与淡水溶解氧含量变动大相适应。
海水鱼类呈现S形,需在较高氧分压条件下才能达到血红蛋白饱和,说明海水鱼类血红蛋白与氧亲和力较小,这与海水环境中氧分压极为稳定相适应。
(5)影响氧离曲线的因素
a 二氧化碳分压和pH值
血红蛋白与氧的结合受血液中CO2分压和pH的影响,同一氧分压下,CO2升高或者pH值降低,使血红蛋白对氧的亲和力降低,使氧饱和度下降,氧离曲线右移,这有利于氧合血红蛋白解离,使组织获得更多的氧。反之,血液中CO2降低或者或pH升高,则血红蛋白对氧亲和力升高,曲线左移,有利于呼吸器官对氧的摄取。
血红蛋白与氧的亲和力随血液中二氧化碳分压升高或pH下降而降低的现象称为波尔效应(Bohr effect)。波尔效应大,表示少量的二氧化碳就能促使氧合血红蛋白解离,血液大量释放氧,以供组织所需。
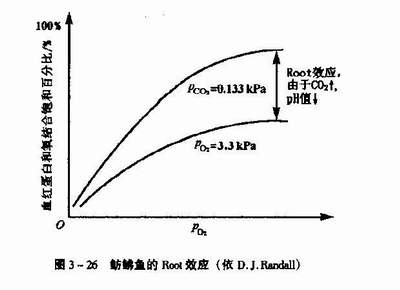
在许多鱼类,血氧容量随二氧化碳分压升高或pH值降低而下降的现象称为鲁特效应(Root effect)。这是鱼类所特有的现象。
b 温度
温度可以在高低和变化速率两方面影响氧离曲线。
温度增加可促进氧离,血红蛋白的氧饱和度下降,氧离曲线右移。温度降低提高了血红蛋白与氧的亲和力,氧饱和度增加,氧离曲线左移,其坡度也越陡。温度的影响,可能与氢离子活动有关,温度升高,氢离子活动度增大,因而降低了氧饱和度。
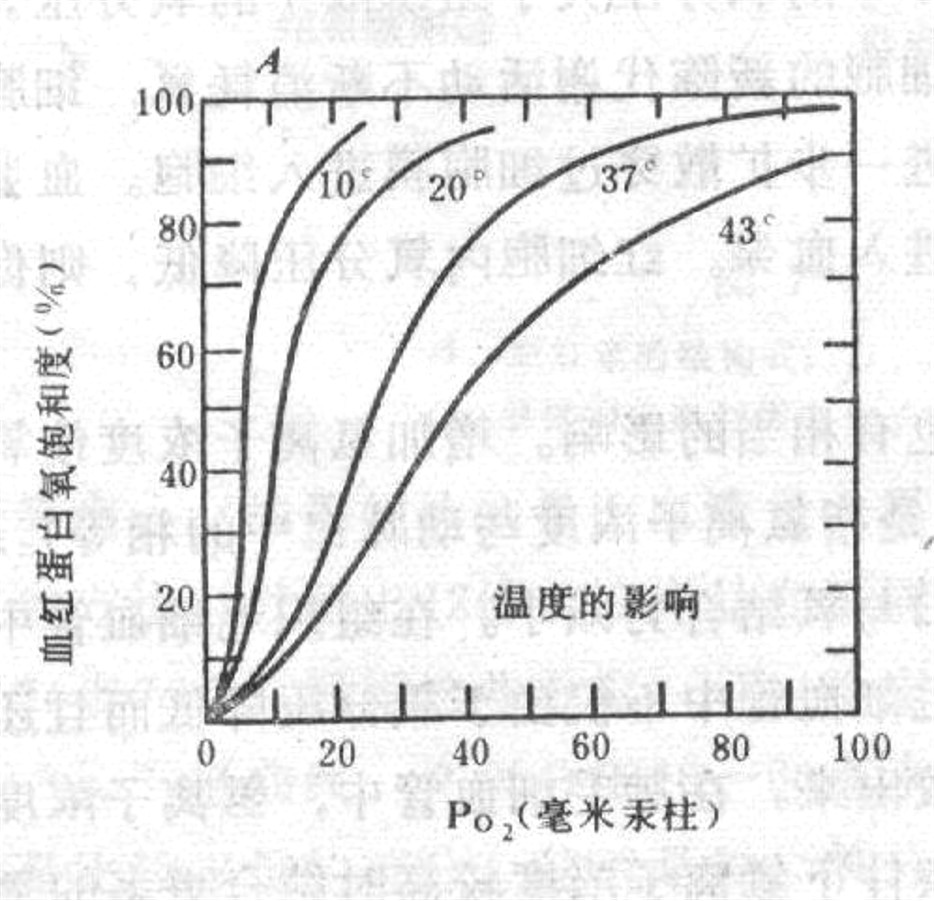
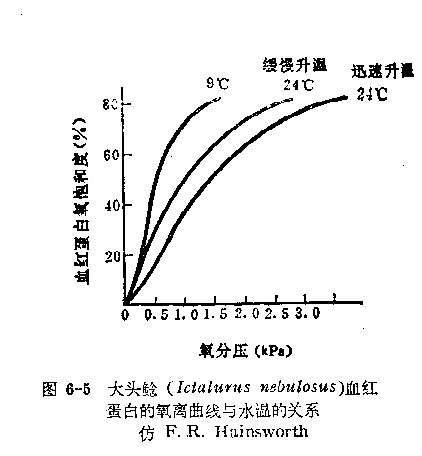
盛夏高温,使水中氧的溶解度降低,高温还使血红蛋白与氧的亲和力变小,从而使鱼容易因缺氧而浮头。
c 红细胞中二磷酸甘油酸(DPG)
红细胞中无氧代谢产生的2,3-二磷酸甘油酸与血红蛋白结合,能降低血红蛋白对O2的亲和力,有利于Hb向组织释放O2 ,这可能是机体对缺氧的适应机制之一。但DPG也妨碍了Hb在肺部与O2的结合,不利于O2的运输。
d ATP
ATP和脱氧血红蛋白α链结合而显著降低其与氧的亲和力,并且明显增加Bohr效应的幅度。
动物在缺氧条件下红细胞ATP含量降低,而使血红蛋白的氧亲和力显著增加,从而使血液在呼吸表面对氧的摄取量增加。
e Hb 自身性质的影响
血液中Hb的数量和质量直接影响运氧的能力。如受某些氧化剂(如亚硝酸盐等)的作用,Hb的Fe2+氧化成Fe3+,失去运O2能力。
f 一氧化碳(CO)
CO与Hb的结合点与O2相同,但亲和力远高于O2 ,为O2的250倍。
(二)二氧化碳运输
进入血液循环的CO2以溶解和化学结合两种方式运输,但以结合态为主,约占总量的95%,化学结合态CO2有两种形式,碳酸氢盐和氨基甲酸血红蛋白,并以前者为主。
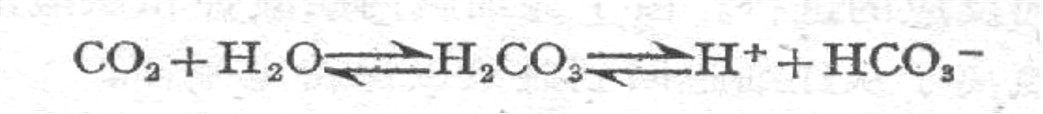
![]()
1、碳酸氢盐形式的运输
碳酸氢盐运输形式有两种:1、血浆中的碳酸氢钠;2、红细胞中的碳酸氢钾。
A 合成
合成部位:组织。碳酸氢根主要在红细胞形成,然后扩散至血浆。
(1) 少量二氧化碳物理性溶解于血浆中,一部分与血浆蛋白结合,大部分扩散至红细胞内。
(2) 进入红细胞的二氧化碳一部分在碳酸酐酶作用下生成碳酸,进而解离为碳酸氢根和氢离子;一部分与去氧血红蛋白结合成氨基甲酸血红蛋白;另一部分生成碳酸后与去氧血红蛋白钾盐作用生成还原血红蛋白和碳酸氢钾。碳酸氢钾再解离成钾离子和碳酸氢根。
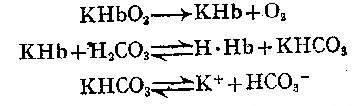
(3) 碳酸氢根透膜进入血浆,钾离子不能同时透出,血浆氯离子进入红细胞作为交换(氯转移),这样,血浆中形成了碳酸氢钠,仅小部分碳酸氢钾留在红细胞中。
B 分离
分离部位:呼吸上皮。
以上反应均为可逆反应。决定反应方向的是毛细血管两侧的CO2分压差。在呼吸器官,CO2分压低,细胞内碳酸酐酶促使碳酸分解为CO2和H2O,于是CO2透过红细胞膜到血浆,再通过呼吸上皮扩散到空气(水)中。
在血液入肺(鳃)时,血中的还原血红蛋白较多,氧与之结合,生成氧合血红蛋白,后者与碳酸氢钾作用生成碳酸和氧合血红蛋白钾盐,由于上述反应可逆,利于向空气(水)中释放二氧化碳。
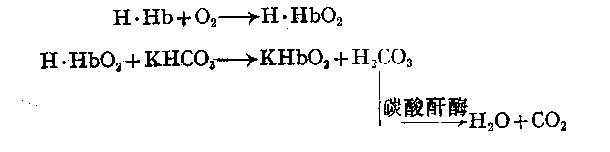
血液出肺(鳃)时,血中的氧合血红蛋白钾盐较多解离生成血红蛋白钾盐,向组织释放氧,同时血红蛋白钾盐与碳酸作用,有利于吸收组织中的二氧化碳。
血红蛋白的氧合作用对碳酸氢根合成与分离的调节作用称为海登效应(Haldane effect)。
C 二氧化碳运输与血液酸碱平衡
血液在组织处结合二氧化碳时的化学反应,如碳酸的生成和解离,氨基甲酸血红蛋白的生成和解离,均会导致产生许多H+,使血液的pH值降低;在呼吸器官,情况又相反,反应使pH值升高。但实际上,血液在运输二氧化碳的过程中,pH值变化并不大。这是因为血液本身具有缓冲酸碱度变化的能力。
血红蛋白是一种两性电解质,既可以表现为酸性,又可以表现为碱性。血红蛋白与氧结合时,其珠蛋白中的一些基团,如组氨酸残基的咪唑基就会解离,放出H+ ,因此氧合血红蛋白的酸性强些;当氧合血红蛋白释放氧而成为去氧血红蛋白时这些基团又可接受H+,故去氧血红蛋白的碱性强些。
在组织毛细血管中,二氧化碳进入血液发生化学反应,使血液趋于酸性,但此时正是氧合血红蛋白释放氧而成为去氧血红蛋白,碱性增强,可接受所生成的H+,缓冲了pH值的变化,并促进了二氧化碳的吸收;
在呼吸器官毛细血管中,二氧化碳的排出导致pH值升高,但此时正是血红蛋白与氧结合,放出H+,又起到了缓冲作用。
血液在运输二氧化碳的过程中,pH值保持相对稳定的主要原因在于血液中存在着H2CO3—HCO3—缓冲对。血液中的NaHCO3的含量被称为血液的碱储藏。 血液中的其它缓冲对也对血液的pH值相对稳定起了一定作用。
2、氨基甲酸血红蛋白形式的运输
反应主要受血红蛋白氧合作用的调节。在相同二氧化碳分压时,还原血红蛋白与二氧化碳结合形成氨基甲酸血红蛋白的能力比氧合血红蛋白的能力大。
在组织,血液中的氧合血红蛋白解离成还原血红蛋白,给组织提供氧,还原血红蛋白则与组织细胞释放的二氧化碳结合成氨基甲酸血红蛋白,有利于组织吸收氧气;
在呼吸器官,还原血红蛋白与氧结合生成氧合血红蛋白,促进氨基甲酸血红蛋白解离,利于释放二氧化碳。


