氧化-还原反应
氧化-还原反应是化学反应前后,元素的氧化数有变化的一类反应。 氧化还原反应的实质是电子的得失或共用电子对的偏移。 氧化还原反应是化学反应中的三大基本反应之一(另外两个为(路易斯)酸碱反应与自由基反应) 。自然界中的燃烧,呼吸作用,光合作用,生产生活中的化学电池,金属冶炼,火箭发射等等都与氧化还原反应息息相关。研究氧化还原反应,对人类的进步具有极其重要的意义。
反应历程
氧化还原反应前后,元素的氧化数发生变化。根据氧化数的升高或降低,可以将氧化还原反应拆分成两个半反应:氧化数升高的半反应,称为氧化反应; 氧化数降低的反应,称为还原反应。氧化反应与还原反应是相互依存的,不能独立存在,它们共同组成氧化还原反应。
反应中,发生氧化反应的物质,称为还原剂,生成氧化产物;发生还原反应的物质,称为氧化剂,生成还原产物。氧化产物具有氧化性,但弱于氧化剂;还原产物具有还原性,但弱于还原剂。用通式表示即为:
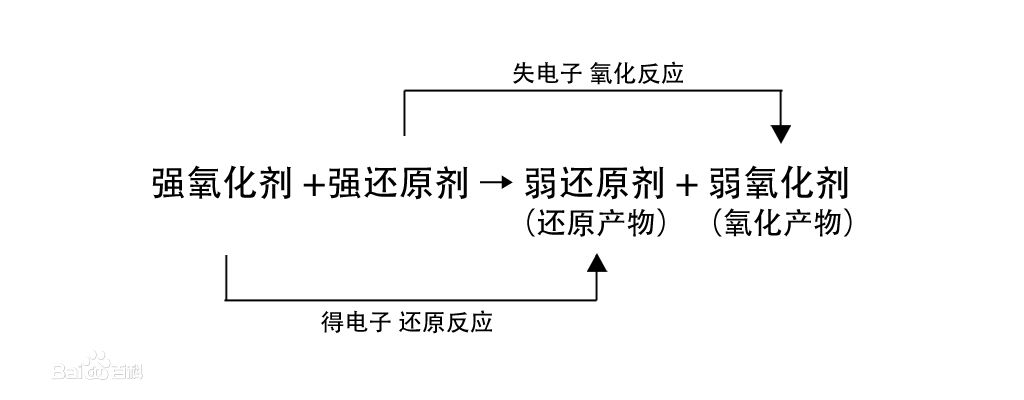
氧化还原反应的发生条件,从热力学角度来说,是反应的自由能小于零;从电化学角度来说,是对应原电池的电动势大于零。
应用与意义
氧化还原性的强弱判定
物质的氧化性是指物质得电子的能力,还原性是指物质失电子的能力。物质氧化性、还原性的强弱取决于物质得失电子的能力(与得失电子的数量无关)。
从方程式与元素性质的角度,氧化性与还原性的有无与强弱可用以下几点判定:
(1)从元素所处的价态考虑,可初步分析物质所具备的性质(无法分析其强弱)。最高价态——只有氧化性,如H2SO4、KMnO4中的S、Mn元素;最低价态,只有还原性,如Cl-、S2-等;中间价态——既有氧化性又有还原性,如Fe、S、SO2等。
(2)根据氧化还原的方向判断:
氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
(3)根据反应条件判断:
当不同的氧化剂与同一种还原剂反应时,如氧化产物中元素的价态相同,可根据反应条件的高、低进行判断,如是否需要加热,是否需要酸性条件,浓度大小等等。
需要注意的是,物质的氧化还原性通常与外界环境,其他物质的存在,自身浓度等紧密相关,通过以上比较仅能粗略看出氧化还原性大小。如欲准确定量地比较氧化还原性的大小,需要使用电极电势。
现实意义
在生物学中,植物的光合作用、呼吸作用是典型的氧化还原反应。人和动物的呼吸,把葡萄糖氧化为二氧化碳和水。通过呼吸把贮藏在食物的分子内的能,转变为存在于三磷酸腺苷(ATP)的高能磷酸键的化学能,这种化学能再供给人和动物进行机械运动、维持体温、合成代谢、细胞的主动运输等所需要的能量。
在工业生产中所需要的各种各样的金属,很多都是通过氧化还原反应从矿石中提炼而得到的。如生产活泼的有色金属要用电解或置换的方法;生产黑色金属和一些有色金属都是用在高温条件下还原的方法;生产贵金属常用湿法还原,等等。许多重要化工产品的合成,如氨的合成、盐酸的合成、接触法制硫酸、氨氧化法制硝酸、食盐水电解制烧碱等等,也都有氧化还原反应的参与。石油化工里的催化去氢、催化加氢、链烃氧化制羧酸、环氧树脂的合成等等也都是氧化还原反应。
在农业生产中,施入土壤的肥料的变化,如铵态氮转化为硝态氮等,虽然需要有细菌起作用,但就其实质来说,也是氧化还原反应。土壤里铁或锰的氧化数的变化直接影响着作物的营养,晒田和灌田主要就是为了控制土壤里的氧化还原反应的进行。
在能源方面,煤炭、石油、天然气等燃料的燃烧供给着人们生活和生产所必需的大量的能量。我们通常应用的干电池、蓄电池以及在空间技术上应用的高能电池都发生着氧化还原反应,否则就不可能把化学能变成电能,把电能变成化学能。
由此可见,在许多领域里都涉及到氧化还原反应,认识氧化还原反应的实质与规律,对人类的生产和生活都是有意义的。


